��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ij��ѧ��ȤС����ľ̿��Ũ����Ϊ��ʼԭ�ϣ�̽��һ��������������Ʒ�Ӧ�Ʊ��������ơ����װ������(����װ���п�����Ӱ��)����ش��������⣺
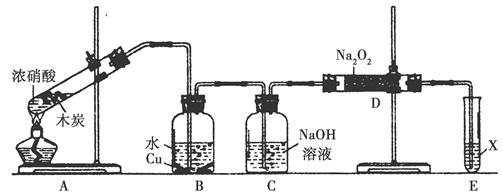
��1����װ������������е�һ�������_________________��
��2��װ��A���Թ��з�����Ӧ�Ļ�ѧ����ʽ��_______________��
��3���Ʋ�B�п��Թ۲쵽����Ҫ������________��Cװ�õ�������________��
��4��װ��D�г�����NaNO2�⣬������һ�ֹ�̬����Y��Y�Ļ�ѧʽ��________������ͨ���ʵ��Ľ���������Y���ʣ���������Ľ�������______________________��
��5����֪�������������ᣬ���ȶ��������´��ڷ�Ӧ3HNO2=HNO3��2NO����H2O����������Һ�У�NO2-�ɽ�MnO4-��ԭΪMn2�������������ɡ�
��д������D�в������������Ƶķ�����_________________��
��Eװ�����Լ�X������________��
A��ϡ����
B�����Ը��������Һ
C��ϡ����
D��ˮ
�ο��𰸣���1�����װ�õ�������
��2��C��4HNO3(Ũ)  CO2��4NO2����2H2O
CO2��4NO2����2H2O
��3��ͭƬ���ܽ⣬��Һ������������ɫ���ݡ���ȥNO�л��е�CO2
��4��NaOH����װ�м�ʯ�ҵĸ���ܴ���Cװ��
��5���ٽ������������Թ��У�����ϡ���ᣬ��������ɫ���岢��Һ���Ϸ���Ϊ����ɫ����D�в�������������(�������������Թ��У���������KMnO4��Һ������Һ��ɫ��ȥ����D�в�������������)����B
�����������3������װ��ͼ��֪��A�в�����NO2��B����ˮ��Ӧ����HNO3��NO������HNO3��ͭ��Ӧ����ͭƬ�ܽ⣬��Һ�������������ݣ�����A�л�������CO2������ͨ��D֮ǰӦ��������������Һ�����ȥ����4������NOͨ������������Һ����Dװ��ʱ�����ˮ����������ԭ���غ��֪�����ɵĹ�������Ӧ�û���NaOH����Ҫ��������NaOH��Ӧ�ó�ȥˮ��������5������������Ϣ��֪���������������ƣ����Խ�����������Һ�зֽ⣻Ҳ���Խ��������Ը��������Һ��Ӧ��
�㲦�����⿼��NO��������������������ʣ����鿼�������������������Ѷ��еȡ�
�����Ѷȣ�һ��
2��ʵ���� �������ƣ�NaNO2����¶�ڿ����л���������Ӧ���������ƣ�����ά��֯Ʒ��Ⱦɫ��Ư�ס����ࡢ��������ҩ�������й㷺Ӧ�ã�Ҳ���������ࡢ�����ʳƷ��Ⱦɫ�ͷ������������ж���������ʳƷ��ҵ�������ϸ����ơ�������ͼ��ʾ�������г�װ����ʡ�ԣ���ҩƷ��̽���������������ᷴӦ���������ɷ֡�
��֪����NO+NO2+2OH��==2NO2��+H2O?������Һ�����¶ȣ�NO2��21�棬NO��-152��

��1��Ϊ�˼���װ��A�����ɵ�����������������˳����������ӣ���A��C��?��?��?��
��2����ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪�����ų�װ���еĿ�����Ŀ����?��
��3���ڹرյ��ɼУ���Һ©������������70%�����A�в�������ɫ���塣
��ȷ��A�в��������庬��NO�����ݵ�������?��
��װ��E��������?��
��4�������D��ͨ�����O2����װ��B�з�����Ӧ�Ļ�ѧ����ʽΪ?�����û��װ��C����ʵ�������ɵ�Ӱ����?��
��5��ͨ������ʵ��̽�����̣��ɵó�װ��A�з�Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���1��E��D��B��2����ֹ�������ɵ�NO��������NO2����ɶ�A�з�Ӧ������������ɸ���
��3����D��ͨ���������ֺ���ɫ����?��������ʹNO2��ȫҺ��
��44NO+O2+4NaOH=2H2O+4NaNO3ˮ�������ڣ�����NO2��Ӧ����NO����ɶ�NO����Դ��ʶ����
��5��2NaNO2+H2SO4 NO��+NO2��+Na2SO4+H2O��
NO��+NO2��+Na2SO4+H2O��
�����������1����Aװ���п��ܷ����ķ�Ӧ�У�2NaNO2+H2SO4(Ũ)  ?Na2SO4+2HNO2��2HNO2
?Na2SO4+2HNO2��2HNO2 NO��+NO2��+H2O����������Һ�����¶ȣ�NO2��21�棬NO��-152�棬����NO2����Һ����Ҫ����E����,Ȼ����Dװ�ø���2NO+O2= 2NO2��ɫ�����Ϊ����ɫ����֤NO�Ĵ��ڡ�NO��NO2���Ǵ�����Ⱦ����Ҫ����β����������Bװ�õ�NaOH��Һ�����ա�Ϊ�˼���װ��A�����ɵ�����������������˳���� A��C��E��D��B����2����ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪�����ų�װ���еĿ�������Ϊ�˷�ֹ�������ɵ�NO��������NO2����ɶ�A�з�Ӧ������������ɸ��š�
NO��+NO2��+H2O����������Һ�����¶ȣ�NO2��21�棬NO��-152�棬����NO2����Һ����Ҫ����E����,Ȼ����Dװ�ø���2NO+O2= 2NO2��ɫ�����Ϊ����ɫ����֤NO�Ĵ��ڡ�NO��NO2���Ǵ�����Ⱦ����Ҫ����β����������Bװ�õ�NaOH��Һ�����ա�Ϊ�˼���װ��A�����ɵ�����������������˳���� A��C��E��D��B����2����ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪�����ų�װ���еĿ�������Ϊ�˷�ֹ�������ɵ�NO��������NO2����ɶ�A�з�Ӧ������������ɸ��š�
��3����D����������ɫ�ģ���ͨ���������ֺ���ɫ���塣��װ��E��������������ʹNO2��ȫҺ��
��4�������D��ͨ�����O2����װ��B�з�����Ӧ�Ļ�ѧ����ʽΪ4NO+O2+4NaOH=2H2O+4NaNO3���û��װ��C�������������к��е�ˮ�������ͻ���NO2������Ӧ��3NO2+H2O=2HNO3+NO��������NO����ɶ�NO����Դ��ʶ���塣Ӱ���жϽ������ȷ�ԡ���5��ͨ������ʵ��̽�����̣��ɵó�װ��A�з�Ӧ�Ļ�ѧ����ʽ��2NaNO2+H2SO4(Ũ)  ?Na2SO4+2HNO2��2HNO2
?Na2SO4+2HNO2��2HNO2 NO��+ NO2�� +H2O�����ӵõ��ܷ���ʽΪ��2NaNO2+H2SO4
NO��+ NO2�� +H2O�����ӵõ��ܷ���ʽΪ��2NaNO2+H2SO4 NO��+NO2+Na2SO4+H2O
NO��+NO2+Na2SO4+H2O
�����Ѷȣ�����
3��ʵ���� ij�о���ѧϰС���������²�����̽��NH3�Ļ�ԭ�ԣ�����ʵ��װ������ͼ��
����1��NH3��ǿ��ԭ�����ܽ�ijЩ���������ﻹԭΪ�������ʻ�ͼ�̬��������磺
2NH3 + 3CuO 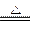 3Cu + N2 +3H2O
3Cu + N2 +3H2O
����2��Cu+��������Һ�в��ȶ����ɷ�������������ԭ��Ӧ����Cu2O����ɫ��������Cu2+��Cu��
Cu2O + 2H+ ="=" Cu2+ + Cu +H2O
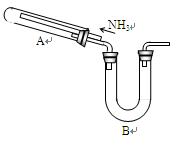
��ش��������⣺
(1)Ϊ֤��NH3��ԭCuO�ķ�Ӧ����ˮ���ɣ�B��Ӧ������Լ���?��
(2)���۲쵽?��������������A�еķ�Ӧ�Ѿ���ɣ�
(3)��С�����������Ϊ1�U4��ϡ�������Լ������鷴Ӧ�Ƿ���Cu2O�������ɡ�����98%��Ũ��������1�U4��ϡ���ᣬ����IJ����������˽�ͷ�ι����?��
(4)��֤����ԭ�����к���Cu2O�IJ�����������?��
(5)��д��A������Cu2O�Ļ�ѧ����ʽ?��
(6)���ö����ķ����ⶨ�÷�Ӧ�Ƿ�����Cu2O��������ȷ�ķ�����?
?��
�ο��𰸣�1����ˮ����ͭ?
��2��A�еĺ�ɫ������ȫ��ɺ�ɫ������2�֣�
��3���ձ�?��Ͳ?������ ��3�֣�?
��4������������Һ����Һ����ɫ?��3�֣�
��5��2NH3+6CuO 3Cu2O?+N2+3H2O��3�֣�
3Cu2O?+N2+3H2O��3�֣�
��6��������Ӧǰ��װ��A�й����������2�֣�
�����������
�����Ѷȣ���
4��ѡ���� ����˵������ȷ����?��?��
A��������ϡ���ᷴӦ���Ʊ�����
B��SO2��ʹʪ�����ɫʯ����ֽ�ȱ�����ɫ
C��NO2 ����ˮ������������ԭ��Ӧ�����������������ǻ�ԭ��
D������������ȼ�շ����⣬���ɰ�ɫ����������
�ο��𰸣�C
������������������������ᣬ�������Ӧ��������������A����ȷ��SO2��Ư��ijЩ��ɫ���ʣ�������Ư�����ָʾ�������SO2��ʹʪ�����ɫʯ���Ա�죬��������ɫ��B����ȷ��NO2����ˮ�ķ���ʽΪ3NO2��H2O=2HNO3��NO���ڷ�Ӧ��3mol NO2����2mol����ԭ������NԪ�صĻ��ϼ��ɣ�4�����ߵ���5�ۣ�����1mol������������NԪ�صĻ��ϼ��ɣ�4�۽��͵���2�ۣ����NO2�������������ǻ�ԭ����C��ȷ������������ȼ�շ�����ɫ���棬���ɵ���ɫ����������ƣ�D����ȷ��
�����Ѷȣ���
5��ѡ���� �����й�������������������ˮ�У����ܷ������ֽⷴӦ�����ܷ���������ԭ��Ӧ���ǣ�������?
A��NaNO3��NaHSO4��CH3COONa?
B��MgSO4��AlCl3��NaAlO2?
C��Ba(NO3)2��FeSO4��NH4HSO4?
D��Na2SO3��Na2SO4��BaCl2
�ο��𰸣�C?
���������
���ܷ������ֽⷴӦ�����ܷ���������ԭ��Ӧ��?
Ba2++SO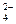
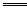 BaSO4����3Fe2++4H++NO
BaSO4����3Fe2++4H++NO
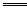 3Fe3++2H2O+NO
3Fe3++2H2O+NO
�����Ѷȣ���