微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是
A.偏二甲肼的摩尔质量为60g
B.1?mol?偏二甲肼的质量为60?g/mol
C.1mol偏二甲肼的质量为60?g
D.6?g偏二甲肼(C2H8N2)含有NA个分子
参考答案:C
本题解析:分析:A.摩尔质量的单位为g/mol;
B.质量的单位为g;
C.1mol物质的质量再数值上等于摩尔质量;
D.利用n=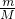 ,N=n×NA来计算分子数.
,N=n×NA来计算分子数.
解答:A.偏二甲肼(C2H8N2)的摩尔质量为(12×2+1×8+14×2)g/mol=60g/mol,故A错误;
B.1?mol?偏二甲肼的质量为60?g,故B错误;
C.1mol偏二甲肼的质量为60?g,故C正确;
D.偏二甲肼的物质的量为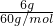 =0.1mol,含有的分子数为0.1×NA,故D错误.
=0.1mol,含有的分子数为0.1×NA,故D错误.
故选C.
点评:本题考查摩尔质量、质量、和分子数,题目难度不大,明确n=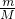 ,N=n×NA等计算公式是解答本题的关键.
,N=n×NA等计算公式是解答本题的关键.
本题难度:简单
2、选择题 用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比是
A.5:4
B.4:5
C.1:8
D.8:1
参考答案:C
本题解析:分析:用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得产物有Na2CO3和NaHCO3,根据Na元素和C元素守恒列式计算.
解答:用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得产物有Na2CO3和NaHCO3,
设生成xmolNa2CO3,ymolNaHCO3,
则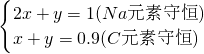
解之得:
所得溶液中的CO32-和HCO3-的物质的量浓度之比等于物质的量之比,为0.1:08=1:8,
故选C.
点评:本题考查物质的量浓度的计算,题目难度不大,注意从质量守恒的角度分析.
本题难度:简单
3、选择题 用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
C.在常温常压下,11.2LCl2含有的分子数为0.5NA
D.在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4NA
参考答案:BD
本题解析:分析:A、氦气为单原子分子.根据n=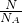 计算氦气物质的量,在根据V=nVm计算体积;
计算氦气物质的量,在根据V=nVm计算体积;
B、根据n= 计算二氧化硫的物质的量,结合二氧化硫的化学式,利用N=nNA计算原子数目;
计算二氧化硫的物质的量,结合二氧化硫的化学式,利用N=nNA计算原子数目;
C、标准状况下气体摩尔体积为22.4L/mol;
D、硝酸镁是强电解质,在溶液中完全电离,由硝酸镁的化学式计算硝酸根离子的浓度,根据n=cV计算硝酸根离子物质的量,利用N=nNA计算硝酸根离子数目.
解答:A、氦气为单原子分子,含有NA个氦原子的氦气的物质的量为1mol,在标准状况下的体积约为22.4L,故A错误;
B、64gSO2中含有的原子数为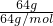 ×3×NAmol-1=3NA,故B正确;
×3×NAmol-1=3NA,故B正确;
C、不是标准状况,气体摩尔体积不一定为22.4L/mol,故C错误;
D、2mol/L的硝酸镁溶液中硝酸根离子浓度为4mol/L,所以1L溶液含有的硝酸根离子数为1L×4mol/L×NAmol-1=4NA,故D正确.
故选BD.
点评:本题考查常用化学计量数的有关计算,难度不大,注意稀有气体为单原子分子,气体摩尔体积使用条件范围,电解质溶液中离子的浓度、数目计算.
本题难度:简单
4、选择题 将1L0.2mol/L?NaCl溶液和1L0.2mL/L?Na2SO4溶液混合,若溶液的体积为二者体积之和,则混合溶液中钠离子浓度为
A.0.2mol/L
B.0.3mol/L
C.0.6mol/L
D.0.8mol/L
参考答案:B
本题解析:分析:0.2mol/L?NaCl溶液中钠离子浓度为0.2mol/L,0.2mL/L?Na2SO4溶液中钠离子浓度为0.4mol/L,根据n=cV计算钠离子的物质的量,混合后溶液中的钠离子的物质的量等于氯化钠溶液与硫酸钠溶液含有的钠离子之和,再根据c=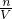 计算.
计算.
解答:解0.2mol/L?NaCl溶液中钠离子浓度为0.2mol/L,1L氯化钠溶液中钠离子的物质的量为1L×0.2mol/L=0.2mol,
0.2mL/L?Na2SO4溶液中钠离子浓度为0.4mol/L,1L硫酸钠溶液中钠离子的物质的量为1L×0.4mol/L=0.4mol,
混合后溶液中的钠离子物质的量为0.2mol+0.4mol=0.6mol,
故混合溶液中钠离子浓度为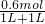 =0.3mol/L
=0.3mol/L
故选B.
点评:本题考查物质的量浓度的有关计算,比较基础,注意公式的理解与灵活运用.
本题难度:简单
5、选择题 下列物质中,前者属于氧化物、后者属于电解质的是
A.Al2O3、CaCO3
B.HClO、Cu
C.C2H6O、CH4
D.NO2、NH3
参考答案:A
本题解析:分析:氧化物由负价氧和另外一种元素组成的二元化合物,属于纯净物;水溶液中或熔融状态下能够导电的化合物称为电解质;在上述两种情况下都不能导电的化合物称为非电解质.注意电解质与非电解质都属于化合物,电解质自身可以离解成自由移动的离子,酸、碱、盐都是电解质;非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子.
解答:A.Al2O3由Al、O两种元素组成,且氧元素为负价,属于氧化物;碳酸钙属于盐,属于电解质,故A正确;
B.HClO由三种元素组成,不属于氧化物;Cu属于单质,即不是电解质,也不是非电解质,故B错误;
C.C2H6O由三种元素组成,不属于氧化物;CH4属于共价化合物,不溶于水,液态不导电,属于非电解质,故C错误;
D.NO2由N、O两种元素组成,且氧元素为负价,属于氧化物;NH3属于共价化合物,液态不导电,溶于水导电,是由于与水反应生成一水合氨,一水合氨电离出铵根离子与氢氧根离子,NH3属于非电解质,故D错误;
故选A.
点评:本题考查氧化物、电解质的基本概念,比较基础,注意抓住概念中的关键词理解概念.
本题难度:困难