��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� A��B��C��D��E��F����Ԫ��ΪԪ�����ڱ��е�ǰ20��Ԫ�أ�0.5molA��Ԫ�ص����ӵõ�NA�����Ӻ�ԭΪ����ԭ�ӣ�0.4gA��������ǡ����100mL0.2mol/L��������ȫ��Ӧ��AԪ��ԭ�Ӻ�������������������ȡ�BԪ��ԭ�Ӻ����������AԪ��ԭ�Ӻ����������1��C�����Ӻ�����Ӳ�����AԪ�ص����Ӻ�����Ӳ�����1��DԪ��ԭ�������������Ǵ�����������2����E���Ȼ���ECl2?1.11g�����Һ������1mol/L����������Һ20mL���ܰ���������ȫ������������E�ĺ���������Ϊ20��F������������Ӧ��ˮ������������⻯�����Ӧ�����Ρ�����д���пո�
(1)�ƶ�A��B��C��D��E��F����Ԫ�صķ���A_________��B_________��C________��D________�� E_________��F_________
(2)C��һ�������ӵĽṹʾ��ͼ__________________��
(3)DԪ�ص����������Ľṹʽ��_______________��
(4)C��D��Ԫ���γɵĻ��������ʽ______________�������ں���_______��(��Ի�Ǽ���)��
(5)55.5g?ECl2���������ӵ����ʵ���Ϊ__________mol��
�ο��𰸣���13�֣�(1)(ÿ��1��)Mg��Al��Cl��C��Ca��N��(2) (ÿ��1��)Cl-?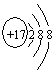 ��(3)O=C=O(1��)��
��(3)O=C=O(1��)��
(4)(ÿ��2��)  �����ԣ���5��(1��)27
�����ԣ���5��(1��)27
���������0.5molA��Ԫ�ص����ӵõ�NA�����Ӻ�ԭΪ����ԭ�ӣ���A�ǵڢ�A��Ԫ�ء�0.4gA��������ǡ����100mL0.2mol/L��������ȫ��Ӧ������0.4gA������������ʵ�����0.01mol�����Ը����������Է���������40����A�����ԭ��������24������ΪAԪ��ԭ�Ӻ�������������������ȣ�����A����������12����A��Mg��BԪ��ԭ�Ӻ����������AԪ��ԭ�Ӻ����������1����B��Al��C�����Ӻ�����Ӳ�����AԪ�ص����Ӻ�����Ӳ�����1�����C����Ԫ�ء�DԪ��ԭ�������������Ǵ�����������2������D��̼Ԫ�ء�E���Ȼ���ECl21.11g�����Һ������1mol/L����������Һ20mL���ܰ���������ȫ���������������������ӵ����ʵ�����0.02mol�����Ը��Ȼ�������ʵ�����0.01mol������Ȼ������Է���������111����E�����ԭ��������111��71��40.����ΪE�ĺ���������Ϊ20��������������20����E��CaԪ�ء�F������������Ӧ��ˮ������������⻯�����Ӧ�����Σ����F�ǵ�Ԫ�ء�
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���ض�ѧ������֪ʶ�Ĺ�����ѵ��������������ѧ����������������������Ҫ��Ԫ�ء�λ�������ԡ����߹�ϵ���ۺϿ��飬�Ƚ�ȫ�濼��ѧ���й�Ԫ���ƶ�֪ʶ���������֪ʶ�������������ԡ����ڱ���Ԫ�ص��ƶϡ�Ϊ���壬����ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�
�����Ѷȣ�һ��
2������� ��10�֣��±�ΪԪ�����ڱ��е�һ���֣��û�ѧʽ��Ԫ�ط��Żش��������⣺
?
| IA
| ��A
| ��A
| ��A
| VA
| ��A
| ��A
| 0
|
2
| ?
| ?
| ?
| ��
| ?
| ��
| ?
| ?
|
3
| ��
| ��
| ��
| ?
| ?
| ?
| ��
| ��
|
4
| ��
| ��
| ?
| ?
| ?
| ?
| ��
| ?
|
��1��10��Ԫ���У���ѧ��������õ���__________����Ԫ�����ƣ���
��2���ڢ٢ڢݵ�����������ˮ�����У�������ǿ����__________���ѧʽ����
��3��Ԫ�آߵij������⻯��Ļ�ѧʽΪ__?__�����⻯�ﳣ���º�Ԫ�آڵĵ��ʷ�Ӧ�����ӷ���ʽ�ǣ�_______________________�����⻯����Ԫ�آ�ĵ��ʷ�Ӧ�����ӷ���ʽ��___________________________��
��4���ٺ͢������������Ӧ��ˮ���ﻯѧʽ�ֱ�Ϊ___________��_______��
��5���ٺ͢�����������Ӧ��ˮ�������Ӧ�Ļ�ѧ����ʽΪ__________________
��6�������ֱ���H2�γɵ��⻯����ȶ��ԣ�__________�����û�ѧʽ��ʾ������������Ӧ��ˮ��Һ�����ԣ�_______________�����û�ѧʽ��
�ο��𰸣���1��벣�2��KOH��3��H2O��2K+2H2O==2K��+2OH�D+H2����Cl2+H2O H��+Cl�D+HClO
H��+Cl�D+HClO
NaOH��HBrO4?��5��NaOH+Al��OH��3==NaAlO2+2H2O
��6�� HCl>HBr��HClO4>HBrO4
�����������1������Ԫ�������ﵽ���ȶ��ṹ����ѧ�����ȶ�����2��ͬ��������������Ӧˮ�����������ǿ��ͬ��������������Ӧˮ���������������KOH>NaOH>Al(OH)3����3��Ԫ�آ�ΪO�����⻯��ΪH2O���غ�ˮ��Ӧ�����������غ�������Ԫ�آ�Ϊ�ȣ�������ˮ��Ӧ��������ʹ����ᣬ�����������ᣬ����д��������ʽ����4����Ϊ�ƣ��Ƶ�����������Ӧ��ˮ����ΪNaOH����Ϊ�壬�������������Ӧˮ����Ϊ�����ᣬ��HBrO4����5���������ƺ�����������Ӧ�ķ���ʽ����6��ͬ������̬�⻯����ȶ�����������HCl>HBr������������Ӧˮ�����������������HClO4>HBrO4
�����Ѷȣ�һ��
3������� ��11�֣� A��B��C��D��E��F����Ԫ�أ����ǵĺ˵������С��18����ԭ��������������֪��A��C��F����ԭ�ӵ�����㹲��11�����ӣ���������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ���������κ�ˮ��11.5g A����ǡ����100mL 5mol/L��������ȫ��Ӧ����Ӧ����Һ�����ԡ�DԪ��ԭ�ӵ������������ȴ�����������4����EԪ��ԭ�ӵĴ�����������������������3������ش��������⣺
��1��D��Ԫ�ط���?��E������������ˮ����ķ���ʽ?��
��2������BԪ�ص�ԭ�ӽṹʾ��ͼ?��
��3��������FԪ�ص�һ��ԭ�ӵ�������Ϊ35��д����ԭ�ӷ���?����ԭ�Ӻ��ڵ���������?��
��4��A��F��C��F��A��CԪ������������ˮ���ﷴӦ�����ӷ���ʽ����
��?��?��?��
�ο��𰸣���11�֣���1��Si? H3PO4?��2��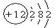
��3�� ? 18
? 18
��4��H++OH- = H2O? Al(OH)3+3H+=Al3++3H2O? Al(OH)3+OH- = AlO2-+2H2O
�������������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ���������κ�ˮ��˵��һ��������Ԫ�ء�����ԭ��������С˳���֪��C������A�ǵ�IAԪ�أ�����F����Ԫ�ء�11.5g A����ǡ����100mL 5mol/L��������ȫ��Ӧ����Ӧ����Һ�����ԣ����A�����ԭ��������11.5��0.5��23������A����Ԫ�أ���B��Mg��DԪ��ԭ�ӵ������������ȴ�����������4������D�ǹ衣EԪ��ԭ�ӵĴ�����������������������3������E��P��
�����Ѷȣ�һ��
4��ѡ���� A��B��C��D��EΪ������Ԫ����ɵ���ѧ�������ʣ�����ת����ϵ��ͼ��ʾ�����ֲ��������ȥ����
����˵����ȷ���ǣ�?��
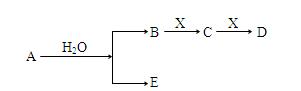
A����CΪ������̼����E������ǿ��Ҳ������ǿ��
B����DΪ��ɫ��״���������AĦ��������ȣ���EΪһ�������嵥��
C����EΪ��������Aһ��Ϊ����������
D����AΪ�������ʣ���Xһ��Ϊ������̼
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
5��ѡ���� ���и��������У�ȫ�����Ӿ�����ԭ�ӵ��Ӳ�ṹ��ͬ����
A��Na+��Mg2+��Al3+��O2-��F-��
B��Li+��Na+��F-��O2-��Cl-
C��Na+��Mg2+��Al3+��K+��Ca2+����
D��S2-��Cl-��K+��Ca2+��Na+
�ο��𰸣�A
�����������ԭ�Ӻ���Ϊ10����������Li+��S2-��Cl-��K+��Ca2+������������
�����Ѷȣ�һ��