��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ʪ�����ɫʯ����ֽ����ʢ�������ļ���ƿ�У��۲쵽��ֽ��ɫ������Ϊ��������
A�����
B�����
C���ȱ�����ɫ
D������ɫ
�ο��𰸣���������ˮ��Ӧ��������ʹ����ᣬ����ʹ����ᶼ�������ԣ�ʹʪ�����ɫʯ����ֽ��죬���������ǿ�����ԣ���ɫ����Ϊ��ɫ���ʣ���������Ϊ���ȱ����ף���ѡ��C��
���������
�����Ѷȣ���
2������� ��ͼ��ijѧϰС����������װ��̽����������֮��ķ�Ӧ������A��F�ֱ�Ϊ�����Ͱ����ķ���װ�ã�DΪ�����������Ͱ����ķ�Ӧװ�ã�
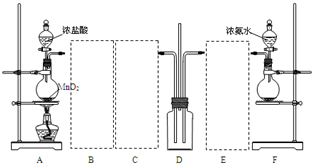
��ش��������⣺
��1��װ��F����ƿ�ڵĹ����ѡ��______
A���Ȼ���?B����ʯ��?C������������?D���ռ�
��2��ʵ�������õ�Ũ�������������Ϊ36.5%�����ܶ�Ϊ1.19?g/cm3���������ʵ���Ũ��Ϊ______��������λС�������ڱ������______L��������λС�����Ȼ�������1Lˮ�вſɵô�Ũ�ȵ����ᣮ
��3�����߿���Ӧ���ӱ�Ҫ�ij���װ�ã��뽫����װ������Ӧ���Լ������������пո��У�B______��C______��E______��
��4��װ��D�ڳ��ְ��̲��������ڱ����ᣬ�����ù������Ȼ������Ҫ���Լ��У�______��
��5����ͬѧ��ΪD�г������Ȼ�������⣬��Ӧ�������������ɣ�����Ϊ����������______�����D������δ���ֺ���ɫ��Ҳû�а��̲�������D�з�����Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣���1��A��C���ܹ��Ͱ�ˮ��Ӧ������ȡ������B��D������ʹŨ��ˮѸ�ٲ����������ʴ𰸵ģ�BD��
��2��1L��Һ������Ϊ��1.19��1000��1=1190��g����c��HCl��=1190��36.5%36.5��1=11.9��mol/L����1L��Һ�У�n��HCl��=11.9mol������£�V��HCl��=22.4��11.9=266.56��L�����ʴ��ǣ�11.9mol/L��266.56��
?��3�������ڱ���ʳ��ˮ���ܽ�Ƚ�С�����ñ���ʳ��ˮ��ȥ�����л��е��Ȼ��⣬����BΪ����ʳ��ˮ��Ũ�����������Ӧ������Ч���ã�����ȡ��������Ũ���������������CΪŨ���E�Ǹ��ﰱ�����Լ���ͨ��ʹ�ü�ʯ�ң���EΪ��ʯ�ң�
�ʴ�Ϊ������ʳ��ˮ��Ũ�����ʯ�ң�
��4�������ù������Ȼ�泥���Ҫ�ֱ��������Ӻ������ӣ�����Ӽ��鷽���ǣ��ȼ�����Һ������ʹ��ɫʯ����ֽ���������壬֤������Ӵ��ڣ������Ӽ��鷽���ǣ��ȵμ���������Һ�������������ټ���ϡ���ᣬ�������ܽ⣬֤�������Ӵ��ڣ��ʴ��ǣ�NaOH��Һ��ʪ��ĺ�ɫʯ����ֽ����������Һ��ϡ���
��5�������Ȼ�����ɣ����ݵ����غ㣬�����е���Ԫ�صõ����ӣ����ϼ۽��ͣ�һ������ʧȥ���ӣ����ϼ����ߵ�Ԫ�أ�����D������δ���ֺ���ɫ��Ҳû�а��̲��������Զ϶������еĵ�Ԫ��Ӧ�������˵����������ķ�ӦΪ2NH3+3Cl2�TN2+6HCl��
�ʴ�Ϊ�����ϼ����ֻ�����Ȼ�泥����ϼ�ֻ�н���û������������������ԭ��Ӧ��ʧ������ȵĹ��ɣ�2NH3+3Cl2�TN2+6HCl��
���������
�����Ѷȣ�һ��
3������� �������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
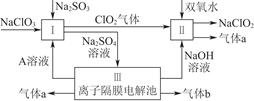
��1��˫��ˮ�ĽṹʽΪ____________�����з�����Ӧ�Ļ�ԭ����__________���ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ��_____________________________________________________________________________________________________________________________________��
��3��A�Ļ�ѧʽ��________��װ�â���A��________����������
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���
��д���÷�Ӧ�Ļ�ѧ����ʽ��________________________________________________________________________________________________________________________________________________��
���о�����������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��________________________________________________________________________
________________________________________________________________________��
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ������NaClO2������һ�ݸ����ʵ�����ʹ֮���ʣ���һ���ϸ棬�������Һ�����ֱ�������FeSO4��Һ��Ӧʱ������Fe2�������ʵ���________�����ͬ��������ͬ�������жϡ�����
�ο��𰸣���1��H��O��O��H��Na2SO3
��2��2ClO2 ��H2O2��2OH��=2ClO2-��O2����2H2O
��3��H2SO4����
��4��5NaClO2��4HCl=5NaCl��4ClO2����2H2O? ClO2-��3Cl����4H��=2Cl2����2H2O
��5����ͬ
�����������1��NaClO3��Clԭ�ӻ��ϼ�Ϊ��5�ۣ����к�ǿ�������ԣ���SO32-�����������¾��н�ǿ�Ļ�ԭ�ԣ��ʢ��з�����Ӧ����������NaClO3����ԭ����Na2SO3����2�����Na2SO4��Һ�൱�ڵ��ˮ��������a��b��Na2SO4��Һ�ĵ������֪ΪH2��O2��������aΪ��Ӧ��IJ���֮һ��֪��ΪO2��ΪH2O2��ClO2�����õ��IJ���ʷ�Ӧ��ķ�Ӧ��ΪClO2��H2O2��NaOH����������NaClO2��O2�����ݵ����غ��ԭ���غ���ƽ���ɣ���3�����Na2SO4��ҺʱOH�����������ɣ���Na��ͨ�����Ӹ�Ĥ�������ƶ��õ�����NaOH��Һ������������H����SO42-�������ƶ��õ�����A����H2SO4��Һ������4�����������֪��Ӧ��ΪNaClO2��HCl������NaClO2��ClԪ�صĻ��ϼ�Ϊ��3�ۣ��ȿ�����Ҳ�ɽ��ͣ��ʷ�ӦΪNaClO2������������ԭ��Ӧ�����ݵ����غ��֪��������ClO2�ͻ�ԭ����Cl�������ʵ���֮��Ϊ4��1������ԭ���غ㽫����ʽ��ƽ���ɣ���������ΪCl2��ClO2-��HCl�����˹��з�Ӧ�����ݵ����غ��֪��Ӧ��ClO2-��HCl�����ʵ���֮��Ϊ3��1������ԭ���غ㽫����ʽ��ƽ���ɣ���5�����ʹ���ΪNaClO2������������ԭ��Ӧ�����۱��������Fe2����Ӧʱ��Ԫ�����ն�ת��ΪCl������ת�Ƶ�������ȡ�
�����Ѷȣ�����
4��ѡ���� ��֪����ĸ�Ļ�ѧʽΪK2H4Al6Si6O24���������������ʽ�ɱ�ʾΪ______________��
�ο��𰸣�K2O��3Al2O3��6SiO2��2H2O
��������������λ�ѧʽ��������������ʽ����ʾ��һ�㷽���ǣ��ٰ�˳��д��������ý��������ﲻ���ý��������� �ǽ���������
�ǽ��������� SiO2
SiO2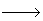 H2O������������Ŀ�ð�������������ǰ���ʾ��
H2O������������Ŀ�ð�������������ǰ���ʾ��
�����Ѷȣ�һ��
5������� ��һ�ֺ����������Ԫ�صĻ�����ɳ�Ϊ����⣬���иû������еĵ�Ԫ�س������ֲ�ͬ��̬+3�ۺ�+5�ۣ�����������л�ѧ֪ʶˮƽ���ۺ�������������û�����Ļ�ѧʽ______________________��
�ο��𰸣�I4O9
�����������������������+3��+5�ۣ��ֳ�Ϊ����⣬�����ΪIO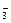 ��IΪ+5�ۣ�����+3��ӦΪI3+�����Ե����ΪI��IO3��3������ʽΪ��I4O9��
��IΪ+5�ۣ�����+3��ӦΪI3+�����Ե����ΪI��IO3��3������ʽΪ��I4O9��
�����Ѷȣ�һ��