��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��ȷ���� ��?��
A���������еμӰ�ˮ��H+ + OH- = H2O
B��Fe(OH)3��������Fe(OH)3 + 3H+ = Fe3+ + 3H2O
C��ͭ����ϡ���3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ��+ 4H2O
D����Na2S2O3��Һ��ͨ������������S2O32����2Cl2��3H2O��2SO32����4Cl����6H+
�ο��𰸣�C
���������A������ˮΪ������ܲ��������ʽ��B�������ɵ������Ӿ���ǿ�����������������ӣ�C��ȷ��D���������ߵ�ǿ����������������������ӣ�
�����Ѷȣ�һ��
2��ʵ���� ��15�֣��������д�������Ⱦ��SO2��NO����ҵ�ϱ䡰�ϡ�Ϊ�������չ�ҵβ��SO2��NO���ɻ��Na2S2O3��NH4NO3��Ʒ������ͼ����(CeΪ��Ԫ��)��
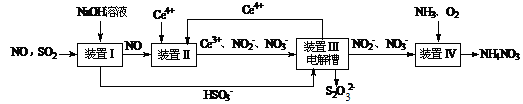
��װ�â��е���Ҫ���ӷ���ʽΪ?��3
�ƺ������(H2SO3��HSO3����SO32��)������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������X(i)����ҺpH �Ĺ�ϵ��ͼ��ʾ��
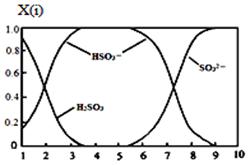
������0.1molNaOH��Ӧ�����Һ�������Һ��pH=8ʱ����Һ�и������ɴ�С��˳����?��
����pH=5��NaHSO3��Һ�еμ�һ��Ũ�ȵ�CaCl2��Һ����Һ�г��ֻ��ǣ�pH��Ϊ2���û�ѧƽ���ƶ�ԭ��������ҺpH���͵�ԭ��?��
��д��װ�â��У����������µ����ӷ���ʽ?��
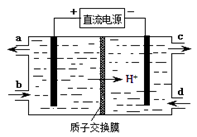
��װ�â���ʹCe4+��������ԭ������ͼ��ʾ��
������Ce4+�ӵ��۵�?(����ĸ���)����������д���������ķ�Ӧʽ?��
����֪����װ�â�����Һ�У�NO2����Ũ��Ϊa g��L-1��Ҫʹ1 m3����Һ�е�NO2����ȫת��ΪNH4NO3����������װ�â���ͨ���״���µ�O2?L��(�ú�a����ʽ��ʾ�� ��������������)
�ο��𰸣���1�� SO2+OH-=HSO3-��
��2�� ��c(Na+)��c(SO32-)��c(HSO3-)��c(OH-)��c(H+) ?���� HSO3-����Һ�д��ڵ���ƽ�⣺HSO3- SO32-+ H+����CaCl2��Һ��Ca2++SO32-=CaSO3��ʹ����ƽ�����ƣ�c(H+)����?
SO32-+ H+����CaCl2��Һ��Ca2++SO32-=CaSO3��ʹ����ƽ�����ƣ�c(H+)����?
��3�� NO+2H2O+3Ce4+=3Ce3++NO3-+4H+��NO+H2O+Ce4+=Ce3++NO2-+2H+
��4��?��a ��?��2HSO3-+4H++4e-=S2O32-+3H2O
��5��243a (242a��244a��5600a/23������)
��������������â���SO2��NaOH��Һ������Ӧ�����ӷ���ʽ��SO2+OH-=HSO3-����2������Һ��pH=8ʱ����Һ�к��е�������Na2SO3��NaHSO3.���������غ�ɵ�c(Na+)=(SO32-)+(HSO3-)+(H2O3)������c(Na+)���֪c(SO32-)��c(HSO3-)������Һ�Լ��ԣ�����c(OH-)��c(H+)����Ϊ����ǿ����ʣ���ˮ��ij̶������ģ�����c(HSO3-)��c(OH-)������Һ�е�����Ũ�ȹ�ϵΪ��c(Na+)��c(SO32-)��c(HSO3-)��c(OH-)��c(H+)����NaHSO3��Һ��pH=5��˵������Һ��NaHSO3�ĵ������ô���ˮ�����ã��������м���CaCl2��Һʱ���ᷢ����Ӧ��Ca2++SO32-=CaSO3�����������ƻ�����Һ��HSO3-����Һ�д��ڵ���ƽ�⣺HSO3- SO32-+ H+��ʹƽ�������ƶ������е������������H+��c(H+)���������Һ��pH��С��pH��Ϊ2������װ�â��У������������¸�������ʾ��ͼ�ɵ÷�Ӧ�����ӷ���ʽ��NO+2H2O+3Ce4+=3Ce3++NO3-+4H+��NO+H2O+ Ce4+=Ce3++NO2-+2H+������װ�â���ʹCe4+������������Ce3+��Ce4+,���ϼ����ߣ�ʧȥ���ӣ���������Ce4+�ӵ��۵�����a�������������������ĵ缫�ķ�Ӧʽ��2HSO3-+4H++4e-=S2O32-+3H2O��������NO2����Ũ��Ϊa g��L-1������1 m3����Һ�е�NO2������Ϊa g��L-1��1000L=1000ag.���ʵ���Ϊ1000ag��46g/mol��ÿ1mol��NO2����ȫת��ΪNH4NO3��ʧȥ����2mol.����ת�Ƶ��ӵ����ʵ���Ϊ1000ag��46g/mol��2=(1000a��23)mol,ÿһmol��������Ӧת�Ƶ���4mol�������������������ʵ���Ϊ(1000a��23)mol��4=(250a��23)mol,��������װ�â���ͨ���״���µ�O2�������(250a��23)mol��22.4L/mol=5600a/23L="243." 5aL��
SO32-+ H+��ʹƽ�������ƶ������е������������H+��c(H+)���������Һ��pH��С��pH��Ϊ2������װ�â��У������������¸�������ʾ��ͼ�ɵ÷�Ӧ�����ӷ���ʽ��NO+2H2O+3Ce4+=3Ce3++NO3-+4H+��NO+H2O+ Ce4+=Ce3++NO2-+2H+������װ�â���ʹCe4+������������Ce3+��Ce4+,���ϼ����ߣ�ʧȥ���ӣ���������Ce4+�ӵ��۵�����a�������������������ĵ缫�ķ�Ӧʽ��2HSO3-+4H++4e-=S2O32-+3H2O��������NO2����Ũ��Ϊa g��L-1������1 m3����Һ�е�NO2������Ϊa g��L-1��1000L=1000ag.���ʵ���Ϊ1000ag��46g/mol��ÿ1mol��NO2����ȫת��ΪNH4NO3��ʧȥ����2mol.����ת�Ƶ��ӵ����ʵ���Ϊ1000ag��46g/mol��2=(1000a��23)mol,ÿһmol��������Ӧת�Ƶ���4mol�������������������ʵ���Ϊ(1000a��23)mol��4=(250a��23)mol,��������װ�â���ͨ���״���µ�O2�������(250a��23)mol��22.4L/mol=5600a/23L="243." 5aL��
���飺���ӷ���ʽ����д������Ũ�ȵıȽϡ����ԭ����Ӧ�á�������ԭ��Ӧ���йؼ����֪ʶ��
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ������ǣ�������
A������ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2��
B������ͭ��NaOH��Һ��Ӧ��Cu2++OH-=Cu��OH��2��
C�����������������Һ��Ӧ��CH3COOH+OH-=CH3COO-+H2O
D��̼��þ�����ᷴӦ��MgCO3+2H+=Mg2++H2O+CO2��
�ο��𰸣�A�����������Ӧ���ɵ��Ƕ��۵�������ȷ�����ӷ���ʽΪ��Fe+2H+=Fe2++H2������A����
B����ɲ��غ㣬��ȷ�����ӷ���ʽΪ��Cu2++2OH-=Cu��OH��2������B����
C�����������ᣬ�÷���ʽ����ȷ�����ӷ���ʽΪ��CH3COOH+OH-=CH3COO-+H2O����C��ȷ��
D��̼��þ���������Σ��÷���ʽ����ȷ�����ӷ���ʽΪ��MgCO3+2H+=Mg2++H2O+CO2������D��ȷ��
��ѡAB��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ����ȷ����
[? ]
A��Fe(OH)3��������Fe(OH)3+3H+=Fe3++3H2O
B����NaHSO4��Һ����ε���Ba(OH)2��Һ��������ȫ��2H++2SO42-+Ba2++2OH-=BaSO4��+2H2O
C����6.72?L��״���µ�CO2����ͨ��2L?0.2?mol/L��NaOH��Һ�У�3CO2+4OH-=
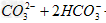 +H2O
+H2O
D��NH4HCO3���ڹ�����NaOH��Һ�У�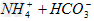 +2OH-=NH3��H2O+
+2OH-=NH3��H2O+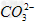 +H2O
+H2O
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��ȷ����
[? ]
A��������̼��Ʒ�Ӧ��CaCO3+ 2H+ ��Ca2++H2O+CO2��
B����������Һ������ȩ�е�ȩ����CH3CHO +2Ag(NH3)2++2OH-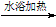 CH3COO-+ NH4++3NH3+
CH3COO-+ NH4++3NH3+
2Ag��+ H2O
C�����������ȵ��������ƵĴ���Һ��У�C2H5Br + OH-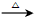 C2H5OH + Br-
C2H5OH + Br-
D����������Һ��ͨ������CO2��CO2+ H2O + 2C6H5O-��2C6H5OH +CO32-
�ο��𰸣�B
���������
�����Ѷȣ�һ��