微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各项与反应热的大小无关的是
[? ]
A.反应物和生成物的状态
B.反应物量的多少
C.反应物的性质
D.反应的快慢
参考答案:D
本题解析:
本题难度:简单
2、选择题 在相同的温度和压强下,将32 g硫分别于纯氧中和空气中完全燃烧,令前者放出的热量为Q1,后者放出的热量为Q2,则关于Q1和Q2相对大小,正确的判断是
[? ]
A.Q1= Q2
B.Q1>Q2
C.Q1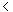 Q2
Q2
D.无法判断
参考答案:C
本题解析:
本题难度:简单
3、选择题 关于下列图示的说法中,正确的是
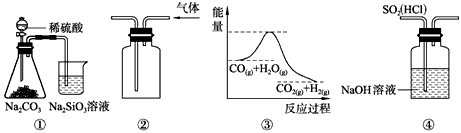
[? ]
A.图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B.用图②所示实验装置排空气法收集CO2气体
C.图③表示可逆反应CO(g)+H2O(g)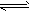 CO2(g)+H2(g)的ΔH大于0
CO2(g)+H2(g)的ΔH大于0
D.图④装置可以用来除去SO2中的HCl
参考答案:A
本题解析:
本题难度:一般
4、填空题 (6分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)在不同温度下,反应N2(g)+O2(g) 2NO(g) DH=a kJ・mol-1的平衡常数K如下表:
2NO(g) DH=a kJ・mol-1的平衡常数K如下表:
温度/℃
| 1538
| 1760
| 2404
|
平衡常数K
| 0.86×10-4
| 2.6×10-4
| 64×10-4
|
?该反应的△H?0(填“>”、“=”或“<”)。
(2)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应:
N2(g)+O2(g) 2NO(g)达到平衡时N2的浓度为?。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为?。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
(3)科学家一直致力于研究常温常压下“人工固氮”的新方法。曾有实验报道:在常温、常压光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方程式如下:
2N2(g)+6H2O(1)=4NH3 (g)+3O2(g)?DH=+1530kJ・mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热DH=?。?(用含a的代数式表示)
参考答案:(1)>? (2)2.5mol/L?(3)(2a-1530)kJ・mol-
本题解析:(1)根据表中数据可知,升高温度,平衡常数增大,所以反应是吸热反应,即△H>0.
(2)? N2(g)+O2(g) 2NO(g)
2NO(g)
起始量(mol)? 2.6? 2.6? 0
转化量(mol)? x? x? 2x
平衡量(mol)? 2.6-x? 2.6-x? 2x
根据该温度下的平衡常数可知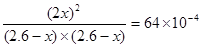
解得x=0.1mol,所以平衡时氮气的浓度为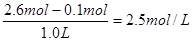
(3)考查盖斯定律的应用。将反应①N2(g)+O2(g) 2NO(g) DH=a kJ・mol-1和反应②2N2(g)+6H2O(1)=4NH3 (g)+3O2(g)?DH=+1530kJ・mol-1叠加,即①×2-②得到4NH3(g)+5O2(g)=4NO(g)+6H2O(1),所以其反应热是(2a-1530)kJ・mol-。
2NO(g) DH=a kJ・mol-1和反应②2N2(g)+6H2O(1)=4NH3 (g)+3O2(g)?DH=+1530kJ・mol-1叠加,即①×2-②得到4NH3(g)+5O2(g)=4NO(g)+6H2O(1),所以其反应热是(2a-1530)kJ・mol-。
本题难度:一般
5、选择题 下列各项与反应热的大小无关的是( )
A.反应物和生成物的状态
B.反应物量的多少
C.反应物的性质
D.反应的快慢
参考答案:A、反应物和生成物的状态,例如同一个化学反应,生成液态水或水蒸气,反应热肯定不一样,故A错误
B、反应物量的多少,例如氢气与氧气反应生成水的化学反应中,氢气和氧气反应的量不同,反应放热不同,故B错误;
C、反应物性质,例如锌和浓硫酸,锌和稀硫酸反应的反应热肯定不一样,反应热和物质的聚集状态有关,和物质的性质有关,故C错误;
D、反应的快慢和反应物以及生成物间没有联系,这不会影响反应热大小,故D正确.
故选D
本题解析:
本题难度:简单