��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ?��֪��������������ȶ�����������������ڸ������H2S��HCl�ױ���������HCl ��H2S�������ɵ��ʺϳɣ�����������Ա�H2S������ǿ��������ʵ�ܹ�˵����ķǽ����Ա���������
A���٢ڢ�
B���ۢܢ�
C���ڢۢ�
D���٢ۢ�
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ѡ���� �� NA��ʾ�����ӵ�����������˵������ȷ����
A�����³�ѹ�£�11.2 L����������ԭ����ΪNA
B��1.8 g ��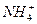 �к��еĵ�����ΪNA
�к��еĵ�����ΪNA
C�����³�ѹ�£�48 g O3���е���ԭ����Ϊ3NA
D��2��4 g����þ��Ϊþ����ʱʧȥ�ĵ�����Ϊ0.1NA
�ο��𰸣�BC
������������³�ѹ�£�11.2 L����(O2)�����ʵ���С��0.5 mol����������ԭ����С��NA��1.8 g��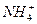 �����ʵ���Ϊ0.1 mol������������Ϊ0.1 mol��10��NA���� NA���� 48 g O3������ԭ�ӵ����ʵ���Ϊ
�����ʵ���Ϊ0.1 mol������������Ϊ0.1 mol��10��NA���� NA���� 48 g O3������ԭ�ӵ����ʵ���Ϊ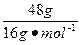 ="3" mol�����Ժ��е���ԭ�ӵ���ĿΪ3NA��2��4 g����þʧȥ���ӵ���ĿΪ0.1 mol��2��NA mol-1=0.2NA��
="3" mol�����Ժ��е���ԭ�ӵ���ĿΪ3NA��2��4 g����þʧȥ���ӵ���ĿΪ0.1 mol��2��NA mol-1=0.2NA��
�����Ѷȣ���
3��ѡ���� ��84������Һ���ճ�������ʹ�ù㷺��������Һ��ɫ����Ư�����ã�������Ч�ɷ����������ʵ�һ�֣�����������
A��NaOH
B��NaClO
C��KMnO4
D��Na2O2
�ο��𰸣�B
�������������Ŀ������Ϣ��������Һ��ɫ����Ư�����á���ѡ�������ʵ������������⡣
A��NaOH��Һ��Ư�����ã���B����
B��NaClO��ˮ��ҺΪ��ɫҺ�壬����ǿ�����ԣ�������ɱ������������Ư���ԣ���Ư��dzɫ�·�����A��ȷ��
C��KMnO4��ˮ��Һ���Ϻ�ɫ����������ɫ��������C����
D��Na2O2����Һ�в����ܴ��ڣ���D����
��ѡB��
������������һ�����ʶ�����⣬ּ�ڿ�����ȡ��Ϣ�������ͶԻ���֪ʶ�����ա����û�ѧ֪ʶ���ʵ��������������ѶȽ�С�����ֻ�ѧ����������������ϵ��
�����Ѷȣ���
4������� A��J����ѧ��ѧ�г����ļ������ʣ�����֮���ת����ϵ��ͼ��ʾ����֪������AΪ���嵥�ʣ�BΪ����ɫ��ĩ��C��F��IΪ��̬���ʣ�E�ڳ�����ΪҺ�壬��E����C��F�ϳɣ�J������ɱ����������
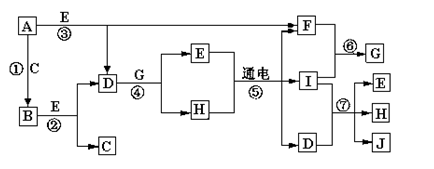
�ش��������⣺
(1)B�Ļ�ѧʽ��?��E�ĵ���ʽ_________��
��2��д����Ӧ�ߵ����ӷ���ʽ? __________________________��
��3����AlCl3��Һ�м�����������B��д����Ӧ�Ļ�ѧ����ʽ_____________________��
��4����PtΪ�缫���μ���������̪��H������Һ������_____________���������������������Һ����ɫ��Ϊ��ɫ����ԭ����_________________ ��
�ο��𰸣���1��Na2O2��2�֣�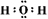
��2��Cl2+2OH��=Cl��+ClO��+H2O
��3��4AlCl3+6Na2O2+6H2O=4Al(OH)3��+12NaCl+3O2��
(4)������1�֣�������������H+�õ����Ӳ���H2���ƻ���ˮ�ĵ���ƽ�⣬�ٽ�ˮ�������룬������Һ��c(OH��)>c(H+)����Һ�ʼ��ԣ���������������Һ��Ϊ��ɫ ��1�֣�
���������
������AΪ���嵥�ʣ�BΪ����ɫ��ĩ����AΪNa��BΪNa2O2����ôCΪO2��E�ڳ�����ΪҺ�壬ӦΪH2O����FΪH2�� DΪNaOH��H��ˮ��Һ��ͨ�������·�Ӧ����H2��I��NaOH��ӦΪ��ⱥ��ʳ��ˮ�ķ�Ӧ����IΪCl2����֪GΪHCl�� HΪNaCl��Cl2��NaOH��Ӧ����NaCl��H2O��NaClO����JΪNaClO����
(1)B�Ļ�ѧʽ��Na2O2��E�ĵ���ʽ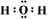
��2��Cl2+2OH��=Cl��+ClO��+H2O
��3��4AlCl3+6Na2O2+6H2O=4Al(OH)3��+12NaCl+3O2��
(4) 2Cl�D��2H2O 2OH�D��H2����Cl2��OH�D����������ⱥ��ʳ��ˮ��������ӦΪ��2Cl��-2e��=Cl2��������ӦΪ2H��+2e��=H2������������H���õ����Ӳ���H2���ƻ���ˮ�ĵ���ƽ�⣬�ٽ�ˮ�������룬������Һ��c��OH������c��H��������Һ�ʼ��ԣ���������������Һ��Ϊ��ɫ
2OH�D��H2����Cl2��OH�D����������ⱥ��ʳ��ˮ��������ӦΪ��2Cl��-2e��=Cl2��������ӦΪ2H��+2e��=H2������������H���õ����Ӳ���H2���ƻ���ˮ�ĵ���ƽ�⣬�ٽ�ˮ�������룬������Һ��c��OH������c��H��������Һ�ʼ��ԣ���������������Һ��Ϊ��ɫ
��Ϊ������������H+�õ����Ӳ���H2���ƻ���ˮ�ĵ���ƽ�⣬�ٽ�ˮ�������룬������Һ��c(OH��)>c(H+)����Һ�ʼ��ԣ���������������Һ��Ϊ��ɫ��
�����Ѷȣ�һ��
5������� Ư������������ҵ��������;�㷺��Ư�۳��˾���Ư�������⣬����ɱ��������
(1)2011��3��11��13ʱ46�֣��ձ�����9.0�����𣬸�������������������˾�������ͲƲ���ʧ�����ֹ�������ˮ������ɱ����Ϊ���ƴ��ģ��Ⱦ�Լ�����������Ч����֮һ��Ư���dz��õ���������
�ٹ�ҵ�Ͻ�����ͨ��ʯ����[Ca(OH)2]����ȡƯ�ۣ���ѧ����ʽΪ_________________��Ư�۵���Ч�ɷ���__________��
��Ư��Ӧ�ܷⲢ�������������棬���û�ѧ����ʽ˵�����е�ԭ��_____________��_____________
(2)��֪Ũ����ʹ�������ܷ������·�Ӧ��Ca(ClO)2+4HCl(Ũ)=CaCl2+2Cl2��+2H2O��������ܾõ�Ư����Ũ�����Ƶõ������У����ܺ��е�����������_________��
��CO2 ��HCl ��H2O ��O2
A���٢ڢ� B���ڢۢ� C���ڢ� D���٢�
�ο��𰸣�(1)��2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O��Ca(ClO)2����Ca(ClO)2+CO2+H2O=CaCO3��+2HClO��
2HClO 2HCl+O2��
2HCl+O2��
(2)A
���������
�����Ѷȣ�һ��