| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《化学平衡》试题强化练习(2017年最新版)(八)
参考答案:D 本题解析:化学平衡的本质是正逆反应速率相等,所以答案选D。 本题难度:一般 2、选择题 恒温恒容条件下,能使 参考答案:D 本题解析: 本题难度:一般 3、填空题 (10分)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。 |
参考答案:(1)向左 不改变 (2)-77.6 (3)c(N2O4)/c2(NO2) 减小 BC
(4)中 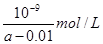
本题解析:(1)在恒压条件下加入氩气,则容积增大,导致原平衡中各物质的浓度同等比例减小,所以平衡向气体体积增大的方向即向左移动;催化剂仅是改变化学反应速率,不会影响焓变。
(2)根据盖斯定律,将化学方程式①+②-③叠加即得到O2(g)+PtF6(g) = O2+PtF6-(s)。
(3)平衡常数是指在一定条件下的可逆反应中,当反应达到平衡时生成物浓度的幂之积和反应物浓度的幂之积的比值。因为反应是放热反应,所以升高温度,平衡向逆反应方向移动,平衡常数减小。减小反应物浓度平衡向逆反应方向移动,转化率降低。温度降低平衡向正反应方向移动,转化率增大,升高温度正好相反。因为反应物和生成物都只有一种,所以增加NO2的物质的量,相当于增大压强,平衡向正反应方向移动,转化率增大。
(4)由溶液的电荷守恒可得: c(H*)+c(NH4*)=c(Cl-)+c(OH-),已知c(NH4*)=c(Cl-),则有c(H*)=c(OH-),溶液显中性;电离常数只与温度有关,则此时NH3・H2O的电离常数
Kb=[c(NH4*)・c(OH-)]/c(NH3・H2O)=(0.01mol・L-1・10-7mol・L-1)/(amol・L-1-0.01mol・L-1)
= 10-9/( (a-0.01)mol・L-1。
本题难度:一般
4、选择题 一定温度下,向一个一定容积的密闭容器中放入2molX和3molY,发生反应:X(气)+Y(气)?mZ(气)+nR(气),达平衡时,Z的体积分数为φ1,维持温度不变,若把3molX和2molY放入另一体积相同的密闭容器,达平衡时,Z的体积分数为φ2,则φ1与φ?2的关系为( )
A.φ1>φ2
B.φ1<φ2
C.φ1=φ2
D.无法判断
参考答案:密闭容器中放入2molX和3molY,发生反应:X(气)+Y(气)?mZ(气)+nR(气),达平衡时,Z的体积分数为φ1;维持温度不变,若把3molX和2molY放入另一体积相同的密闭容器,达平衡时,Z的体积分数为φ2,x和y这两种气体的反应比为1:1,达到平衡时参与反应的量取决于最小者,即2molx和2moly反应生成z,生成的Z的量是相同的,容器体积不变,Z的条件分数相同;
故选C.
本题解析:
本题难度:一般
5、选择题 在恒压条件下化学反应:2SO2(g)+O2(g)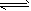 2SO3(g);△H= -QkJ/mol,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
2SO3(g);△H= -QkJ/mol,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是 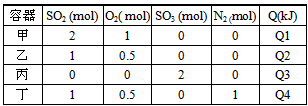
[? ]
A.平衡时,向甲容器中再加1mol O2,一段时间后达到平衡时O2的体积分数减小
B.平衡时,升高丙容器温度,正反应速率增大,逆反应速率减小,平衡逆向移动
C.各容器中反应放出热量的关系为:Q1=2Q2>2Q4
D.丁容器中反应达到平衡时,其化学平衡常数小于乙容器中反应的平衡常数
参考答案:C
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《溶液的酸碱.. | |