微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (2014届河北省冀州中学高三3月摸底考试理综化学试卷)
氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如下图所示:
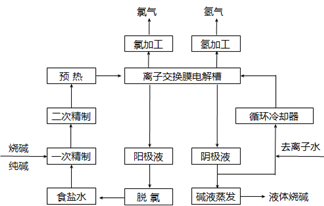
(1)该流程中可以循环的物质是?。
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式?,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果?。
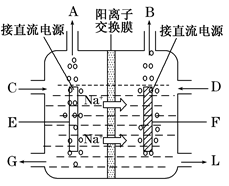
(3)右图是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成)。则B处产生的气体是?,E电极的名称是?。电解总反应的离子方程式为?。
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为?。
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3,电解槽的电流强度1.45 ×104A,该电解槽的电解效率为?。
参考答案:(1)氯化钠?氢氧化钠
(2)Ca2++ CO32- = CaCO3↓? Mg2+ + 2OH- = Mg(OH)2↓?用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜。
(3)H2 阳极 ?2Cl-+2H2O Cl2↑+H2↑+2 OH-
Cl2↑+H2↑+2 OH-
(4)Na2SO3 + Cl2 + H2O = Na2SO4 + 2HCl
(5)93.46%
本题解析:
氯碱工业的电解原理是2Cl-+2H2O Cl2↑+H2↑+2OH-。(1)从图上看未电解的NaCl和产物NaOH可以循环使用。(2)粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,一次精制时加入纯碱和烧碱,其中CO32-使Ca2+沉淀,OH-使Mg2+沉淀;用试剂处理后的盐水中还含有少量Mg2+、Ca2+,若食盐水不经过二次精制就直接进入离子膜电解槽,碱性条件下会生成沉淀,损害离子交换膜。
Cl2↑+H2↑+2OH-。(1)从图上看未电解的NaCl和产物NaOH可以循环使用。(2)粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,一次精制时加入纯碱和烧碱,其中CO32-使Ca2+沉淀,OH-使Mg2+沉淀;用试剂处理后的盐水中还含有少量Mg2+、Ca2+,若食盐水不经过二次精制就直接进入离子膜电解槽,碱性条件下会生成沉淀,损害离子交换膜。
(3)图中Na+由左侧通过离子交换膜进入右侧,说明F电极为H+放电,是阴极,B处产生的气体是H2;
E电极是阳极。电解总反应的离子方程式即电解原理。
(4)溶解氯与亚硫酸钠溶液反应,Cl2变成Cl-,亚硫酸钠变成硫酸钠,注意水参与了反应。
(5)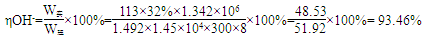
本题难度:一般
2、选择题 糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
B.脱氧过程中铁作原电池正极,电极反应为:Fe-2e