微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越 来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:xMg+Mo3S4 MgxMo3S4;在镁原电池放电时,下列说法错误的是
MgxMo3S4;在镁原电池放电时,下列说法错误的是
[? ]
A.Mg2+向正极迁移
B.正极反应为:Mo3S4+2xe-= Mo3S42x-
C.Mo3S4发生氧化反应
D.负极反应为:xMg-2xe-= xMg2+
参考答案:C
本题解析:
本题难度:一般
2、填空题 (7分)用导线将锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,此电池的负极是 ,正极的电极反应式是 ,负极的电极反应式是 ,总电极反应式是 。
参考答案:(共7分) Zn 1分,2H++2e-==H2 2分 Zn-2e-==Zn2+2分, Zn+2H+= Zn2+ + H2 2分
本题解析:略
本题难度:简单
3、填空题 (14分)碳和氮的许多化合物在工农业生产和生活中有重要的作用。
(1)用CO2 和H2 合成CH3OH具有重要意义,既可以解决环境问题,还可解决能源危机。已知: +
+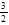
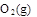 =
= 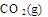 ?+ 2
?+ 2 △H = -725.5 kJ・mol-1
△H = -725.5 kJ・mol-1
2H2 (g)+O2(g) = 2H2O(l)?△H = -565.6 kJ・mol-1,
请写出工业上用CO2 和H2 合成CH3OH(l)的热化学方程式:?;
(2)一种新型燃料电池,一极通入空气,一极通入CH3OH(g),电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。则在该熔融电解质中,O2-向?(填“正”或“负”)极移动,电池负极电极反应为:? ?;
(3)如图是一个电化学装置示意图。用CH3OH-空气燃料电池做此装置的电源。如果A是铂电极,B是石墨电极,C是CuSO4溶液,通电一段时间后,向所得溶液中加入8 g CuO固体后恰好可使溶液恢复到电解前的浓度和pH.则电解过程中收集到标准状况下的气体体积为?;
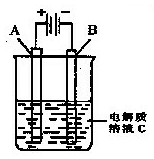
(4)常温下0.01 mol・L-1的氨水中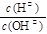 = 1×10- 6 ,则该溶液的pH为____,溶液中的溶质电离出的阳离子浓度约为?;将 pH = 4的盐酸溶液V1 L与 0.01 mol・L-1氨水V2 L混合,若混合溶液pH = 7,则V1和V2的关系为:V1??V2(填“>”、“<”或“=”)。
= 1×10- 6 ,则该溶液的pH为____,溶液中的溶质电离出的阳离子浓度约为?;将 pH = 4的盐酸溶液V1 L与 0.01 mol・L-1氨水V2 L混合,若混合溶液pH = 7,则V1和V2的关系为:V1??V2(填“>”、“<”或“=”)。
参考答案:(1)CO2(g) + 3H2(g)=CH3OH(l) + H2O(l)?△H=-122.9 kJ・mol-1(2分)
(2)负(2分),CH3OH-6e-+3O2-=CO2 + 2H2O(2分)
(3)1.12 L(2分)
(4)10,10-4 mol・L-1 ; >?(每空2分)
本题解析:(1)写出反应方程式:CO2(g)+3H2(g)=CH3OH(l)+H2O(l),再根据盖斯定律有目标方程式等于②×-①,故ΔH=×(-565.5)-(725.5)=-122.75 KJ/mol;(2)在原电池中阳离子向正极移动,阴离子向负极移动,燃料做负极,故负极反应为:CH3OH-6e-+3O2-=CO2 + 2H2O;(3)电解后加入CuO能恢复到原来状态,说明生成物为Cu和O2,8gCuO为0.1mol,故生成0.05mol氧气,标况下体积为1.12L;(4)===10-6,故c(H+)=10-10mol/L,pH=10,c(HCl)<c(NH3・H2O),现要呈中性,故有V1>V2。
本题难度:一般
4、选择题 在用锌片、铜片和稀硫酸组成的原电池装置中,经过一段时间后,下列说法正确的是(?)
A.铜片上有气泡产生,发生还原反应
B.锌是负极,发生还原反应
C.电流方向是从锌片沿导线流向铜片
D.铜片逐渐溶解,被氧化
参考答案:A
本题解析:考查原电池的判断和应用。原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极方向移动,正极得到电子,发生还原反应。锌比铜活泼,锌是负极,铜是正极,氢离子在正极得到电子生成氢气。所以答案选A。
本题难度:一般
5、选择题 镍氢电池比碳锌或碱性电池有更大的输出电流,更适合用于高耗电产品。镍氢电池的总反应式是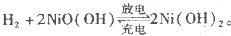 。下列叙述错误的是
。下列叙述错误的是

A.电池充电时,氢元素被还原
B.电池放电时,镍元素被氧化
C.电池放电时,氢气在负极反应
D.电池放电时,电池负极周围溶液的碱性减弱
参考答案:B
本题解析:A、电池充电时,H元素的化合价降低发生还原反应,正确;B、电池放电时,Ni元素的化合价降低,发生还原反应,错误;C、电池放电时,氢气发生氧化反应,所以在电池的负极被氧化,正确;D、结合C选项,氢气发生氧化反应生成氢离子,与电解质溶液中的氢氧根离子结合生成水,所以电池负极周围溶液的碱性减弱,正确,答案选B。
本题难度:一般