��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ͼ������������̽�����������ʡ�ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ���˷��ɿ����Ʊ�����������������һ������������档�±��ж�ʵ�����������Ľ�����ȷ����

ѡ��
| ʵ������
| ����
|
A
| Ũ���ḽ����������
| NH3��Ũ���ᷴӦ������NH4Cl����
|
B
| Ũ���ḽ������������
| NH3��Ũ���������Ӧ
|
C
| �Ȼ�����Һ�����
| ����Һһ����AlCl3��Һ
|
D
| �����ʯ����ֽ����ɫ��ʪ���ɫʯ����ֽ����
| NH3��һ�ֿ����Լ�
2��ѡ���� ��֪������ʵ������������Ա�����ǿ����������ǿ�����ԣ������ǿ�����ԣ��۵���������ֱ�ӻ��ϣ����������ֱ�ӻ��ϣ��ܰ��������ȶ���������˵����Ԫ�صķǽ����Ա���Ԫ��ǿ���ǣ�?��
A���٢ڢ�
B���٢ڢ�
C���٢ۢ�
D���ڢۢ�
3��ѡ���� ��ʢ�е����Ͷ���������������N2O4�����������Թܵ�����ˮ�У������㹻��ʱ����Թ�������������СΪԭ����һ�룬��ԭ��������е��������������������ǣ�?��
A��1��1
B��1��2
C��1��3
D��3��1
4������� ��8�֣����ᡢ�������������ѧ�γ���������ǿ�ᡣ������������ͭ�ķ�Ӧ������ش��������⣺
��1������100mL 1 8 mol��L-1��Ũ�����м��������ͭƬ������ʹ֮��ַ�Ӧ�������������ڱ�״���µ����������?
A��40��32L
B��30.24L
C��20��16L
D��6��72L
|
����ͬѧ�������ʹ������Ӧ����ʣ���ͭƬ�����ܽ⣬�������м��������ƣ����жϸ÷����Ƿ����?�� �����У���˵��ԭ�������У���д����Ӧ�����ӷ���ʽ��?��
�����У���˵��ԭ�������У���д����Ӧ�����ӷ���ʽ��?��
��2������6��4gͭ����һ����Ũ���ᷴӦ����ͭ����ȫ�ܽ�ʱ���������壨NO��NO2����2.24L����״��������Ӧ�������ĵ���������ʵ���Ϊ?��
��3��ijͬѧ�����ͭƬ��ϡ�����м���H2O2��ͭƬ�ܽ⣬���Ҹ÷�Ӧ�IJ���ֻ���Ȼ�ͭ��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��??��
5��ʵ���� Ϊ��̽��AgNO3�������Ժ����ȶ��ԣ�ij��ѧ��ȤС�����������ʵ�顣
��.AgNO3��������
����������˿����AgNO3��Һ�У�һ��ʱ�����˿ȡ����Ϊ������Һ��Fe�������������Һ�е�Ag����������������ʵ�顣��ѡ�õ��Լ���KSCN��Һ����ˮ��
��1��������±���
����
| ����
| ����
|
ȡ��������Ag�������Һ���Թ��У�����KSCN��Һ����
| ____
| ����Fe3��
|
?
��.AgNO3�����ȶ���
����ͼ��ʾ��ʵ��װ��A����AgNO3���壬��������ɫ���壬��װ��D���ռ�����ɫ���塣����Ӧ�����Ժ��Թ��в�������Ϊ��ɫ��
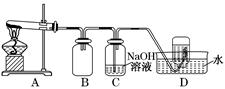
��2��װ��B��������____________________________________________________��
��3����С�����۲���֤����ɫ����ΪO2������֤������__________________________________________________________��
��4�����������ϡ�Ag2O�ͷ�ĩ״��Ag��Ϊ��ɫ��Ag2O�����ڰ�ˮ��
��������롿�Թ��в����ĺ�ɫ��������ǣ���Ag����.Ag2O����.Ag��Ag2O��
��ʵ����֤����С��Ϊ��֤�������룬�ֱ�ȡ������ɫ��������Թ��У�����������ʵ�顣
ʵ����
| ����
| ����
|
a
| ����������ˮ����
| ��ɫ���岻�ܽ�
|
b
| ��������ϡ���ᣬ��
| ��ɫ�����ܽ⣬�����������
|
?
��ʵ�����ۡ���������ʵ�飬����ȷ���������ɷֵ�ʵ����__��__(��ʵ����)��
��ʵ����ۡ���������ʵ��������С��ó�AgNO3�����ȷֽ�IJ�����__��__��