微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
【方案一】
将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.实验中发生反应的化学方程式是______.
(1)称取5.4g铝镁合金粉末样品,溶于V?mL?2.0mol/L?NaOH溶液中.为使其反应完全,则NaOH溶液的体积V≥______.
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将______(填“偏高”、“偏低”或“无影响”).
【方案二】
将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01×105Pa)的体积.
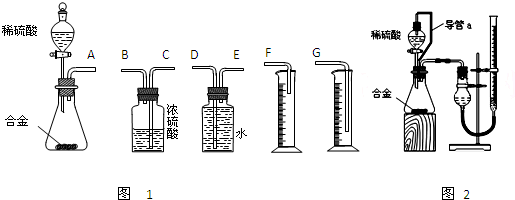
(1)同学们拟选用下列实验装置完成实验如图1:
①你认为最简易的装置其连接顺序是:A接______接______接______(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因______.
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是______.
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸?滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了图2所示的实验装置.
①装置中导管a的作用是______.
②实验前后碱式滴定管中液面读数分别为V1?mL、V2?mL.则产生氢气的体积为______mL.
参考答案:方案一:铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(1)含镁为3%时,金属铝的含量最高,5.4g合金中铝的质量为,5.4g×(1-3%)=5.4×97%g,则:
? 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
? 54g?2mol?
5.4g×97%g? ?V×10-3L×2.0mol/L
所以54g:(5.4g×97%g)=2mol:(V×10-3L×2.0mol/L),解得:V=97,故V(NaOH溶液)≥97mL;
故答案为:97mL;
(2)镁上会附着偏铝酸钠等物质,未洗涤导致测定的镁的质量偏大,镁的质量分数偏高;
故答案为:偏高;
方案二:(1)①装置的组装顺序:合金与水反应,用排水量气法测定氢气的体积,其中盛水的试剂瓶导管一定要短进长出,利用增大压强原理将水排出,量筒中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部,故连接顺序为:(A)接(E)(D)接(G);
故答案为:E、D、G;
②镁、铝与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大,导致硫酸不能顺利滴入锥形瓶;
故答案为:镁、铝与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大;
③反应放热导致氢气的温度偏高,故应冷却后再进行读取氢气的体积,读取实验中生成氢气的体积时上下移动量筒,使其中液面与广口瓶中液面相平,视线与凹液面的最低点水平读取氢气的体积;
故选ACD;
(2)①装置中导管a的作用是:保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差;
故答案为:保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差;
②滴定管的数值零刻度在上方,两次的体积之差为测定的氢气的体积,收集氢气后滴定管内液面读数减小,故测定氢气的体积为V1-V2;
故答案为:V1-V2.
本题解析:
本题难度:一般
2、选择题 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生 气体的体积(V)与时间(t)关系如图。反应中镁和铝的
气体的体积(V)与时间(t)关系如图。反应中镁和铝的
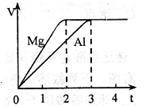

A.物质的量之比为3:2
B.质量之比为3:2

C.摩尔质量之比为2:3
D.反应速率之比为2:3
参考答案:A
本题解析:略
本题难度:一般
3、填空题 (10分) 某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500 mL 0.5 mol・L-1的硫酸溶液中,右图为反应产生氢气速率与反应时间的关系图。
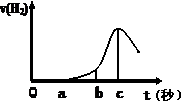
(1)关于图像的描述不正确的是?(填序号,下同);
① o→a段不产生产生H2是室温过低,反应难以发生。
② b → c段产生H2较快可能是反应放热,温度升高,加快了反应
③ c以后,产生H2速率逐渐下降原因可能是铝片趋于消耗完全
(2)在b到c这段时间内,收集到氢气VL(标准状况),则这段时间内用硫酸表示的平均速率为??mol/(L・s)(假设反应前后溶液体积不变)。
(3)其他条件不变,现换用500 mL 1 mol・L-1盐酸,产生氢气速率普遍较使用500 mL 0.5 mol・L-1硫酸的快,可能的原因是________;
(4)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,合理的有 ?
①加入2 mol・L-1硝酸②加入少量CuSO4溶液 ③将铝片换成铝粉 ④增加硫酸的浓度至18 mol/L ⑤加CH3COONa固体; ⑥加入少量Na2SO4溶液
(5)催化剂会影响反应速率,请根据①反应写出FeCl3催化H2O2分解的另一反应原理(用离子方程式)①2Fe3++ H2O2= 2Fe2++ 2H+ +O2↑;②?;
参考答案:(1)①③;(2)V/11.2(c―b)?mol/(L・s);(3)氯离子由催化作用或硫酸根由阻化作用;(4)②③;(5)②2Fe2+ + H2O2 + 2H+====2Fe3+ + 2H2O。
本题解析:(1)① o→a段不产生产生H2是由于金属铝表面有一层氧化膜,氧化铝与稀硫酸反应生成硫酸铝和水,错误;② b → c段产生H2较快可能是反应放热,温度升高,加快了反应,正确;③ 根据题给数据知,铝过量,c以后,产生H2速率逐渐下降原因可能是稀硫酸趋于消耗完全,错误,选①③;(2)在b到c这段时间内,收集到氢气VL(标准状况),物质的量为V/22.4mol,时间为(c―b)s,硫酸的物质的量变化为V/22.4mol,则这段时间内用硫酸表示的平均速率为V/11.2(c―b)?mol/(L・s);(3)其他条件不变,现换用500 mL 1 mol・L-1盐酸,产生氢气速率普遍较使用500 mL 0.5 mol・L-1硫酸的快,可能的原因是氯离子由催化作用或硫酸根由阻化作用;(4)①加入2 mol・L-1硝酸,硝酸具有强氧化性,与铝反应不放氢气,错误;②加入少量CuSO4溶液,铝置换出铜,形成原电池,反应速率加快,正确; ③将铝片换成铝粉 ,增大反应物的接触面积,反应速率加快,正确;④增加硫酸的浓度至18 mol/L ,铝遇浓硫酸钝化,阻止反应进行,错误;⑤加CH3COONa固体,硫酸与醋酸钠反应生成醋酸,氢离子浓度较小,反应速率减慢,错误; ⑥加入少量Na2SO4溶液,将硫酸稀释,反应速率减慢,错误,选②③;(5)催化剂会影响反应速率,请根据①反应写出FeCl3催化H2O2分解的另一反应原理(用离子方程式)①2Fe3++ H2O2= 2Fe2++ 2H+ +O2↑;②2Fe2+ + H2O2 + 2H+====2Fe3+ + 2H2O。
本题难度:一般
4、填空题 (12分)
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
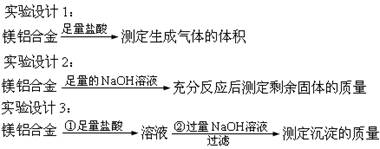
回答下列问题:
(1)上述方案中,能测出Mg的质量分数的方案是?(填写代号,下同)
A.实验设计1? B.实验设计2? C.实验设计3? D.都可以
(2)上述方案中的化学反应体现了Mg、Al的性质是??
A.氧化性? B.还原性? C.酸性? D.碱性
(3)某同学设计了右图装置。该装置适合的实验设计是?
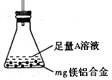

用该装置测定镁铝合金中镁的质量分数,所需的实验操作是
?。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.称量反应前后,装置和药品的总质量
(4)若按实验设计3进行实验。将m g镁铝合金,溶于过量盐酸中,再加入过量的NaOH溶液,可得到白色沉淀,该沉淀物质是?(填化学式);将此沉淀洗净、干燥后,称得质量为w g。求合金中镁的质量分数?;
参考答案:(1)D(2分) (2)B (2分)?(3) B (2分)? B (2分)
(4)Mg(OH)2 (2分)? 12w/29m(2分)
本题解析:(1)设计(1)根据镁铝合金质量及氢气的体积可计算出结果,设计(2)铝能溶于强碱而镁不溶可知剩余的是镁,设计(3)利用Al(OH)3能溶于强碱而Mg(OH)2不溶于强碱可求解;(2)金属和酸反应或和碱反应都表现了还原性;(3)设计1需要气体收集装置,设计3第一步反应完还需要继续加NaOH溶液,所以,此装置只适用于设计2,因镁不溶于NaOH溶液,所以剩余固体即为镁;(4)因Mg(OH)2不溶于NaOH溶液Al (OH)3能溶于NaOH溶液,可知剩余的是Mg(OH)2,根据镁的物质的量等于氢氧化镁的物质的量,质量等于物质的量乘以摩尔质量这一计算式可求出镁的质量,再用镁的质量除以m克乘以100%,即可求出镁的质量分数。
本题难度:简单
5、填空题 材料 近年来,科技人员研究得到一种新型材料--泡沫铝。 它是把发泡剂加到熔融或固体粉末的铝合金中而制成的,其优点是硬度高,密度小(约为0.16克/厘米3~0.5克/厘米3), 比木材还轻,可浮于水面,又有很大的刚性,且隔音、保温,是 一种良好的建筑材料和轻质材料,可大批量投放市场。
(1)铝制成铝箔作食品包装,是利用它的(? ?)。
A.金属光泽
B.延展性
C.导电性
D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物) 而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,且酸、碱均与铝制品发生反应,故不能用铝制品盛放酸性、碱性食品。
①写出铝与盐酸、NaOH溶液反应的化学方程式:____。
②等质量的Al分别加入0.3L 1mol/L的盐酸和NaOH溶液中,生成氢气的体积比为1:2,则加入Al的质量为___。
A.2. 7g
B.5.4g C.
8.1g
D.10g
参考答案:(1) B
(2)①2Al+6HCl=2AlCl3+3H2↑、2Al+ 2NaOH+2H2O=2NaAlO2+3H2↑
②B
本题解析:
本题难度:一般