微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应中,属于氧化还原反应且氧化剂与还原剂是不同物质的是( )
A.2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
B.SO2+Cl2+2H2O═H2SO4+2HCl
C.CaCO3+2HCl═CaCl2+CO2↑+H2O
D.2KClO3=2KCl+3O2↑
参考答案:A、Cl2+H2O=H Cl+HClO中,氯气中氯元素的化合价既升高又降低,则氯气既做氧化剂又做还原剂,故A错误;
B、SO2+Cl2+2H2O═H2SO4+2HCl中氯元素的化合价降低,所以氯气作氧化剂;硫元素的化合价升高,所以二氧化硫作还原剂,该反应属于氧化还原反应且氧化剂与还原剂是不同物质,故B正确;
C、CaCO3+2HCl═CaCl2+CO2↑+H2O中,各元素的化合价都没有发生变化,则不属于氧化还原反应,故C错误;
D、2KClO3=2KCl+3O2↑中,氯元素化合价降低,氧元素化合价升高,所以氯酸钾既作氧化剂又作还原剂,故D错误;
故选B.
本题解析:
本题难度:简单
2、选择题 运用有关概念判断下列叙述正确的是( )
A.1?mol?H2燃烧放出的热量为H2的燃烧热
B.Na2SO3与H2O2的反应为氧化还原反应
C.
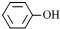
和
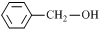
互为同系物
D.BaSO4的水溶液不易导电,故BaSO4是弱电解质
参考答案:A.你mol氢气燃烧生成液态水时放出的热量为氢气的燃烧热,故A错误;
B.亚硝酸钠有还原性,双氧水具有氧化性,二者发生氧化还原反应,故B正确;
C.苯酚和苯甲醇不属于同一类物质,不是同系物,故C错误;
少.硫酸钡属于难溶强电解质,故少错误;
故选A.
本题解析:
本题难度:简单
3、简答题 偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是______.
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)?2NO2(g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为______(填“吸热”或“放热”)反应.
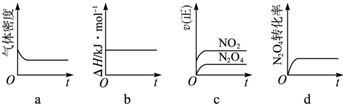
(3)一定温度下,反应(Ⅱ)的焓变为△H.现将1mol?N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是______.若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数______(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=______?mol/(L?s)-1.
(4)NO2可用氨水吸收生成NH4NO3.25℃时,将a?mol?NH4NO3溶于水,溶液显酸性,原因是______(用离子方程式表示).向该溶液滴加b?L?氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将______(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为______mol?L-1.(NH3?H2O的电离平衡常数取Kb=2×10-5?mol?L-1)
参考答案:(1)反应(I)中,N2O4(l)中N元素得电子化合价降低,所以N2O4(l)是氧化剂,故答案为:氧化剂;
(2)升高温度,化学平衡向吸热反应方向移动,当温度升高时,气体颜色变深,平衡向正反应方向移动,所以正反应是吸热反应,故答案为:吸热;
(3)一定温度下,反应(Ⅱ)的焓变为△H.现将1mol N2O4充入一恒压密闭容器中;
a、密度等于质量除以体积,平衡体系质量不变,反应体积增大,密度在反应过程中不变,说明反应达到平衡,故a符合;
b、反应的焓变和反应物与生成物能量总和之差计算,与平衡无关,故b不符合;
c、图象制表示正反应速率变化,不能证明正逆反应速率相同,故c不符合;
d、N2O4(l)转化率不变,证明反应达到平衡,故d符合;
示意图正确且能说明反应达到平衡状态的是ad;K=c2(NO2)c(N2O4),化学平衡常数只与温度有关,与物质的浓度无关,所以平衡常数K不变;v(NO2)=△c△t=0.6mol1L3s=0.2mol/L.s,则v(N2O4)=12v(NO2)=0.1mol/L.s;
故答案为:ad;不变;0.1;
(4)NO2可用氨水吸收生成NH4NO3.25℃时,将a mol NH4NO3溶于水,溶液显酸性,是因为铵根离子水解;反应的离子方程式为:NH4++H2O?NH3?H2O+H+;加入氨水溶液抑制铵根离子水解,平衡逆向进行;将a mol NH4NO3溶于水,向该溶液滴加b L 氨水后溶液呈中性,溶液中氢氧根离子浓度=10-7mol/L;NH3?H2O的电离平衡常数取Kb=2×10-5 mol?L-1,设混合后溶液体积为1L,根据一水合氨电离平衡得到:NH3?H2O?NH4++OH-,平衡常数K=c(NH4+)c(OH-)c(NH3?H2O)=bmol/L×10-7mol/Lb×c(NH3?H2O)mol/L=2×10-5 mol?L-1,计算得到c(NH3?H2O)=a200bmol/L,
故答案为:NH4++H2O?NH3?H2O+H+;逆向;a200b.
本题解析:
本题难度:一般
4、选择题 下列情况下的酸既表现出强氧化性,又表现了酸性的是( )
A.常温下将木炭加入浓硫酸中
B.氧化亚铁(FeO)加入稀硝酸
C.常温下将铜粉加入浓硝酸中
D.氧化铝溶于稀硝酸
参考答案:BC
本题解析:
本题难度:简单
5、填空题 在?K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2+7H2O反应中.
(1)______元素被氧化,______是氧化剂,氧化产物是______;
(2)此反应若转移了12mol的电子,则生成氯气______L(标准状况).
参考答案:(1)氧化还原反应K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2+7H2O反应中,化合价升高的元素Cl元素被氧化,对应产物Cl2是氧化产物,化合价降低元素Cr被还原,所在的反应物K2Cr2O7是氧化剂,发生还原反应,
故答案为:Cl;K2Cr2O7;Cl2;
(2)氧化还原反应K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O中,化合价升高元素Cl失电子,化合价降低元素Cr得电子,得失电子数目相等=反应中转移电子数=6,产生氯气3mol,此反应若转移了12mol的电子,产生氯气6mol,体积为:6mol×22.4L/mol=134.4L,故答案为:134.4L.
本题解析:
本题难度:简单