微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 锌加入很稀的硝酸后生成硝酸锌、硝酸铵和水。在这一氧化还原反应中,用于氧化1?mol?Zn所需的HNO3的物质的量为
A.2.5 mol
B.4 mol
C.0.25 mol
D.0.5 mol
参考答案:A
本题解析:由题意配平方程式为:4Zn+10HNO3====4Zn(NO3)2+NH4NO3+3H2O
本题难度:一般
2、选择题 常温下,下列溶液中各微粒浓度关系不正确的是
A.PH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,C(Na+)大小关系:①>③>②
B.向氨水中滴加稀硫酸至溶液呈中性:C(NH4+)>C(SO42-)>C(OH-)=C(H+)
C.向1L 0.1mol/L的NaOH溶液中通入6.6gCO2:2C(Na+)=3[C(CO32-)+C(HCO3-)+C(H2CO3)]
D.CH3COONa溶液中加入少量KNO3后的碱性溶液一定有:C(Na+)+C(H+)=C(CH3COO-)+C(OH-)
参考答案:C
本题解析:试题分析: A.阴离子水解程度大小关系是CH3COO-<HCO3-<C6H5O-,等pH的这三种盐溶液,盐浓度大小顺序是:①>③>②,所以C(Na+)大小关系:①>③>②,正确;B.溶液呈中性,则C(OH-)=C(H+),溶液中存在电荷守恒C(NH4+)+C(H+)=2C(SO42-)+C(OH-),所以C(NH4+)=2C(SO42-),正确;C.氢氧化钠的物质的量是0.1mol,n(CO2)=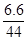 mol=0.15mol,氢氧化钠和二氧化碳的物质的量之比是0.1mol:0.15mol=2:3,所以二氧化碳和氢氧化钠发生的反应为CO2+NaOH=NaHCO3,二氧化碳有剩余,溶液中的溶质是碳酸氢钠,根据物料守恒得C(Na+)=C(CO32-)+C(HCO3-)+C(H2CO3),错误;D.溶液中存在电荷守恒C(Na+)+C(H+)+c(K+)=C(CH3COO-)+C(OH-)+C(NO3-),硝酸钾是强酸强碱盐,则c(K+)=C(NO3-),所以得C(Na+)+C(H+)=C(CH3COO-)+C(OH-),正确.
mol=0.15mol,氢氧化钠和二氧化碳的物质的量之比是0.1mol:0.15mol=2:3,所以二氧化碳和氢氧化钠发生的反应为CO2+NaOH=NaHCO3,二氧化碳有剩余,溶液中的溶质是碳酸氢钠,根据物料守恒得C(Na+)=C(CO32-)+C(HCO3-)+C(H2CO3),错误;D.溶液中存在电荷守恒C(Na+)+C(H+)+c(K+)=C(CH3COO-)+C(OH-)+C(NO3-),硝酸钾是强酸强碱盐,则c(K+)=C(NO3-),所以得C(Na+)+C(H+)=C(CH3COO-)+C(OH-),正确.
考点: 离子浓度大小的比较;盐类水解的应用;酸碱混合时的定性判断及有关PH的计算.
本题难度:一般
3、选择题 镁铝合金m?g和足量盐酸反应后得到的气体在标准状况下的体积为2.24L,m的数值可能是
A.1.8
B.2.0
C.2.2
D.2.4
参考答案:BC
本题解析:极值法,气体在标准状况下的体积为2.24L,也就是1mol,转移2mol电子,假设都是镁,质量为2.4g,假设都是铝,质量为1.8g,所以1.8g<m<2.4g
本题难度:一般
4、选择题 只用一种试剂,一次区别开Na2SO4、AgNO3?和Na2CO3三种溶液,该试剂是
A.BaCl2溶液
B.KOH溶液
C.NaNO3溶液
D.稀盐酸
参考答案:D
本题解析:分析:只用一种试剂,与Na2SO4、AgNO3?和Na2CO3三种溶液反应的现象不同,即可区别;稀盐酸与Na2SO4不反应,稀盐酸与AgNO3反应生成白色沉淀,稀盐酸与Na2CO3反应生成气体,以此来解答.
解答:A.BaCl2溶液与Na2SO4、AgNO3?和Na2CO3三种溶液反应均生成白色沉淀,现象相同,无法区别,故A错误;
B.KOH溶液与Na2SO4、Na2CO3两种溶液均不反应,无法区别,故B错误;
C.NaNO3溶液与Na2SO4、AgNO3?和Na2CO3三种溶液均不反应,无法区分,故C错误;
D.稀盐酸与Na2SO4不反应,稀盐酸与AgNO3反应生成白色沉淀,稀盐酸与Na2CO3反应生成气体,现象不同,能区别,故D正确;
故选D.
点评:本题考查物质的鉴别区分,题目难度不大,注意把握物质的性质,明确反应产生的现象及利用不同现象来区分.
本题难度:困难
5、选择题 氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2+2H2O
参考答案:
本题解析 :
本题难度:一般