微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述:
①我国科学家在世界上第一次人工合成结晶牛胰岛素;
②最早发现电子的是英国科学家道尔顿;
③创造联合制碱法的是我国著名化学家侯德榜;
④首先制得氧气的是法国科学家拉瓦锡;
⑤首先在实验室合成有机化合物尿素的是维勒,其中正确的是
A.只有①
B.①③⑤
C.①②③
D.①②③④
参考答案:B
本题解析:
本题难度:困难
2、填空题 在中学化学中,常用作氧化剂的物质有 、 、 (列举出三种),常用作还原剂的物质有 、 、 (列举出三种)。
参考答案:氧化剂:氧气、氯气、浓硫酸、硝酸、高锰酸钾、氯化铁
还原剂:铝、锌、铁、碳、氢气、一氧化碳
本题解析:略
本题难度:简单
3、填空题 在化学反应中,如果反应前后元素化合价发生变化,就一定量 有转移,这类反应就属于 反应,元素化合价升高,表明该元素的原子 电子,含有该元素的物质发生 反应,这种物质是 剂,元素化合价降低,表明该元素的原子 电子,含有该元素的物质发生 反应,这种物质是 剂。
参考答案:

本题解析:略
本题难度:一般
4、填空题 (12分)填空题
(1)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式_____________________________________。
(2)实验室可用MnO2+4HCl(浓)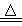 MnCl2+Cl2↑+2H2O制备氯气,请回答以下问题:
MnCl2+Cl2↑+2H2O制备氯气,请回答以下问题:
①该反应的还原剂是 ,氧化剂与还原剂的物质的量比是______________。被氧化的元素是_______________,还原产物是 。
②若反应中转移了NA个电子,则生成的Cl2在标准状况下的体积是 。
③实验室用12.00 mol/L盐酸配制100mL 1 mol/L 盐酸,需要的玻璃仪器除了烧杯、量筒、玻璃棒,还有____________。若定容时俯视刻度线,则配得溶液的浓度___________(填“偏高”,“偏低”,“不变”)。
参考答案:(1)CaH2 + 2H2O = Ca(OH)2 + 2H2↑ (2分)
(2)①HCl 1:2 Cl MnCl2(1×4=4分)
②11.2L (2分)
③100mL容量瓶、胶头滴管(1×2=2分) 偏高(2分)
本题解析:(1)根据现象分析,溶液变红,说明有碱性物质生成,有气泡生成说明有气体生成,氢化钙中的氢元素化合价为-1,和水的氢元素+1发生氧化还原反应生成氢气,所以氢化钙和水反应生成氢氧化钙和氢气,方程式为:CaH2 + 2H2O = Ca(OH)2 + 2H2↑。(2)①反应中盐酸中的氯元素化合价升高,做还原剂,二氧化锰中的锰元素化合价降低,每摩尔二氧化锰得电子需要2摩尔盐酸失去电子,所以氧化剂和还原剂的物质的量比为1:2;盐酸中的氯元素化合价升高被氧化,二氧化锰中锰元素化合价降低,被还原生成氯化锰是还原产物。②每生成1摩尔氯气转移2摩尔电子,所以转移1摩尔电子时生成0.5摩尔氯气,标准状况下体积为11.2L。③配制100毫升溶液必须用100mL容量瓶还用胶头滴管;定容时俯视,溶液的体积偏小,则配制的浓度偏高。
考点:氯气的制取,一定物质的量浓度的溶液的配制。
本题难度:一般
5、选择题 下列实验事实不能证明醋酸是弱酸的是
A.常温下,测得醋酸钠溶液的pH>7
B.常温下,测得0.1 mol・L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和
参考答案:D
本题解析:试题分析:常温下,测得醋酸钠溶液的pH>7,说明醋酸钠水解,因此可以说明醋酸是弱酸,A正确;常温下,测得0.1 mol・L-1醋酸溶液的pH=4,说明溶液中氢离子的浓度小于醋酸的浓度,因此没有完全电离,可以证明,B正确;常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4,说明在稀释过程中,醋酸能继续电离出氢离子,因此存在电离平衡,可以证明,C正确;D只能说明醋酸是一元酸,向酸性,但无法确定是否是弱酸,答案选D。
考点;考查弱电解质的判断
点评:弱电解质的证明,是基于与强电解质对比进行的。弱电解质与强电解质最大的区别就是弱电解质存在电离平衡,而强电解质不存在电离平衡。因此只要证明有电离平衡存在,就证明了弱电解质。
本题难度:简单