��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��ΪʹFe3����Fe2����Zn2������ȫ���γ����������������Һ��pHӦ�ֱ�Ϊ3.7��9.6��4.4���ҡ�ij����п������Һ�к�������Fe3����Fe2����Ϊ��ȥ��Щ�����Ƶô���������п��Ӧ������Լ���
A��NaOH��Һ
B����ˮ
C��KMnO4��ZnCO3
D��H2O2��ZnO
�ο��𰸣�D
����������ȼ���H2O2��Fe2������ΪFe3+���ټ���ZnO����pH��3.7ʱFe3+������ȫ��
�����Ѷȣ���
2������� ����CuSO4?5H2O��һ����ɫ���壬�����������¼���ʵ�飺��ȡ�������壬���в��������Ӳ�ʲ������У����ȣ����Կ���������ɫ��ɰ�ɫ��ͬʱ�Թܿ���ˮ�����ɣ�����ȴ��ȡ�Թ���������ɫ��ĩ��������ˮ�ܽ⣬�ֵõ���ɫ��Һ���۽�����Һ������A��B��֧�Թ��У�����A�Թ��е���NaOH��Һ�ɹ۲쵽����ɫ�������ɣ��ݽ�һö������������B�Թ��У�Ƭ�̺�ȡ���������������渽��һ���ɫ���ʣ����û�ѧ����ʽ��ʾ�����仯����ָ���������ķ�Ӧ�����ͣ�
��1�����ȵ������壺______��______��
��2��A�Թ��з�Ӧ��______��______��
��3��B�Թ��з�Ӧ��______��______��
�ο��𰸣���1��CuSO4?5H2O���ȶ������ȷֽ�����CuSO4��H2O����Ӧ�ķ���ʽΪCuSO4?5H2O��.CuSO4+5H2O����
�ʴ�Ϊ��CuSO4?5H2O��.CuSO4+5H2O�����ֽⷴӦ��
��2����ɫ����ΪCu��OH��2��CuSO4��NaOH�������ֽⷴӦ����Cu��OH��2��Na2SO4����Ӧ�ķ���ʽΪCuSO4+2NaOH=Cu��OH��2��+Na2SO4��
�ʴ�Ϊ��CuSO4+2NaOH=Cu��OH��2��+Na2SO4�����ֽⷴӦ��
��3���������渽��һ���ɫ���ʣ�ӦΪCu��˵��Fe��Cu���ã��ɷ����û���Ӧ������ʽΪCuSO4+Fe=FeSO4+Cu��
�ʴ�Ϊ��CuSO4+Fe=FeSO4+Cu���û���Ӧ��
���������
�����Ѷȣ�һ��
3��ʵ���� ��6�֣���Ȫʵ����һ����Ȥʵ�顣����250mL����ƿ����ij���������ʵ�顣�貣�����ܳ�35cm���� ͷ�ι��пɼ���0.50mLˮ�������������ʵ���ʧ��
ͷ�ι��пɼ���0.50mLˮ�������������ʵ���ʧ��
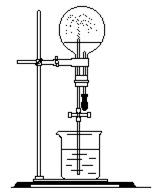
��1��0.5mLˮ������Ҫ�ܽ���������壨��״������ˮ���ܴӼ�������������ˮ�汣�ֲ��䣩��
��2������������������Ȫʵ�����____������ѡ����ѡ���Ʒ֣�
����
| A
| B
| C
| D
| E
|
�ܽ�ȣ������
| 2.6
| 40
| 5.8
| 10.2
| 23.1
|
��3������NO2�ܽ�����Ȫʵ�飬ʵ������ƿ����Һ�����ʵ���Ũ��Ϊ���٣���������λ��Ч���֣�
�ο��𰸣��Ŵ���17mlʱ�ܽ�����Ȫʵ���BE(��ѡ����ѡ���Ʒַ�)��0.045mol/L
�����������
�����Ѷȣ���
4������� ��ʵ��������ȡ����ϩ�г�����������������ij��ѧ����С���������ͼ��ʾʵ�飬��ȷ��������������к�����ϩ�Ͷ�����������д���пհף�
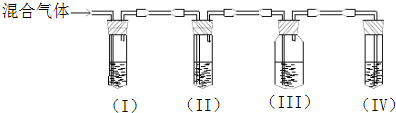
��1����˵��SO2������ڵ�������______��
��2��ʹ��װ�â��Ŀ����______���йط�Ӧ�����ӷ���ʽ��______��
��3��ʹ��װ�â��Ŀ����______��
��4��ȷ��������ϩ��������______����ϩ����ˮ��Ӧ�Ļ�ѧ����ʽΪ______��
�ο��𰸣���ϩ����NaOH��Һ��Ӧ����������������Ӧ��SO2+2NaOH=Na2SO3+H2O�������������Ƿ���ڿ���Ʒ����Һ���飮��ϩ�ļ���Ӧ�����ų�SO2�ĸ��ź���У�ѡͨ��Ʒ����Һ��ɫ����SO2�Ĵ��ڣ���ͨ��NaOH��Һ��ȥSO2����ͨ��Ʒ����Һ����ɫȷ��SO2�ѳ��ɾ�������ø������������Һ��ɫʵ�������ϩ��
��1�����������Ƿ���ڿ���Ʒ����Һ���飬Ʒ����Һ��ɫ˵�����ж�������
�ʴ�Ϊ��װ�â���Ʒ����Һ��ɫ��
��2����ϩ�Ͷ���������ʹ��ˮ��������������Һ��ɫ����������Ĵ���Ӱ����ϩ�ļ��飬�ʼ�����ϩʱӦ�ȳ�ȥ���������йط�Ӧ�����ӷ���ʽ��SO2+Br2+H2O�T4H++SO42-+2Br-��
�ʴ�Ϊ����ȥ�����������壬���������ϩ��ʵ�飬SO2+Br2+H2O�T4H++SO42-+2Br-��
��3��ͨ��NaOH��Һ��ȥSO2����ͨ��Ʒ����Һ����ɫȷ��SO2�ѳ��ɾ���
�ʴ�Ϊ��������������Ƿ������
��4������ø������������Һ��ɫʵ�������ϩ��װ�â��е����Ը��������Һ��ɫ��˵��������ϩ����ϩ����ˮ�����ӳɷ�Ӧ�ķ���ʽ��CH2=CH2+Br2��CH2BrCH2Br
�ʴ�Ϊ��װ�â��е�Ʒ����Һ����ɫ��װ�â��е����Ը��������Һ��ɫ��CH2=CH2+Br2��CH2Br-CH2Br��
���������
�����Ѷȣ�һ��
5��ʵ���� ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ijЩ������Ʊ������ʵ�ʵ�飨ͼ�мг�װ����ʡ�ԣ����밴Ҫ�����

��̽��������?�����ķ�Ӧ
��1��Ϊ��ȡ���ﰱ�����ɽ�װ��C��________����װ�ñ�ţ����ӣ�װ��C�е���ƿ�ڹ�����ѡ��_____��
a����ʯ��? b���Ȼ���? c������������? d����ʯ��
��2��װ��A��E��E���ӿ���ȡ�����������������������Eװ���ڵ�ҩƷ������_________��
��3��װ��F������̽�������백������֪�����백���ɷ�����Ӧ��3Cl2+2NH3��N2+6HCl���ķ�Ӧ��ʵ��ʱ����1��3���ر�2��������ƿ��ͨ��________��Ȼ��ر�1��3����2������ƿ�л���ͨ��һ��������һ�����塣ʵ��һ��ʱ�����ƿ�ڳ���?Ũ��İ��̲��������ڱ����ᣬ�����һ��ʵ�鷽�������ù����е�������___________________��
��̽��ijЩ���ʵ�����
��4������װ��A��E�������ʵ��Ƚ�Cl-��Br-�Ļ�ԭ��ǿ������֤�����۵�ʵ�������� __________________________��
��5��������װ��A��E������ϩ����ˮ��Ӧ��ʵ�飬�����װ��A���еĸĶ���______��
��6����װ��B��C�ֱ���F��������H2S��SO2��Ӧ��ʵ�顣�����ʵ����鷴Ӧ��F����ƿ�п���ʣ������ijɷ֡�
__________________________
�ο��𰸣���1��D��?a��d
��2������ʳ��ˮ��Ũ����
��3��������ȡ�����������Թ��У���������NaOH��Һ�����ȣ��ڹܿ���ʪ��ĺ�ɫʯ����ֽ������������壬��ʪ��ĺ�ɫʯ����ֽ������֤����������NH4+
��4��װ��E�е�NaBr��Һ��Ⱥ�ɫ
��5������ƿ�в���һֻ�¶ȼƣ���ʹ�¶ȼ�ˮ����û����ƿ��Һ����
��6����ƿ����������һ��մʪ���Ʒ����ֽ����ƿ�ڣ���ɫ֤��ʣ������Ϊ������������һ��մʪ��Ĵ���Ǧ��ֽ����ƿ�ڣ����֤��ʣ������Ϊ����
���������
�����Ѷȣ�һ��