��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���¿�ͼ��A��M����ѧ��ѧ���������ʣ�����A��E�ǽ�����F��JΪ���嵥�ʣ������Ϊ�����������Һ��CΪ����ɫ���壬DΪ����ɫ��ĩ��MΪ���ɫ���壮
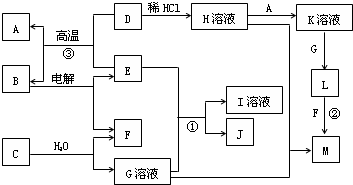
��ش��������⣺
��1��B�Ļ�ѧʽ______��
��2��19.5gC��������ˮ��Ӧת�Ƶ��ӵ����ʵ���Ϊ______mol��
��3������H��Һ�������ɡ����գ����յõ��Ĺ������ʵĻ�ѧʽ______��
��4��д���ٷ�Ӧ�����ӷ���ʽ______��
��5��д���ڡ��۷�Ӧ�Ļ�ѧ����ʽ��______����______��
�ο��𰸣�CΪ����ɫ���壬����ˮ��Ӧ����G��Һ��F���嵥�ʣ���CΪNa2O2��GΪNaOH��FΪO2��
DΪ����ɫ��ĩ��ΪFe2O3��MΪ���ɫ���壬ΪFe��OH��3����D����
���������
�����Ѷȣ�һ��
2������� �Ե���AΪԭ�Ͽ����Ƶ���������ζ��H���ְ����·�ʽ���кϳɸ����ϣ�������A��B��C��D��E��F��Ϊ�л��ͬʱ������ijЩ������ʡ�ԣ�
��֪��RCH2Cl��NaOH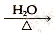 RCH2OH��NaCl
RCH2OH��NaCl

��ش��������⣺
��1��A�Ļ�ѧʽΪ______��B������Ϊ______��
��2��д���٢ڵķ�Ӧ���ͣ���______����______��
��3��C��D�Ļ�ѧ����ʽΪ______��
��4��F+E��H�Ļ�ѧ����ʽΪ______��
��5��д��C������ͬ���칹��Ľṹ��ʽ______��______��
�ο��𰸣���11�֣���1����C6H10O5��n��1�֣������ǣ�1�֣�?��2��ȡ��?��1�֣�������1�֣�
��3��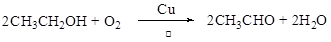 ��2�֣�
��2�֣�
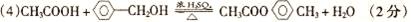
��5��CH3CH2OH��CH3OCH3��ֻд��1����1�֣�д2����3�֣�������������ͬ�����֣�
�������������ˮ�����������ǣ���B�������ǡ���������ø�������·ֽ������Ҵ�����C���Ҵ����Ҵ������к����ǻ����ܷ���������������ȩ����D����ȩ����ȩ����ȩ���������������Ȼ�����E�����ᡣ�ױ��ڹ��յ������·���ȡ����Ӧ������±������±�������������Ƶ���Һ�з���ˮ�ⷴӦ���ɴ�����F�DZ��״������״������ᷢ��������Ӧ�������ᱽ����H��
�����Ѷȣ�һ��
3������� ��12�֣�A��G�����ʼ�Ĺ�ϵ����ͼ������B��DΪ��̬���ʡ�
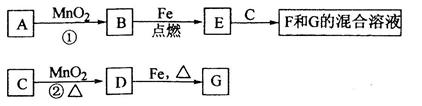
��ش��������⣺
(1)����C��E�����Ʒֱ�Ϊ?��?��
(2)��ѡ�ò�ͬ��A���з�Ӧ�٣������ڳ����½��У��仯ѧ����ʽΪ?��
��ֻ���ڼ�������½��У���Ӧ��A�Ļ�ѧʽ������ʽ��Ϊ?��
(3)��Ӧ�ڵĻ�ѧ����ʽΪ? ?��
?��
(4)�����Ƶ�F��ҺӦ����?�Է�ֹ��ת��ΪG������G��Һ�������ӵij����Լ���?���ѧʽ����ʵ������Ϊ?��
�ο��𰸣���12�֣� ?��1��Ũ���ᣨ1�֣���������������1�֣� 2H2O2
?��1��Ũ���ᣨ1�֣���������������1�֣� 2H2O2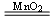 2H2O+O2����2�֣�, ?KClO3��1�֣�(3) MnO2+4HCl(Ũ)
2H2O+O2����2�֣�, ?KClO3��1�֣�(3) MnO2+4HCl(Ũ) MnCl2+Cl2��+2H2O��2�֣�? (4)���ۣ�1�֣���KSCN��2�֣�����Һ��죨2�֣�
MnCl2+Cl2��+2H2O��2�֣�? (4)���ۣ�1�֣���KSCN��2�֣�����Һ��죨2�֣�
�����������
�����Ѷȣ���
4������� A��B��C��D��E����ѧ�����ļ��ֻ����A��B�������Ԫ��X��Y�ĵ����������г����Ľ�����������ʼ�Ĺ�ϵ����ͼ��ʾ��
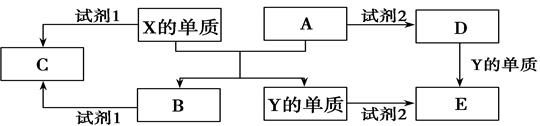
�ش��������⣺
��1��X�ĵ�����A��Ӧ�Ļ�ѧ����ʽ��________________________________��
��2����C��Һ�Լ��ԣ����Լ�1��? ____��Һ(д��ѧʽ)����C��Һ�����ԣ��������Ե�ԭ����(�����ӷ���ʽ��ʾ)?��
��3�����Լ�1���Լ�2����ϡ���ᡣ
�ټ�������D����Һ�н������ӵķ�����?��
��д��D��E��Ӧ�����ӷ���ʽ?��
��ij��Ч��ˮ������Y(OH)SO4�ۺϵõ��ġ���ҵ����E��ϡ�������������(NaNO2)Ϊԭ�����Ʊ�Y(OH)SO4����Ӧ����NO���ɣ��÷�Ӧ�Ļ�ѧ����ʽ�ǣ�?��
�ο��𰸣���1��2Al��Fe2O3 2Fe��Al2O3
2Fe��Al2O3
��2��NaOH(��OH-)��Al3����3H2O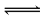 Al(OH)3��3H��
Al(OH)3��3H��
��3����ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ����Fe3��
��2Fe3����Fe=3Fe2��?��2FeSO4��2NaNO2��H2SO4=2Fe(OH)SO4��Na2SO4��2NO��
���������Ԫ��X��Y�ĵ����������г����Ľ�����Y�����������XΪAl��YΪFe��A��B���������Al����������Ӧ����Fe����������Al�����������������ᷴӦ������Ӧ����Fe���������������ᷴӦ����C��Һ�Լ��ԣ����Լ�1ΪNaOH��Һʱ��CΪƫ�����ƣ���C��ҺΪ���ԣ�CΪǿ���Ӧ�����Σ��Լ�2Ϊ����ʱ��DΪ��������EΪ�����������Լ�1Ϊ����ʱ��CΪ������������Һˮ�������ԣ�
��1��X�ĵ�����A��ӦΪ���ȷ�Ӧ����Al����������Ӧ������������Fe���÷�ӦΪFe2O3+2Al
Al2O3+2Fe��
��2����C��ҺΪ���ԣ��Լ�1��NaOH��Һ����Al��NaOH��Һ��Ӧ����ƫ�����ƺ����������ӷ�ӦΪ2Al+2H2O+2OH-�T2AlO2-+3H2�����ʴ�Ϊ��2Al+2H2O+2OH-�T2AlO2-+3H2������C��Һ�����ԣ��������Ե�ԭ����Al3����3H2O Al(OH)3��3H��
Al(OH)3��3H��
��3�����Լ�1���Լ�2����ϡ���ᣬ
��DΪ�����������������ӵķ���Ϊȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ�к���Fe3+��
�ʴ�Ϊ��ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ�к���Fe3+��
��д��D��E��Ӧ�����ӷ���ʽ2Fe3����Fe=3Fe2����
��EΪ������������ϡ�������������Ϊԭ������Fe��OH��SO4����Ӧ����NO���ɣ��÷�ӦΪ2FeSO4+2NaNO2+H2SO4�T2Fe��OH��SO4+Na2SO4+2NO����
�ʴ�Ϊ��2FeSO4+2NaNO2+H2SO4�T2Fe��OH��SO4+Na2SO4+2NO����
�����Ѷȣ�һ��
5���ƶ��� �������ʣ���Ϊ��ѧ��ѧ�������ʣ�ת����ϵ��ͼ��ʾ����֪DΪ����ɫ��ĩ����Ӧ���������ַ�Ӧ�����δȫ�������
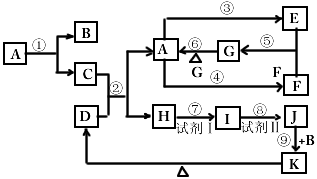
����ͼʾת����ϵ��д���пհ�
��1��д���������ʵĻ�ѧʽ��A��_________��B��_________��E��_________��K��_________��
��2��C��D�Ļ����ͨ������_________�������ƣ�
��3��д�����л�ѧ��Ӧ����ʽ��ע����Ӧ�������������ӷ�Ӧ��д���ӷ���ʽ����
��__________________����__________________����__________________��
�ο��𰸣���1��A��Al2O3��B��O2��E��NaAlO2��K��Fe(OH)3
��2�����ȼ�
��3����2Al2O3 4Al+3O2������2Al+Fe2O3
4Al+3O2������2Al+Fe2O3 Al2O3+2Fe����Al3++3AlO2-+6H2O=4Al(OH)3��
Al2O3+2Fe����Al3++3AlO2-+6H2O=4Al(OH)3��
���������
�����Ѷȣ�һ��