��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��д��ȷ����
A.���������Һ��ͨ�������CO2? Ca2++2ClO-+H2O+CO2====CaCO3��+2HClO
B.����������Һ�������� ?2OH-+Cl2====Cl-+ClO-+H2O
C.��������������Һ��Ӧ ?HCl+Ag+====AgCl��+H+
D.����ͨ��ˮ�� ?Cl2+H2O====2H++Cl-+ClO-
�ο��𰸣�B
���������A���й���CO2Ӧ����Ca��HCO3��2��C����HClӦ�����ӣ�D����HClOӦ�Ƿ��ӡ�
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�У�������������ԭ��Ӧ����
A.2H2O22H2O+O2��
B.2Al��OH��3Al2O3+3H2O
C.Fe2O3+3CO2Fe+3CO2
D.Cl2+2NaOH�TNaCl+NaClO+H2O
�ο��𰸣�B
�����������������ѧ��Ӧ�д���Ԫ�صĻ��ϼ۵ı仯����÷�ӦΪ������ԭ��Ӧ�������ǣ��Դ������
���A.2H2O2 2H2O+O2����OԪ�صĻ��ϼ۱仯����÷�Ӧ����������ԭ��Ӧ����A��ѡ��
2H2O+O2����OԪ�صĻ��ϼ۱仯����÷�Ӧ����������ԭ��Ӧ����A��ѡ��
B.2Al��OH��3 Al2O3+3H2O�У���Ԫ�صĻ��ϼ۲��䣬������������ԭ��Ӧ����Bѡ��
Al2O3+3H2O�У���Ԫ�صĻ��ϼ۲��䣬������������ԭ��Ӧ����Bѡ��
C��Fe2O3+3CO 2Fe+3CO2�У�Fe��CԪ�صĻ��ϼ۱仯����÷�Ӧ����������ԭ��Ӧ����C��ѡ��
2Fe+3CO2�У�Fe��CԪ�صĻ��ϼ۱仯����÷�Ӧ����������ԭ��Ӧ����C��ѡ��
D��Cl2+2NaOH�TNaCl+NaClO+H2O�У�ClԪ�ػ��ϼ۱仯����÷�Ӧ����������ԭ��Ӧ����D��ѡ��
��ѡB��
���������⿼��������ԭ��Ӧ����ȷԪ�صĻ��ϼ۱仯�ǽ����Ĺؼ�����Ŀ�ϼ�
�����Ѷȣ�����
3��ѡ���� ��ˮ��Ӧ���ɼ�ų��������
A.F2
B.Na2O
C.Na2O2
D.K
�ο��𰸣�CD
���������2Na2O2+2H2O====4NaOH+O2��? 2K+2H2O====2KOH+H2��
�����Ѷȣ���
4��ѡ���� ��10.2gþ�����Ļ�ͷ�ĩ����500mL?4mol?L-1�������У�������2mol?L-1������������Һ��Ҫʹ�����ij������������������������������Һ�����Ϊ
A.100ml
B.500mL
C.1000mL
D.1500mL
�ο��𰸣�C
����������������������֪�����ǡ����ȫ�к�ʱ�����ij�����������������������������Ƶķ�Ӧ�Ĺ�ϵ�����㣮
���������ij��������������Ԫ�غ���Ԫ����NaCl���ڣ�
���൱�����ǡ���к�ʱ���������
������������������Һ�����ΪΪx��
��? ?HCl��NaOH
? ?1? 1
0.5L��4mol/L? x��2mol/L
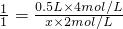 ��
��
���x=1L=1000mL��
��ѡC��
���������⿼��������ἰ����Ӧ����ȷ���ɳ������ʱ������Ԫ�صĴ�����ʽ�ǽ����Ĺؼ���Ȼ�����ù�ϵʽ�����ɼ�����
�����Ѷȣ�һ��
5��ѡ���� ��һС���ƾ����ڿ����У�������ɵIJ�����
A.Na2O2
B.NaHCO3
C.Na2CO3
D.Na2CO3��10H2O
�ο��𰸣�C
������������ڿ����о��ã���仯�����ǣ�Na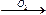 Na2O
Na2O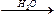 NaOH
NaOH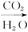 ?Na2CO3��10H2O
?Na2CO3��10H2O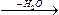 Na2CO3��
Na2CO3��
�����Ѷȣ�һ��