微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
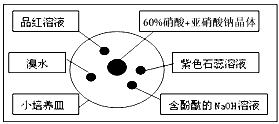
1、选择题 下图是研究二氧化硫性质的微型实验装置。现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气。下列说法中错误的是
[? ]
A.紫色石蕊溶液变蓝色
B.品红溶液褪色
C.溴水橙色褪去
D.含酚酞的NaOH溶液红色变浅
参考答案:A
本题解析:
本题难度:简单
2、选择题 把SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,产生白色沉淀,在上述一系列变化过程中,氧化剂是( )
A.SO2
B.SO42-
C.Fe3+
D.HNO3
参考答案:由滴入BaCl2溶液,则会产生白色沉淀,则可知具有还原性的SO2通入Fe(NO3)3溶液中发生的氧化反应为
SO2→SO42-,白色沉淀为硫酸钡沉淀;三价铁离子具有氧化性被还原为亚铁离子,溶液由黄色变为浅绿色,但立即又变为黄色,说明又被氧化为三价铁离子,则可知溶液中的硝酸根离子在酸溶液中具有强氧化性,把亚铁离子氧化为三价铁离子,起氧化性的是硝酸;
故选D.
本题解析:
本题难度:简单
3、选择题 下列物质不能使酸性高锰酸钾溶液褪色的是( )
A.二氧化硫
B.乙烯
C.丙烷
D.间二甲苯
参考答案:C
本题解析:
本题难度:简单
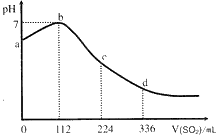
4、选择题 标准状况下,某同学向100mL H2S饱和溶液中通入SO2, 所得溶液pH变化如图所示。下列分析中,正确的是
[? ]
A.ab 段反应是:SO2 + 2H2S=3S↓+2H2O
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05mol・L-1
D.b 点对应的溶液导电性最强
参考答案:A
本题解析:
本题难度:一般
5、填空题 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验.
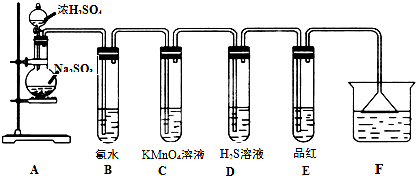
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是______、______;
(2)反应后,装置B中发生的现象是______,反应的离子方程式为______;装置C中的现象是______,表现了SO2的______;装置D中现象是______,发生反应的化学方程式为______;
(3)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象______.
(4)F装置的作用是______,漏斗的作用是______.
参考答案:(1)根据反应的原理和实验的需要,装置A中盛放浓硫酸的为分液漏斗,盛放亚硫酸钠的仪器是圆底烧瓶,
故答案为:分液漏斗;圆底烧瓶;
(2)二氧化硫中硫元素是+4价,是中间价态,既有还原性,又有氧化性,氯气为黄绿色的气体,其溶液为黄绿色,具有强氧化性,能氧化二氧化硫中+4价的硫,生成硫酸和盐酸,溶液褪色;酸性高锰酸钾有强氧化性,也能氧化二氧化硫中+4价的硫,所以二氧化硫能被酸性高锰酸钾溶液氧化而褪色,同时说明二氧化硫有还原性;硫化氢中的硫为-2价,与二氧化硫作用,二氧化硫表现为氧化性,被还原成0价的硫,
故答案为:溶液褪色;SO2+Cl2+2H2O=H2SO4+2HCl;溶液紫色褪去;还原性;有黄色沉淀生成;2H2S+SO2=2H2O+3S;
(3)二氧化硫具有漂白性,能使品红溶液褪色,但加热褪色后的品红溶液,溶液的颜色能复原,
故答案为:将试管E在酒精灯上加热,溶液恢复红色;
(4)1体积水中能溶解40体积的二氧化硫,所以用水可吸收二氧化硫,倒扣的漏斗溶液上升具有缓冲作用,能防止倒吸,故答案为:吸收多余的二氧化硫;防止倒吸;
本题解析:
本题难度:一般