微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题
为了探究草酸(H2C2O4)的化学性质,设计如下3个实验:
实验1:取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
(1)该实验说明草酸具有________(填“氧化”或“还原”)性,该反应的反应速率先慢后快的主要原因可能是__________________。
实验2:取少量草酸晶体装入试管,加水溶解,向试管里滴加足量的澄清石灰水,有白色沉淀生成。
(2)该实验说明草酸具有______性。写出反应的化学方程式:__________________。
实验3:草酸在常温下呈无色晶体状,其晶体的熔化温度低于草酸的分解温度,且易升华。为了探究草酸的不稳定性,某同学设计如下实验装置
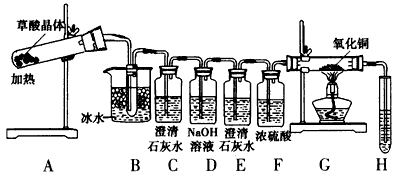
(3)B装置的作用是__________________。C装置变浑浊,E处无现象,G玻璃管里黑色变红色,写出A中反应的化学方程式:__________________。
(4)为了检验G中反应的氧化产物,H试管所装试剂是___________,从环境保护角度来看,该方案的不足之处是________________________。
2、选择题 下列实验结论不正确的是
?
| 实验操作
| 现象
| 结论
|
A
| 某有机物与溴的四氯化碳溶液混合
| 溶液褪色
| 有机物含碳碳双键
|
B
| 乙醇与重铬酸钾(K2Cr2O7)溶液混合
| 橙色溶液变为绿色
| 乙醇具有还原性
|
C
| 常温下,将二氧化碳通入苯酚钠溶液
| 溶液变浑浊
| 酸性:碳酸>苯酚
|
D
| 苯和苯酚稀溶液分别与浓溴水混合
| 后者产生白色沉淀
| 羟基影响了苯环的活性
3、实验题 某学生试图用电解法根据电极上析出的物质的质量来测定阿伏加德罗常数值。其实验方案的要点为:
①用直流电电解氯化铜溶液,所用仪器如图;
②在电流强度为I安培,通电时间为t分钟后,精确测得某电极上析出的铜的质量为m克。
试回答

(1)连接这些仪器的正确顺序为(用图中标注仪器接线柱的英文字母表示)E接____,C接____,____接F。
(2)写出B电极上发生反应的离子方程式____________,G试管中淀粉KI溶液变化的现象为____________;相应的离子方程式是____________________
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序应是_____(选填下列操作步骤的编号)。
①称量电解前电极质量;②刮下电解后电极上的铜并清洗;③用蒸馏水清洗电解后电极;
④低温烘干电极后称量;⑤低温烘干刮下的铜后称量;⑥再次低温烘干后称量至恒重。
(4)已知电子的电量为1.6×10-19库仑。试列出阿伏加德罗常数的计算表达式:NA=____________。
4、实验题 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究。

(1)写出试管B中的实验现象______________________。
(2)写出A中反应的化学方程式______________________。
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______________________。若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)___________、
___________。
(4)B试管口的棉花应沾有的试剂是___________。
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4・xH2O)。小组成员采用加热法测定该晶体里结晶水x的值。
①在他们的实验操作中,至少称量___________次;
②下面是其中一次实验的数据:
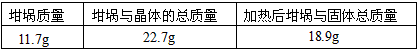
根据上表数据计算判断x的实侧值比理论值(x=5)________(填“偏大”、“偏小”),这次实验中产生误差的原因可能是___________(填序号)
A.硫酸铜晶体中含有不挥发的杂质
B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去
D.加热失水后露置在空气中冷 却
5、实验题 某研究性学习小组设计实验探究铝等金属的性质:将铝片(不除氧化膜)投入浓氯化铜溶液中,铝表面很快出现一层海绵状暗红色物质,接下来铝片上产生大量气泡。触摸容器知溶液温度迅速上升,收集气体,检验其具有可燃性。若用同样的铝片投入同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
⑴铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因可能是______________。
A.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强?
B.硫酸铜水解生成硫酸使铝钝化
C.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能?
D.生成氯化铝溶于水,而生成硫酸铝不溶于水
请设计一个简单实验验证你的选择:__________________。?
⑵铝片表面出现的暗红色物质的过程中发生的离子反应方程式是_____________。?用离子方程式解释产生气泡的原因:_____________。
⑶放出的气体是_______________,请从有关物质的浓度、能量、是否有电化学作用等分析开始阶段产生气体的速率不断加快的原因是_______________?。(写出一点即可)
⑷某同学通过一定的实验操作,也能使铝片与硫酸铜溶液反应加快,他采取的措施可能是___________________?。
A.用砂纸擦去铝片表面的氧化膜后投入硫酸铜溶液中?
B.把铝片投入热氢氧化钠溶液中一段时间后,取出洗涤,再投入硫酸铜溶液中
C.向硫酸铜溶液中滴加氢氧化钠溶液,再投入铝片
D.在铝片上捆上几枚铜钉后投入同浓度的硫酸铜溶液中
⑸除去氧化铝的铝片与铜片为电极,在X电解质溶液中构成原电池,列表如下:
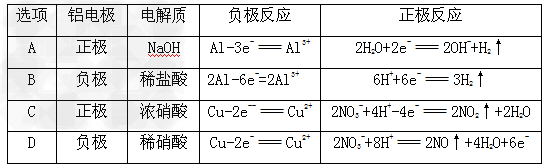
其中正确的是____________?,由此推知,金属作电极不仅与本身性质相关,而且与? __________?有关。
|