��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��FeI2��FeBr2�Ļ����Һ��ͨ��������������Һ��ijЩ���ӵ����ʵ����仯��ͼ��ʾ��
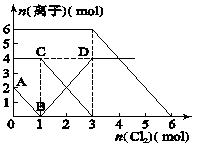
��֪��2Fe2����Br2===2Fe3����2Br����2Fe3����2I��===2Fe2����I2���������й�˵���У�����ȷ����(����)
A��ԭ�����Һ��FeBr2�����ʵ���Ϊ6 mol
B���߶�BD��ʾFe3�����ʵ����ı仯
C����ͨ��2 mol Cl2ʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��2Fe2����2I����2Cl2===2Fe3����I2��4Cl��
D��ԭ��Һ�У�n(Fe2��)��n(I��)��n(Br��)��2��1��3
�ο��𰸣�A
�����������Һ�����ӵĻ�ԭ��ǿ����ϵΪ��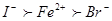 �����ԣ�A��BΪI��������Ӧ���ɷ���ʽ
�����ԣ�A��BΪI��������Ӧ���ɷ���ʽ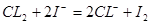 �ɵã���Һ��I�������ʵ���Ϊ2mol��C��DΪFe2+������Ӧ���ɷ���ʽ
�ɵã���Һ��I�������ʵ���Ϊ2mol��C��DΪFe2+������Ӧ���ɷ���ʽ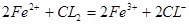 �ɵã���Һ��Fe2+�����ʵ���Ϊ4mol�����ΪBr�����ӷ�����Ӧ���ɷ���ʽ
�ɵã���Һ��Fe2+�����ʵ���Ϊ4mol�����ΪBr�����ӷ�����Ӧ���ɷ���ʽ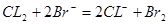 �ɵã���Һ��Br�������ʵ���Ϊ6mol��
�ɵã���Һ��Br�������ʵ���Ϊ6mol��
������ȷѡ��ΪA��
�����Ѷȣ�����
2��ѡ���� ���������У������¼��ܸ����ᷴӦ�����ܸ�NaOH��Һ��Ӧ����
[? ]
A��Mg
B��Al
C��Si
D��Cl2
�ο��𰸣�B
���������
�����Ѷȣ���
3��ѡ���� CsICl2��һ�ּ�����Ķ�±������������ڻ�ѧ��Ӧ�мȿɱ����������ֿɱ��ֻ�ԭ�ԣ��йظ����ʵ�˵����ȷ����?��?��
A��Cs��+3�ۣ�I ��Cl ���ԣ�1
B��Cs�� +1�ۣ�Cl��+1�ۣ�I�ԣ�1�ۡ�
C����CsICl2��Һ��ͨ��Cl2 ,�е��ʵ�����
D����CsICl2��Һ��ͨ��SO2���壬����������
�ο��𰸣�D
�����������
�����Ѷȣ���
4������� ������һ����Ҫ�Ļ���ԭ�ϣ�ijѧϰС����ʵ������������ͼ��ʾװ����ȡ������̽�������ʣ�
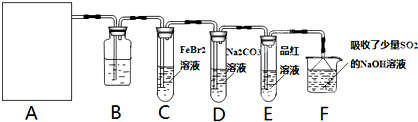
��1����A���ö������̺�Ũ���ᷴӦ��ȡ�����ķ���װ�ã���Բ����ƿ�͵�����õ��IJ���������______��
��2����װ��B��ʢ�е��Լ���______��������______��
����E��Ʒ����Һ��ɫ����Cװ���з�����Ӧ�����ӷ���ʽ��______��֤��FeBr2��Cl2������������ԭ��Ӧ��ʵ�鷽����______���������������
����֪̼�������ǿ�ڴ����ᣬ��װ��D�з�Ӧ�Ļ�ѧ����ʽΪ______��
��3��ij�о���ѧϰС���ø����չ�����SO2��NaOH��Һ���մ�������ʵ����β��������β��һ��ʱ�������Һ����ǿ���ԣ��п϶�����Cl-��OH-��CO32-��SO42-�������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������������ˮ�⣻�ڼ���������ClO-Ҳ��ǿ�����ԣ�����
������������裺
����1��ֻ����SO32-��
����2��ֻ����ClO-��
����3���ȴ���SO32-��Ҳ����ClO-��
����4���Ȳ�����SO32-��Ҳ������ClO-��
ָ����ʦ��������Ϊ������һ�����貢������������______���жϵ�ԭ����______��
�����ʵ�鷽��������ʵ�飬��д��ʵ�鲽���Լ�Ԥ������ͽ��ۣ���ѡʵ���Լ���
a��3mol/L?H2SO4?b��0.01mol/L?KMnO4 c��1mol/L?BaCl2��Һ
d������һKI��Һ?e����̪��Һ?f��Ʒ����Һ
����һ��ȡ��������Һ���Թ��У��μ�3mol/L?H2SO4����Һ�����ԣ�Ȼ��������Һ��װ��A��B���Թ��У�
���������A�Թ��еμ�1��2��______?������ţ�������Һ______�������������1������
����������B�Թ��еμ�1��2��______������ţ�������Һ______�������������2������
��������2������д���������е����ӷ���ʽ��______��
�ο��𰸣���1���������̺�Ũ���ᷴӦ��ȡ�����ķ���ʽΪ��MnO2+4HCl��Ũ��?����?.? MnCl2+Cl2��+2H2O���ӷ���ʽ��֪�÷�Ӧ����ȣ���ƾ��ƣ���Ӧ��Ũ����ĵμ��Լ����������ݳ����Һ©�����ʴ�Ϊ����Һ©�����ƾ��ƣ�
��2���ٵ����Ȼ��������ͨ������ʳ��ˮʱ���Ȼ����ܽ������У������������ܣ��ʴ�Ϊ������ʳ��ˮ����ȥ�����е��Ȼ������ʣ�
����E��Ʒ����Һ��ɫ��˵������E��������������E��������˵��Cװ���У��廯�����еĶ������������Ӿ�����������FeBr2��Cl2����������ԭ��Ӧ���廯�����еĶ������ȱ�����������ֻ��֤�������������ڼ��ɣ�KSCN��Һ�����������γ�Ѫ��ɫ�����軯����֤�������������ڣ�
�ʴ�Ϊ��2Fe2++4Br-+3Cl2�T2Fe3++6Cl-+2Br2��ʵ���ȡ��װ��C��������ȡ����C����Һ���Թ��У��μ�KSCN��Һ��
�۾���װ��D�������Ⱥ�ˮ��Ӧ��Cl2+H2O=HCl+HClO��������Na2CO3��Һ��Ӧ��2HCl+Na2CO3=2NaCl+CO2��+H2O���ܷ�ӦΪ2Cl2+Na2CO3 +H2O=CO2+2NaCl+2HClO��
�ʴ�Ϊ��2Cl2+Na2CO3 +H2O=CO2+2NaCl+2HClO��?
��3����ClO-��+1�۵��Ⱦ���ǿ�����ԣ�SO32-��+4�۵�����л�ԭ�ԣ�ClO-��SO32-�ᷢ��������ԭ��Ӧ��?�ʴ�Ϊ������3��ClO-��SO32-����������ԭ��Ӧ�����ܴ������棻
�ڲ������KMnO4 ����ǿ����������л�ԭ�Ե�SO32-����������ԭ��ӦKMnO4��ɫ���ʴ�Ϊ��b����ɫ��
? ��������ClO-��+1�۵��Ⱦ���ǿ�����ԣ��ܽ��⻯����-1�۵ĵ������ɵⵥ�ʣ����������ⵥ������ɫ���ʴ�Ϊ��d������ɫ��
��������2��������������ClO-�����⻯�سɵⵥ�ʣ��ʴ�Ϊ��2I-+ClO-+2H+�TI2+H2O+Cl-��
���������
�����Ѷȣ�һ��
5��ѡ���� ���б仯�У����������仯���ǣ��ٺ�����������ɰ��ס����Ȼ�茶������Ⱥ����Թܵײ��Ƶ��Թ��ϲ����۹�������ȱ�ɵ��������ܸɱ���������Ũ�������ɫҺ���ɻ�ɫҺ��
A���٢ڡ���
B���ۢܡ���
C���ܢݡ���
D���ۢܢ�
�ο��𰸣�B
�����������
�����Ѷȣ���