|
高考化学知识点总结《物质的量》试题巩固(2017年最新版)(二)
2017-08-08 05:44:27
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。已知空气的平均相对分质量为29,则A的相对分子质量是 ( )
A.29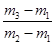
B.29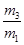
C.29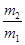
D.29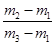
|
参考答案:A
本题解析:真空瓶质量为m1,该瓶充入空气后质量为m2.令气体的物质的量为n,则:m1g+n×29g/mol=m2g,n=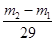 ,在相同状况下,若改为充入某气体A时,总质量为m3.所以A的质量为(m3-m1)g,物质的量为 ,在相同状况下,若改为充入某气体A时,总质量为m3.所以A的质量为(m3-m1)g,物质的量为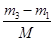 ,同温同压下,空气和A气体的物质的量相等,故 ,同温同压下,空气和A气体的物质的量相等,故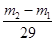 = =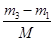 ,M=29 ,M=29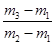 ,答案选A. ,答案选A.
考点:物质的量的有关计算
本题难度:一般
2、计算题 容积为30ml充满NO2、O2混合气体的试管倒立在水槽中,最后试管内剩余气体5ml, 则原混合气体中O2的体积为 ml,或 ml。
参考答案:10mL 3 mL
本题解析:试管内剩余气体5ml,这些剩余的气体可以是NO,也可以是O2,
当剩余气体是O2时,根据4NO2+2H2O+O2=4HNO3,即NO2:O2=4:1,即
NO2的体积=(30-5)*4/(4+1)ml=20ml,所以O2的体积为10ml;当剩余气体为NO时,即可以认为发生了4NO2+2H2O+O2=4HNO3,和3NO2+H2O=2HNO3+NO↑,生成的5mlNO需要NO215ml,所以O2的体积为(30-15)*1/(4+1)ml=3ml。
考点:化学计算
点评:本题考查了化学计算,有一定的难度,注意要分两种情况进行讨论。
本题难度:一般
3、填空题 (1)0.5 mol H2O的质量为 ,其中含有 个水分子,共有 个原子。
(2)在 mL 0.2 mol/L NaOH溶液中含1 g溶质;配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4?5H2O g。(3)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为 。
参考答案:(1) 9 g 0.5NA 1.5NA (2) 125mL 2.5g (3) A-N-2
本题解析:略
本题难度:一般
4、填空题 在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g・cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是 、 。
(2)取出这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是 。
(3)在40.0 mL 0.065 mol・L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过 mL。
(4)将不纯的NaOH样品1 g(样品含少量Na2CO3和水),放入50 mL 2 mol・L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL 1 mol・L-1的NaOH溶液。蒸发中和后的溶液,最终得到 克固体。
参考答案:(1)36.5% 11.8 mol・L-1 (2)1 mol・L-1 (3)2.6 (4)5.85
本题解析:(1)n(HCl)=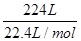 =10 mol, =10 mol,
m(HCl)=10 mol×36.5 g・mol-1=365 g,
盐酸的质量分数w=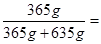 ×100%=36.5%, ×100%=36.5%,
c(HCl)=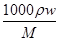
=
=11.8 mol・L-1。
(2)根据c(浓)・V(浓)=c(稀)・V(稀)
可知:c(稀)=11.8 mol・L-1×0.1 L/1.18 L=1 mol・L-1。
(3)n(Na2CO3)=0.040 L×0.065 mol・L-1
=0.002 6 mol,
设加入稀盐酸的体积最多不超过x mL,
则n(HCl)=1 mol・L-1×0.001x L=0.001x mol,
根据反应Na2CO3+HCl=NaHCO3+NaCl得0.002 6=0.001x,x=2.6。
(4)经过反应,蒸发中和后的溶液,最后所得固体为NaCl、根据Cl原子守恒:
n(NaCl)=n(HCl)=0.050 L×2 mol・L-1=0.1 mol,
m(NaCl)=0.1 mol×58.5 g・mol-1=5.85 g。
本题难度:一般
5、选择题 下列说法正确的是( )
A.水的摩尔质量是18g
B.摩尔是一种基本物理量
C.任何物质的摩尔质量都等于它的式量
D.摩尔是物质的量的单位
参考答案:D
本题解析:
本题难度:一般
|