��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ʻ�Ϻ��������������Ƶ���
A��Ba(OH)2��Na2CO3��Һ����
B��Na��H2O
C��KOH��NaCl��Һ
D��Na2O2��H2O
�ο��𰸣�C
���������C�������ʲ��ܷ�����Ӧ���������������ӷ�Ӧ������
�����Ѷȣ�һ��
2��ѡ���� ��0.5 mol����0.5 molþ�ֱ����2 mol��L��1��400 mL�������У�������Һ��������
A����������Һ��������
B��ͬ����
C������þ��Һ��������
D����ȷ��
�ο��𰸣�B��?
����������ɷ�Ӧ����ʽ֪�����߾������������
2Na��2H��===2Na����H2��������m
2 mol? 44 g
0.5 mol? 11 g
Mg��2H��===Mg2����H2��������m
1 mol? 22 g
0.5 mol? 11 g
��Һ����������ȡ������������������(��m)���йؽ������ᷴӦ������Һ�����������⡣
�����Ѷȣ�һ��
3��ѡ���� ��Na2O2Ͷ��FeCl3��Һ�У��Թ۲쵽����������ȷ����
A�����ɰ�ɫ����
B�����ɺ��ɫ����
C�������ݲ���
D�����ɺ��ɫ�����������ݲ���
�ο��𰸣�B
�����������������֪����Na2O2Ͷ��FeCl3��Һ�У������ķ�ӦΪ��2Na2O2+2H2O�T4NaOH+O2����Fe3+���������Ʒ�Ӧ��3OH-+Fe3+�TFe��OH��3�����������ɺ��ɫ��Fe��OH��3���������Կ����������ǣ��д����������ɣ��к��ɫ�������ɣ����ѡ��֪��ѡB��
�����Ѷȣ�һ��
4������� ��12�֣���ͼ����ѧ�������ʼ��ת����ϵ����֪��
��AΪ����ɫ���壬BΪ���¡�����ЧӦ������Ҫ���ʣ� ��EΪ����������JΪ���ɫ������
��G��ʵ�����г����ڼ���B�Ĵ��ڣ���L��һ����Ҫ�Ĺ�ҵԭ�ϣ�����������ըҩ��Ũ��Һ���ʻ�ɫ����������ɫƿ�С�

�ش��������⣺
��1��A�ĵ���ʽ____________________________________________________��
��2����Ӧ�ٵĻ�ѧ����ʽΪ?����Ӧ�ڵ����ӷ���ʽΪ?��
��3�����μӷ�Ӧ��A������Ϊ39g��������CO2�����������£�Ϊ?L��
��4��L�Ļ�ѧʽ?��G�Ļ�ѧʽ?��
�ο��𰸣�
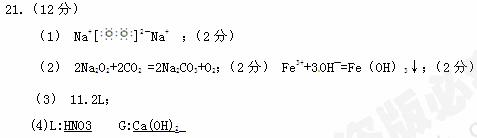
�����������
�����Ѷȣ�һ��
5��ѡ���� ��2 mol NaHCO3��һ������Na2O2�����ϣ��ڼ��ȵ�������ʹ�䷴Ӧ�����ⶨ��Na2O2ʣ�࣬��������ù�������ʵ�����n��Ϊ��?��
A��1mol��n��2mol
B��1mol��n��4mol
C��2mol��n��4mol
D��n��4mol
�ο��𰸣�B
������������ü�ֵ�����м��㣬Na2O2��Сֵ�ļ���Ϊ0��2 mol NaHCO3�ֽ�����1mol Na2CO3��Na2O2���ֵΪǡ����2mol NaHCO3�ֽ������CO2��H2O��ȫ��Ӧ��1mol������̼�������Ʒ�Ӧ����1mol̼���ƣ�1molˮ�������Ʒ�Ӧ����2mol�������ƣ��ټ���2 mol NaHCO3�ֽ����ɵ�1mol Na2CO3����������ù�������ʵ���Ϊ4mol����B����ȷ��
�����Ѷȣ�һ��