微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验。(夹持装置已略去)
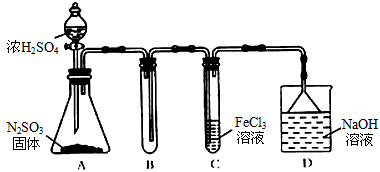
(1)在配制氯化铁溶液时需先把氯化铁晶体溶解在_________ 中,再加水稀释,这样操作的目的是______________________,操作中不需要的仪器有____(填入正确选项前的字母);
a.药匙 b.烧杯 c.石棉网 d.玻璃棒 e.坩埚
(2)通入足量SO2时C装置中观察到的现象为____________________
(3)根据以上现象,该小组同学认为SO2与Fe3+反应生成SO42-和Fe2+。
①写出SO2与Fe3+反应的离子方程式________________________;
②请设计实验方案检验C试管中生成的Fe2+:________________________
③该小组向C装置反应后的溶液中加入稀硝酸酸化的BaCl2溶液,出现白色沉淀,证明反应生成了SO42-,该做法______(填“合理”或“不合理”),理由是__________________
(4)D装置中倒置漏斗的作用是___________________
(5)为了验证SO2具有还原性,实验中可以代替FeCl3溶液的试剂是_________(填字母)
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.Na2S溶液
参考答案:(1)浓盐酸;抑制氯化铁水解;ce
(2)溶液由棕黄色变为浅绿色
(3)①2Fe3++SO2+2H2O=SO42-+4H++2Fe2+;②取装置C中反应后的溶液,向其中滴入KSCN溶液,不变 红,再加新制氯水,溶液变红(合理即可);③不合理;硝酸可以将溶解的SO2氧化为H2SO4,干扰实验 (4)使气体充分吸收、防止溶液倒吸
(5)bc
本题解析:
本题难度:一般
2、实验题 某学习小组做以下实验:在溴水中加入足量乙醛溶液,充分反应,溴水褪色;为探究褪色的原因,他们提出了如下猜想:
①溴水中的Br2可能与乙醛发生取代反应,产生HBr;
②乙醛分子中含有不饱和键,溴水可能与乙醛发生加成反应;
③乙醛具有还原性,溴水可能将乙醛氧化为乙酸,Br2转化为HBr。
设计如下方案进行探究:
方案(一):检验褪色后溶液的酸碱性,确定其发生哪类反应;
方案(二):测定反应前溴水中Br2的物质的量和反应后Br-的物质的量确定其发生哪类反应;
(1)假设测得反应前溴水中Br2的物质的量为amol,
若测得反应后n(Br-)=0mol,说明溴水与乙醛发生了__________反应;
若测得反应后n(Br-)=amol,说明溴水与乙醛发生了__________ 反应;
若测得反应后n(Br-)=2amol,说明溴水与乙醛发生了__________ 反应。
(2)向含Br2 0.005mol的溴水中加入足量乙醛使其褪色,然后加过量的AgNO3溶液,过滤.洗涤.干燥.称量,得到固体1.88g。已知CH3COOAg易溶于水,通过计算,判断溴水与乙醛发生的反应为(填序号):__________
①氧化反应 ②取代反应 ③加成反应
(3)方案(一)是否可行?______ (填“是”或“否”), 原因是:__________________________。
参考答案:(1)加成(②);取代(①);氧化(③)
(2)①
(3)否;因为如果发生的是取代反应,也生成HBr使溶液显酸性
本题解析:
本题难度:困难
3、实验题 (14分)某研究性学习小组设计了如图所示的定量测定装置,其中B是底面积为100cm2、高20cm的圆筒状玻璃容器(带密封盖),上面标有以厘米为单位的刻度。其他夹持装置已略去。

I.甲同学用这套装置测定出了空气中氧气的体积分数,他的操作过程是:
①检查装置的气密性;
②打开B容器密封盖,加入液体C,调整A的高度,使B中液面至刻度15.0cm处;
③将过量的铁粉平铺在电热板上,盖紧容器B的密封盖;
④通电加热铁粉,待充分反应后,冷却到原来的状况,调整A的高度使容器A、B中的液面保持水平,记录液面刻度。
请回答下列问题:
(1)在操作①中检查装置气密性的方法是__________________________? __。
(2)在该同学的实验中,下列物质不能用于代替铁粉的是______。
A.红磷? B.木炭? C.铜粉
(3)在操作④结束时,与装置B中的液面最接近的刻度是______cm(填整数)。
II.乙同学欲用此装置测定铁在氯气中燃烧产物的化学式。他的操作与甲不同之处有:将操作③中铁粉的质量改为1.0g,并使容器B充满氯气后,再盖紧容器。请回答下列问题:
(1)在乙同学的实验中,下列试剂中适合于做液体C的是_______。
A.水? B.氢氧化钠溶液? C.饱和食盐水
(2)实验结束时,液面在刻度8.8cm处。若将当时的实验条件近似看作标准状况,请据此计算生成物FeClx中x的值是______(计算结果保留1位小数)。
(3)上面的实验结果比理论值________(填“偏大”或“偏小”),误差产生的原因可能是____________________________________________________________。
参考答案:.I(1)盖严B容器密封盖,向A中加水,使A中液面高于B中的液面,一段时间后,A、B液面差高度不变,则气密性良好。?(2)B?(3)12
II(1)C?(2)3.1?(3)偏大?氯气溶于水;漏气;读数时A中液面高于B。(其他合理答案也可给分)
本题解析:略
本题难度:一般
4、简答题 (14分)硒(34Se)和碲(52Te)都是第VIA族元素,硒是分布在地壳中的稀有元素。工业上硒鼓废料(主要成分硒、碲、碳、铜和铁合金)回收精炼硒的流程如下:

已知:
物理性质
| 熔点
| 沸点
| 升华
| 溶解性
|
SeO2
| 340℃
| 684℃
| 315℃
| 易溶于水
|
TeO2
| 733℃
| 1260℃
| 450℃
| 微溶于水
|
(1)Se的氢化物的电子式是______。
(2)步骤①中通入的氧气使硒鼓废料翻腾,目的是______。
(3)废气的主要成分是______;废渣II的主要成分是______。
(4)步骤④中主要反应的化学方程式是______;步骤⑥反应的化学方程式是______。
(5)根据表中数据,步骤⑤最适宜的分离方法是______。
参考答案:(14分)
(1)
(2)增大接触面积,加快反应速率,使废料充分燃烧
 (3)CO2? TeO2
(3)CO2? TeO2
(4)H2SeO3?SeO2+H2O? 2H2SO3 + SeO2=Se+2H2SO4
(5)升华,将温度控制在315℃到450℃之间
本题解析:(1)Se是第六主族元素,氢化物的化学式与H2O相似,属于共价化合物,电子式为 ;
;
(2)步骤①中通人的氧气使硒鼓废料翻腾,目的是增大接触面积,加快反应速率,使废料充分燃烧
(3)根据硒鼓废料的成分判断,废气是CO2;SeO2易溶于水,TeO2微溶于水,所以废渣主要是TeO2;
(4)SeO2溶于水生成H2SeO3,受热分解生成SeO2,化学方程式为H2SeO3 SeO2+H2O;步骤⑥发生氧化还原反应 ,根据所给反应物和产物写出其化学方程式:2H2SeO3+SeO2=Se+2H2SO4
SeO2+H2O;步骤⑥发生氧化还原反应 ,根据所给反应物和产物写出其化学方程式:2H2SeO3+SeO2=Se+2H2SO4
(5)根据SeO2和TeO2升华的温度,二者分离的最适宜方法是升华,将温度控制在315℃到450℃之间
本题难度:一般
5、选择题 下列有关实验原理或操作正确的是?
A.仅用硝酸银溶液便可鉴别亚硝酸钠和食盐
B.减压过滤是为了加快过滤速度,得到较大颗粒的晶体
C.硫酸亚铁铵晶体过滤后用无水乙醇洗涤
D.纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮
参考答案:C
本题解析:略
本题难度:一般