��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼװ���У����õ缫��Ϊ���Ե缫��ͨ��һ��ʱ���b��������Һ�ʺ�ɫ������˵������ȷ����

A��X��������Y�Ǹ���
B��a��������b�Ǹ���
C��NaCl��Һ��pH���ֲ���
D��NaCl��Һ��pH��С
�ο��𰸣�A
�����������
�����Ѷȣ���
2��ѡ���� ���й���ԭ��ص�������ȷ���� (? )
A������ԭ��ص������������������ֲ�ͬ�Ľ���
B��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ��
C����ԭ����У�����������һ���Ǹ������õ缫����ԭ
D��ԭ��طŵ�ʱ�������ķ����ǴӸ���������
�ο��𰸣�B
�������������ԭ��ص��������������ý����缫��ǽ�������̼���缫��ԭ����е���������һ������������Ӧ�������ķ����Ǵ����������·����������������ķ������෴�ġ�
�����Ѷȣ�һ��
3������� (12��)���ڵؿ��еĺ���Լռ 5 �����ҡ�����ʯ������ܶ࣬��Ҫ���д�����ʯ
����Ҫ�ɷ���Fe3O4����������ʯ����Ҫ�ɷ��� Fe2O3)�ȡ�
��1�����ȵ����ܸ�ˮ������Ӧ��һ�ֲ�������������Ҫ�ɷ���ͬ����һ�ֲ�����
��ȼ�����壬���䷴Ӧ�Ļ�ѧ����ʽΪ �� �ÿ�ȼ����������
�����£����Ƴ�ȼ�ϵ�أ�д�������巢���ĵ缫��Ӧʽ ��
��2���ڳ����£�����ˮ����Ӧ�����ڳ�ʪ�Ŀ����У������������⣨�������Ҫ�ɷ��� Fe203��������ʴ��ÿ����ʴ����ʧ�ĸֲ�ռ���������������ķ�֮һ��������Ļ�ѧԭ�����£����������ӷ���ʽ�ͻ�ѧ����ʽ����������
�� ԭ��ط�Ӧ��
������2Fe��4e-=2Fe2+�������� ��
�� ����������γɣ� Fe2 + + 2OH��=" Fe(OH)" 2�� ��
�� ��������ķֽ⣺ 2Fe(OH)3 =Fe2O3+3H2O��
��3��Ϊ�˷�ֹ�����⣬��������Ʒ�������һ��ͭ����ͼװ�ã���aΪ �������������������
����Ʒ���淢���ĵ缫��Ӧʽ Ϊ ��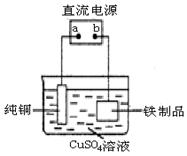
�ο��𰸣���1��3Fe+4H2O Fe3O4+4H2 ; H2��2e-=2H+
Fe3O4+4H2 ; H2��2e-=2H+
��2����O2+4e-+2H2O=4OH- ���� 4Fe(OH)2+O2+2H2O=4Fe(OH)3��
��3������ �� Cu2++2e-="Cu" ��
�����������1�����ȵ����ܸ�ˮ������Ӧ��һ�ֲ�������������Ҫ�ɷ���ͬ��ΪFe3O4����һ�ֲ����ǿ�ȼ�����壬ΪH2�����Ի�ѧ����ʽΪ��3Fe+4H2O Fe3O4+4H2�����������£�����ͨ��ȼ�ϵ�صĸ������缫��ӦʽΪ��H2��2e-=2H+
Fe3O4+4H2�����������£�����ͨ��ȼ�ϵ�صĸ������缫��ӦʽΪ��H2��2e-=2H+
��2��������O2�õ�������OH?���缫����ʽΪ��O2+4e-+2H2O=4OH-
��Fe(OH)2��O2��H2O��Ӧ����Fe(OH)3����ѧ����ʽΪ��4Fe(OH)2+O2+2H2O=4Fe(OH)3
��3��������Ʒ�϶�ͭ������ƷΪ���������ӵ�Դ�ĸ���������aΪ��Դ��������Cu2+������Ʒ����õ�������Cu���缫����ʽΪ��Cu2++2e-=Cu��
���㣺���⿼��ԭ���ԭ�������ԭ��������ʽ����д��
�����Ѷȣ�����
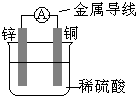
4��ѡ���� ������ͼ��ʾװ�õ���������ȷ���ǣ�������
A��ͭΪ������ͭƬ�������ݲ���
B��ͭƬ��������
C��������пƬ����������ͭƬ
D����������ͭƬ���汻��ԭ