| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ�ؿ�֪ʶ�㡶��ѧƽ�⡷��Ƶ����ǿ����ϰ��2017�����°棩(ʮ)
�ο��𰸣�C ���������A��ƽ�ⳣ�����ݷ�����ƽ�ⳣ�����¶�����С��˵��ƽ��������У����������ȷ�Ӧ�������Ƿ��ȷ�Ӧ����A����B�����º�ѹ�£����������ٳ���������Ar��ѹǿ���ֺ�ѹ��ƽ���������������ķ�����У�����ƽ�⽫�����ƶ�����C����C��80��ʱ�����ijʱ��Ni(CO)4��g����CO��g��Ũ�Ⱦ�Ϊ0.5 mol?L-1��Qc=c(Ni(CO)4)/c4(CO)=0.5/0��54=8��2��˵��ƽ��������У����ʱv��������v���棩����C��ȷ��D�����º����£����������ٳ���������Ni��CO��4��g�����൱������ѹǿƽ��������У��ﵽ��ƽ��ʱ��CO�İٷֺ�������С����D���� �����Ѷȣ����� 4��ѡ���� ��һ�������£���2 L�ܱ������г���3 mol X(g)��1 mol Y(g)���з�Ӧ�� |
�ο��𰸣�C
�����������2 L�ܱ������г���3 mol X(g)��1 mol Y(g)���з�Ӧ������Ӧ���ף�����Z="1.5" mol / L������W="1" mol / L��ʵ���Ϸ�Ӧ���ܽ��е��ף�����Z<1.5 mol / L�� W<1 mol / L �����ܵ���C��
���㣺������淴Ӧ��������
�����Ѷȣ�һ��
5������� ��10�֣�ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
��1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��
C(s)��H2O(g)  CO(g)��H2(g) ��H=��131.3 kJ?mol-1����S=��133.7J?(K?mol) -1
CO(g)��H2(g) ��H=��131.3 kJ?mol-1����S=��133.7J?(K?mol) -1
�ٸ÷�Ӧ�ܷ��Է������� �йأ�
��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� ������ĸ����ͬ����
a�������е�ѹǿ���� b��1 mol H ��H�����ѵ�ͬʱ����2 molH��O��
��H�����ѵ�ͬʱ����2 molH��O��
c��v��(CO) = v��(H2O) d��c(CO)=c(H2)
��2������ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ CO(g)��H2O(g) CO2(g)��H2(g)���õ������������ݣ�
CO(g)��H2O(g) CO2(g)��H2(g)���õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 ��
�� CH3OH(g)��H2O(g) ������ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ?mol-1)�ı仯�������Ϊ1 L�ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc (CH3OH)�������___________��
CH3OH(g)��H2O(g) ������ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ?mol-1)�ı仯�������Ϊ1 L�ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc (CH3OH)�������___________��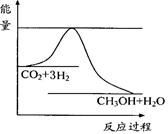
 )��ʹ��ϵѹǿ����
)��ʹ��ϵѹǿ�����ο��𰸣�(1)���¶ȣ�2�֣�
��bc��2�֣�(2)�� 0.16mol��L-1��min-1��2�֣� ������2�֣� (3)cd��2�֣�
�����������
�����Ѷȣ�����
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ�ؿ�֪ʶ�㡶���仯��.. | |
| �����Ŀ |