微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在溶液中加入过量Na2O2后仍能大量共存的离子组是
A.Fe2+、NH4+、Cl-、NO3-
B.K+、CO32-、Cl-、SO42-
C.Ca2+、Na+、NO3-、HCO3-
D.Na+、H+、Cl-、Br-
参考答案:B
本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。过氧化钠溶于水生成氢氧化钠和氧气,溶液显碱性,同时过氧化钠还具有强氧化性,则A、在碱性条件下Fe2+、NH4+均不能大量共存,且亚铁离子还具有还原性,极易被氧化,不能大量共存,A不正确;B、在碱性溶液中K+、CO32-、Cl-、SO42-均可以大量共存,B正确;C、在碱性条件下HCO3-不能大量共存,C不正确;D、在碱性溶液中H+不能大量共存,D不正确,答案选B。
本题难度:一般
2、选择题 在下列各组溶液中,离子间一定能大量共存的是(?)
A.pH=1的溶液:K 、Cu
、Cu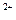 、Br
、Br 、SO
、SO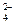
B.含有0.1 mol・L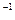 I
I 的溶液:NH
的溶液:NH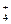 、Fe
、Fe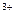 、SO
、SO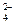 、Cl
、Cl
C.含有0.1 mol・L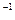 HCO
HCO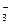 的溶液:Na
的溶液:Na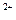 、Al
、Al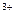 、NO
、NO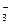 、OH
、OH
D.强酸性溶液:K 、Mg
、Mg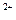 、NO
、NO 、ClO
、ClO
参考答案:A
本题解析:略
本题难度:简单
3、选择题 铝投入下列溶液中有气体生成,其中一定能大量共存的离子组是?(?)
A.NO3-、Cl-、Na+、H+
B.AlO2-、K+、ClO- CO32-
C.Ca2+、Cl-、SO42-、Na+
D.SO42-、Fe2+、OH-、NH4+
参考答案:A
本题解析:根据溶液中离子之间不能结合生成水、气体、沉淀、弱电解质,不能发生氧化还原反应、不能相互促进水解来分析离子在溶液中能大量共存;然后根据溶液中的离子与NaOH溶液反应既有气体放出又有沉淀生成的即为正确答案。
A、因该组离子之间不反应,则离子能大量共存,加入铝有氢气放出,故A正确;
B、加入铝没有气体放出,则该组离子不能大量共存,故B错误;
C、加入铝没有气体放出,则该组离子不能大量共存,故C错误;
D、因该组离子之间OH-与NH4+产生NH3,则离子能不大量共存,故D错误;
故选A。
点评:本题考查离子的共存问题及复分解反应,明确题意中原离子组能共存,当加入碱既有气体又有沉淀生成两个条件来分析解答,熟悉离子的性质及常见离子之间的反应是解答的关键。
本题难度:一般
4、填空题 (10分)现有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl―、Mg2+、Ba2+、CO32―、SO42―。现取3份100 mL该溶液分别进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到标准状况下20.16 L气体;
第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥、得到白色沉淀,再将沉淀经足量盐酸洗涤,发现沉淀部分溶解。
根据上述实验,试回答下列问题:
(1)由第一份进行的实验对Cl-是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”);
(2)由第二份进行的实验得知该混合物中应含有 (填离子符号),其物质的量浓度为 ;
(3)第三份实验中最终得到的沉淀成分为 ;(填化学式)
(4)综合上述实验,你认为以下结论正确的是 。
A.该混合液中一定含NH4+、CO32―、SO42―、K+,可能含Cl―
B.该混合液中一定含NH4+、CO32―、SO42―,可能含K+、Cl―
C.该混合液中一定含NH4+、CO32―、SO42―,可能含Mg2+、K+、Cl―
D.该混合液中一定含NH4+、SO42―,可能含Mg2+、K+、Cl―