微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)(1)在298K时,1molCH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.0 kJ。写出该反应的热化学方程式 。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,并放出515kJ热量,则CH4的物质的量为 。
(2)利用该反应设计一个燃料电池:用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入甲烷和氧气。通入甲烷气体的电极应为 极(填写“正”或“负”),该电极上发生的电极反应式为 。
(3)在下图所示实验装置中总反应的方程式为 ;

如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 ;
若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 。
参考答案: (1)CH4(g)+ 2O2(g)==CO2(g)+ 2H2O(l) △H = -890.0kJ/mol 0.5 (2)负 CH4―8e- + 10OH- ="=" CO32- + 7H2O (3)2CuSO4+2H2O 2Cu+2H2SO4+O2↑石墨电极表面有气泡产生,铁电极上附着一层红色物质,溶液颜色变浅 氧化铜(/碳酸铜) 4g 或6.2g
2Cu+2H2SO4+O2↑石墨电极表面有气泡产生,铁电极上附着一层红色物质,溶液颜色变浅 氧化铜(/碳酸铜) 4g 或6.2g
本题解析:(1)燃烧热就是1mol物质完全燃烧生成稳定氧化物放出的热量。根据题意CH4的燃烧热化学方程式为:CH4(g)+ 2O2(g)==CO2(g)+ 2H2O(l) △H = -890.0kJ/mol,水只能由CH4燃烧生成,18g液态水的物质的量为1mol,根据反应中的计量数关系,生成1mol水需要消耗CH4物质的量为0.5mol,(2)燃料电池中燃料反应的一极是负极,发生的电极反应为CH4―8e- + 10OH- ="=" CO32- + 7H2O.(3)根据电子的移动方向知道石墨做阳极,Fe做阴极,装置就是电解CuSO4溶液,方程式为2CuSO4+2H2O 2Cu+2H2SO4+O2↑,Cu2+在阴极放电,生成铜单质,那么铁电极上附着一层红色物质,CuSO4溶液颜色变浅,Cl-在阳极放电生成Cl2,石墨电极表面有气泡产生。溶液的pH变为1则c(H+)=0.1mol/L,n(H+)=0.1mol/L×1L=0.1mol,则生成的H2SO4物质的量为0.05mol,溶液中减少了Cu和O2,相当于减少的是CuO,根据少什么就加什么,可以加入CuO,质量为0.05mol×80g/mol=4.0g,也可加入碳酸铜,质量为0.05mol×124g/mol=6.2g
2Cu+2H2SO4+O2↑,Cu2+在阴极放电,生成铜单质,那么铁电极上附着一层红色物质,CuSO4溶液颜色变浅,Cl-在阳极放电生成Cl2,石墨电极表面有气泡产生。溶液的pH变为1则c(H+)=0.1mol/L,n(H+)=0.1mol/L×1L=0.1mol,则生成的H2SO4物质的量为0.05mol,溶液中减少了Cu和O2,相当于减少的是CuO,根据少什么就加什么,可以加入CuO,质量为0.05mol×80g/mol=4.0g,也可加入碳酸铜,质量为0.05mol×124g/mol=6.2g
考点:热化学方程式的书写和计算,燃料电池电极反应的书写,电解池的有关反应方程式的书写和计算。
本题难度:一般
2、选择题 按图甲装置进行实验,实验结果如图乙所示.乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量,下列叙述不正确的是( )
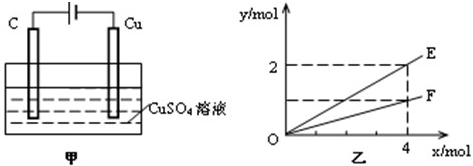
A.E表示反应生成铜的物质的量
B.E表示反应消耗水的物质的量
C.F表示反应生成氧气的物质的量
D.F表示反应生成硫酸的物质的量
参考答案:由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑+2H2O,Cu为阴极,发生Cu2++2e-=Cu,总反应为2CuSO4+2H2O?电解?.?2Cu+O2↑+2H2SO4,结合乙可知,转移4mol电子生成2molE,生成1molF,
A.由电子与物质的物质的量的关系可知E表示反应生成铜的物质的量,故A正确;
B.由总反应可知,Cu与水的物质的量相同,则E表示反应消耗水的物质的量,故B正确;
C.由电子与物质的物质的量的关系可知F表示反应生成氧气的物质的量,故C正确;
D.因硫酸与氧气的物质的量不等,则F不能表示生成硫酸的物质的量,故D错误;
故选D.
本题解析:
本题难度:一般
3、选择题 电解含下列离子的水溶液,若阴极析出相等质量的金属,则消耗的电量最多的是
A.Ag +
B.Cu2+
C.Na+
D.Mg2+
参考答案:B
本题解析:既然是电解含有离子的水溶液,所以不可能析出钠单质、镁单质,因为在阴极氢离子得电子的能力比Na+ 、Mg2+得电子能力强,所以应该看A、B选项,假设都析出mg金属,Ag + 需要消耗的电量为m/108,Cu2+消耗的电量为2m/64,所以消耗电量最多的是Cu2+,故选B。
本题难度:一般
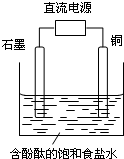
4、选择题 (如014?广州一模)某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )
A.铜电极附近观察到黄绿色气体
B.石墨电极附近溶液呈红色
C.溶液中的Na+向石墨电极移动
D.铜电极上发生还原反应