微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列判断正确的是( )
①稳定性:HI>HBr>HCl?②熔点:SiO2>NaCl>SiI4
③酸性:HClO4>H2SO4>H3PO4?④碱性:NaOH>Mg(OH)2>Al(OH)3
A.只有①
B.只有③
C.②③④
D.①②③④都正确
参考答案:C
本题解析:非金属性越强,氢化物的稳定性越强,①不正确,应该是HI<HBr<HCl,其余都是正确的,答案选C。
本题难度:一般
2、选择题 下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
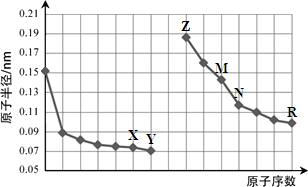
A.Y、R两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
B.简单离子的半径:X > Z > M
C.由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z单质不能从M与R元素构成的盐溶液中置换出单质M
参考答案:BD
本题解析:由关系图可知X是O;Y是F;Z是Na; M是Al;N是Si;R是Cl.A. F的气态氢化物HF的水化物是弱酸,无最高价氧化物的水化物;而Cl的气态氢化物HCl的水化物是强酸,其最高价氧化物的水化物HClO4是强酸。错误。B.O2-、Na+、Al3+是电子层结构相同的离子,核电荷数越大,离子的半径就越小。正确。C.由O与Si两种元素组成的化合物SiO2能与氢氟酸反应SiO2+4HF=SiF4↑+ 2H2O,也能与强碱发生反应SiO2+2NaOH=Na2SiO3+H2O。错误。Na的活动性很强,当将其放入AlCl3溶液使,首先与水发生反应:2Na+2H2O=2NaOH+H2↑;发生反应的产物继续发生反应AlCl3+3NaOH=Al(OH)3↓+3NaCl。因此不能把Al从溶液中置换出来。
本题难度:一般
3、推断题 (10分)A、B、C、D、E都是短周期元素,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是?乙物质的电子式是__________
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是_________ (用元素符号填写)
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是?
(4)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,其中有一种产物是TiC(在火箭和导弹上有重要应用)其反应方程式为?
参考答案:(1)第三周期第IIA族?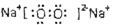 ?
?
(2)O<N<Al<Mg<Na
(3)2 Al + 2OH― + 2H2O = 2AlO2― + 3H2↑
(4)4Al + 3C +3TiO2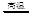 2Al2O3 +3TiC
2Al2O3 +3TiC
本题解析:根据“E是地壳中含量最高的金属元素”确定E为Al;根据“A原子的最外层电子数比次外层电子层多3个”确定A为N;根据“C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。”确定B为O,C为Na,最后根据“A、B、C、D、E都是短周期元素,原子序数逐渐增大”确定D为Mg;据此便可回答相关问题。
本题难度:一般
4、选择题 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是(?)
A.元素周期表含元素最多的族是第ⅢB族
B.元素周期表有18个族
C.第ⅠA族的元素全部是金属元素
D.短周期是第一、二、三、四周期
参考答案:A
本题解析:第ⅢB族中包含锕系与镧系元素,共有32种元素,A项正确;元素周期表中共有18个纵行,16个族,B项错误;第ⅠA族中H为非金属元素,C项错误;短周期包括第一、二、三周期,D项错误。
本题难度:一般
5、选择题 下列说法中不正确的是(?)
A.若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子
B.C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键
C.同周期ⅠA族元素和 ⅦA族元素之间只能形成离子化合物
D.由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键
参考答案:D
本题解析:A项XY3是三角形,为非极性分子,正确;B项C2H5OH分子间存在氢键,正确;C项同周期ⅠA族元素和 ⅦA族元素,排除了H的可能性,则只能形成离子化合物,正确;D项由两种非金属元素组成的化合物分子如H2O2中,则有非极性键,错误。
点评:根据分子的空间结构可以确定分子的极性。
本题难度:简单