微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于Na2CO3和NaHCO3性质的有关叙述正确的是(?)
A.在水中溶解性:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与酸反应的速度:Na2CO3<NaHCO3
D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3
参考答案:C
本题解析:碳酸钠的溶解度大于碳酸氢钠的,A不正确;碳酸钠的热稳定性大于碳酸氢钠的,B不正确;碳酸钠能和CO2的水溶液反应生成碳酸氢钠,D不正确,所以正确的答案选C。
点评:该题是常识性知识的考查,难度不大。主要是考查学生对碳酸氢钠和碳酸钠性质的了解掌握情况,以及灵活运用基础知识解决实际问题的能力,有利于巩固学生的基础性知识。该题学生记住即可,难度不大,不难得分。
本题难度:一般
2、填空题 (6分)已知:
①某银白色固体A,放在空气中可氧化成白色固体B
②将A点燃,火焰呈黄色,生成淡黄色固体C
③A、B、C三种物质都能跟无色液体D反应,生成碱性物质E,其中A跟D反应时还
可生成可燃性气体F,C跟D反应时则生成另一种气体G
④F和G混合后遇火可剧烈反应而发生爆炸,并生成D。
完成下列问题:
(1) C的名称为______________,A与D反应的类型属于?。
(2)写出下列反应的化学方程式
A→B?
C→E?
参考答案:(6分)(1)过氧化钠?置换反应?(各1分)
(2)4Na +O2 =2Na2O?(2分)?2Na2O2 + 2H2O="4NaOH" +O2↑(2分)
本题解析:考查钠及其化合物的性质和相互的转化等。
根据反应的应该现象及有关性质可知,A是钠,B是氧化钠,C是过氧化钠,D是水,E是氢氧化钠,F是氢气,G是氧气。钠与水反应生成氢氧化钠和氢气的反应是置换反应。其中A生成B和C生成E的反应方程式分别是4Na +O2 =2Na2O、2Na2O2 + 2H2O="4NaOH" +O2↑。
本题难度:一般
3、选择题 将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中,点火花点燃,反应结束后,容器温度为150℃、压强为0Pa。将残留物溶于水,无气体逸出。下列叙述正确的是(? )
A.原混合气体中O2和CH4的体积比为2∶1;
B.原混合气体中O2和CH4的体积比为1∶1;
C.残留固体中有Na2CO3和NaOH;
D.残留固体中只有Na2CO3
参考答案:C
本题解析:由题意可知,剩余固体溶于水中,无气体放出,说明过氧化钠反应完全,无剩余;利用方程式叠加法得过氧化钠与甲烷、氧气反应的总方程式为6Na2O2+O2+2CH4→8NaOH+ 2Na2CO3,所以答案选C。
本题难度:一般
4、实验题 在实验室模拟工业生产碳酸钠:一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2,一段时间后,出现沉淀,过滤得到NaHCO3晶体。
(1)该过程的化学方程式:?。
(2)加热NaHCO3得到纯碱制品,实验室可进行此操作的装置是?。
 ?
?
A? B? C? D
(3)得到的纯碱制品含有少量NaHCO3和NaCl,设计实验验证样品中各种组分。试剂和仪器限选用:试管、胶头滴管、过滤装置、Ba(NO3)2溶液、NaOH溶液、AgNO3溶液、澄清石灰水、稀硫酸、稀盐酸、稀硝酸。
步骤一:取少量制品于试管中,加少量蒸馏水,振荡,溶解。往试管中加入??
?振荡,观察?
| 现象:溶液中产生大量白色沉淀;
结论:??。
|
步骤二:将步骤一的浊液过滤,取滤液于试管中B中,加入?,
振荡,观察
| ?
现象:??;
结论:样品中含有NaHCO3。
|
步骤三:将步骤二的浊液过滤,取滤液于试管C中,??
?振荡,观察
| ?
现象:??;
结论:??。
|
?
(4)用碘量法测量自来水中残留的Cl2的浓度:
① 在大锥形瓶中放置过量的KI,加一定量的冰醋酸,准确取水样200mL加入瓶中,迅速塞上瓶塞摇动,水样呈淡黄色,发生反应:Cl2+2I-=2Cl-+ I2。
②加少许淀粉溶液,用cmol/L Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当?,达到滴定终点。
③重复操作3次,平均读数为V mL,则该样品中残留Cl2的浓度:??mg/L(Cl的相对原子质量:35.5)
参考答案:(16分)
(1) NaCl + NH3 + CO2 + H2O = NaHCO3 ↓+ NH4Cl? (2分,没有沉淀符号扣1分)
(2)BC?(2分)
(3)
步骤一:取少量制品于试管中,加入少量蒸馏水,振荡,溶解:往试管中加入
过量的Ba(NO3)2溶液,振荡,观察 (2分)
现象:溶液中产生大量白色沉淀;
结论:试样中含有Na2CO3。(1分)
步骤二:将步骤一的浊液过滤:取滤液于试管B中,加入
适量的NaOH溶液, 振荡,观察(1分)
现象:有少量白色沉淀生成 ;(1分)
结论:试样中含有NaHCO3。
步骤三: 将步骤二的浊液过滤后,取滤液于试管C中,先加入足量的稀硝酸,再加入少许AgNO3溶液,振荡,观察(2分)
?
现象:有少量白色沉淀生成 ;
结论:试样中含有NaCl 。(1分)
?
(8分)检验出Na2CO3得3分;检验出NaHCO3得2分(若用硝酸检验得1分),
检验出NaCl得3分(未加过量硝酸不得分)。三种物质检验不诛连。
(4)②最后一滴溶液滴入,锥形瓶内的液体恰好从蓝色变成无色,且半分钟不变化?(2分)
③ 177.5 cV (即:0.5×c×V×10-3×71×1000/0.2)(2分)
本题解析:(1)氨气易溶于饱和食盐水,且NH3+H2O=NH3?H2O,得到氯化钠、氨水溶液;一水合氨是弱碱,二氧化碳是酸性氧化物,不断通入二氧化碳气体时,NH3?H2O+CO2=NH4HCO3;由于碳酸氢钠的溶解度比氯化钠、碳酸氢铵都小,碳酸氢钠最先达到饱和,则碳酸氢铵与氯化钠容易反应,生成碳酸氢钠晶体和氯化铵溶液,即NH4HCO3+NaCl=NaHCO3↓+NH4Cl;上述几步反应加起来可得:NaCl + NH3 + CO2 + H2O = NaHCO3 ↓+ NH4Cl;(2)碳酸氢钠是固体,加热固体样品应该选择试管或坩埚,故BC正确;A项,属于蒸发装置,加热盐溶液,分离和盐和水,故A错;未了防止冷凝水回流时,导致热的试管底突然遇冷炸裂,试管底应该略低于试管口,故D错;(3)制品是碳酸钠、碳酸氢钠和氯化钠组成的混合物,它们都是可溶性盐,根据实验步骤一、二、三的操作及预期现象和结论综合推断,步骤I加入的试剂是过量或足量Ba(NO3)2溶液,振荡,因为硝酸钡只能与碳酸钠反应,生成碳酸钡沉淀和硝酸钠,可以检验制品中含有碳酸钠,并且除去其中的碳酸钠,防止碳酸钠对碳酸氢钠、氯化钠的检验产生干扰;由于碳酸氢钠与硝酸钡不能反应,但是碳酸氢钠与足量或过量氢氧化钠能发生反应,生成水和碳酸钠,生成物中的碳酸钠与步骤一中加入的过量或足量的硝酸钡反应,滤液中又产生少量的白色沉淀,说明制品中含有少量碳酸氢钠;检验制品中的氯化钠可以用硝酸银溶液检验,但是碳酸钠也能与硝酸银反应,都产生白色沉淀,因此需要除去制品中的碳酸钠,由于步骤二的滤液中含有过量氢氧化钠,氢氧化钠也能与硝酸银反应,产生白色沉淀,对氯化钠的检验造成干扰,则步骤三必须先用过量或足量稀硝酸酸化,中和氢氧化钠之后,再向步骤二的滤液中滴入少量或几滴AgNO3溶液,产生少量的白色沉淀,说明制品中含有氯化钠;(4)实验①中发生的反应为Cl2+2I-=2Cl-+ I2,则锥形瓶内溶液中的碘离子被自来水中的氯气氧化为单质碘;单质碘遇淀粉变蓝,则实验②中发生的反应为I2+2S2O32-=2I-+S4O62-,碘离子遇淀粉不变色,则锥形瓶内溶液的颜色由蓝色变为无色,说以滴定终点的现象为:最后一滴Na2S2O3溶液溶液滴入,锥形瓶内的液体恰好从蓝色变成无色,且半分钟不变化;先根据c?V=n求Na2S2O3溶液中溶质的物质的量,即n(Na2S2O3)=cmol/L×V×10-3L= c×V×10-3mol;由于Na2S2O3是强电解质,完全电离出钠离子和硫代硫酸根离子,且n(S2O32-)= n(Na2S2O3)= c×V×10-3mol;由于I2+2S2O32-=2I-+S4O62-中I2与S2O32-的物质的量之比等于系数之比,则单质的物质的量为c×V×10-3mol×1/2;由于Cl2+2I-=2Cl-+ I2中Cl2与I2的物质的量之比等于系数之比,则自来水中氯气的物质的量为c×V×10-3mol×1/2×1/1; 氯气的相对分子质量为71,然后根据n?M=m求自来水中所含氯气的质量,则m(Cl2)= c×V×10-3mol×1/2×1/1×71g/mol;200mL=0.2L,最后根据n/V=c求自来水中所含氯气的浓度,则c(Cl2)= c×V×10-3mol×1/2×1/1×71g/mol÷0.2L=0.5×c×V×10-3×71/0.2g/L=0.5×c×V×10-3×71×1000/0.2mg/L= 177.5 cV mg/L,因为1g=1000mg。
本题难度:困难
5、填空题 我国濒临海域的省份,能够充分利用海水制得多种化工产品。下图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中E是一种化肥,N是一种常见的金属单质。
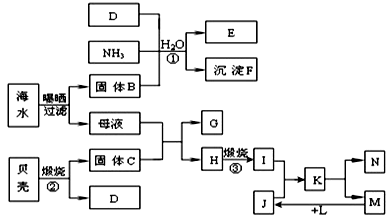
结合上述工艺流程回答下列问题:
(1)物质G和L的化学式分别为?和???;固体B是生活中的一种必需品,主要用作 ??
(2)上述工艺流程中可以循环使用的物质的化学式为??
(3)反应①的化学方程式为?;在反应①中必须先通入NH3,而后通入D,其原因是?
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为?
(5)由K溶液经如何处理才能制得N??
参考答案:(1)CaCl2? H2?调味品
(2)CO2
(3)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl? NH3在溶液中的溶解度大,利于吸收CO2,使其转化为(NH4)2CO3
(4)2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(5)MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得MgCl2晶体,熔融电解可制取金属镁
本题解析:贝克高温煅烧得到CaO和CO2。海水曝晒得到NaCl固体和含有CaCl2、MgCl2的母液。NaCl、CO2、NH3在水溶液中发生反应:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl产生小苏打沉淀。滤液中含有NH4Cl。将CaO加入含有MgCl2溶液中,发生反应:CaO+ MgCl2+H2O=Mg(OH)2↓+ CaCl2. 将过滤出来,洗涤干净,然后灼烧Mg(OH)2,发生分解反应Mg(OH)2 MgO+ H2O。用HCl溶解MgO,得到纯净的MgCl2溶液。将该溶液蒸发、浓缩,冷却结晶得到MgCl2・6H2O.将MgCl2・6H2O加热,在HCl的气氛中加热蒸发得到无水MgCl2。然后电解熔融的Mg Cl2即得到Mg和Cl2.(1)物质G和L的分别为CaCl2和H2。固体NaCl是生活中的一种必需品,主要用作调味品。(2)上述工艺流程中可以循环使用的物质的化学式为CO2。(3)反应①的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。在反应①中必须先通入NH3,而后通入CO2,是因为NH3在溶液中的溶解度大,利于吸收CO2,使其转化为(NH4)2CO3。(4)工业上利用NaHCO3可制得另一种化工产品Na2CO3,该反应的化学方程式为2NaHCO3
MgO+ H2O。用HCl溶解MgO,得到纯净的MgCl2溶液。将该溶液蒸发、浓缩,冷却结晶得到MgCl2・6H2O.将MgCl2・6H2O加热,在HCl的气氛中加热蒸发得到无水MgCl2。然后电解熔融的Mg Cl2即得到Mg和Cl2.(1)物质G和L的分别为CaCl2和H2。固体NaCl是生活中的一种必需品,主要用作调味品。(2)上述工艺流程中可以循环使用的物质的化学式为CO2。(3)反应①的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。在反应①中必须先通入NH3,而后通入CO2,是因为NH3在溶液中的溶解度大,利于吸收CO2,使其转化为(NH4)2CO3。(4)工业上利用NaHCO3可制得另一种化工产品Na2CO3,该反应的化学方程式为2NaHCO3 Na2CO3+ CO2↑+H2O。(5)MgCl2是强酸弱碱盐,加热发生水解反应得到Mg(OH) 2和HCl,HCl容易挥发,导致得到的固体为Mg(OH) 2。为了抑制其水解,所以必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,然后电解熔融氯化镁,可制取金属镁。
Na2CO3+ CO2↑+H2O。(5)MgCl2是强酸弱碱盐,加热发生水解反应得到Mg(OH) 2和HCl,HCl容易挥发,导致得到的固体为Mg(OH) 2。为了抑制其水解,所以必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,然后电解熔融氯化镁,可制取金属镁。
本题难度:一般