��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���з��ӵĿռ乹�Ϳ���sp2�ӻ���������͵���______������ţ���CH4?��CH2=CH2��C6H6?��CH��CH?��NH3?��BF3��
�ο��𰸣���CH4?������̼ԭ���ӻ������Ϊ4�����Բ�ȡsp3�ӻ����ʴ���
?��CH2=CH2������ÿ��̼ԭ���ӻ������Ϊ3�����Բ�ȡsp2�ӻ�������ȷ��
��C6H6������̼ԭ���ӻ������Ϊ3�����Բ�ȡsp2�ӻ�������ȷ��
?��CH��CH������ÿ��̼ԭ���ӻ������Ϊ2�����Բ�ȡsp�ӻ����ʴ���
��NH3�����е�ԭ���ӻ������Ϊ4�����Բ�ȡsp3�ӻ����ʴ���
��BF3��������ԭ���ӻ������Ϊ3�����Բ�ȡsp2�ӻ�������ȷ��
���������
�����Ѷȣ�һ��
2������� ��A�����������(Se)����(Te)��Ԫ���ڻ������г����ֳ���������̬������A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺ ?
?��1��S���ʵij�����ʽΪS8���价״�ṹ����ͼ��ʾ��Sԭ�Ӳ��õĹ���ӻ���ʽ��_____��
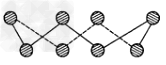
��2��ԭ�ӵĵ�һ��������ָ��̬�����Ի�̬ԭ��ʧȥһ������ת��Ϊ��̬��̬����������Ҫ�����������O��S��Seԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ_______��
��3��Seԭ������Ϊ____�������M����ӵ��Ų�ʽΪ____��
��4��H2Se�����Ա�H2S___���ǿ��������������̬SeO3���ӵ����幹��Ϊ____��
SO32-���ӵ����幹��Ϊ______��
��5��H2SeO3��K1��K2�ֱ�Ϊ2.7��10-3��2.5��10-8��H2SeO4��һ��������ȫ���룬K2Ϊ
1.2��10-2������ݽṹ�����ʵĹ�ϵ���ͣ�
��H2SeO4��H2SeO3��һ������̶ȴ��ڵڶ��������ԭ��______��
��H2SeO4��H2SeO3����ǿ��ԭ��____________��
��6��ZnS��ӫ���塢�����ϡ�Ϳ�ϡ����ϵ���ҵ��Ӧ�ù㷺������ZnS����ṹ����ͼ��ʾ���侧���߳�Ϊ540.0?pm���ܶ�Ϊ_________g��cm-3����ʽ�����㣩��aλ��S2-������bλ��Zn2+����֮��ľ���Ϊ_____pm����ʽ��ʾ����

�ο��𰸣���1��sp3
��2��O��S��Se
��3��34��3s23p63d10
��4��ǿ��ƽ�������Σ�������
��5���ٵ�һ����������ɵĸ����ӽ��ѽ�һ�������������ɵ�������
��H2SeO4��H2SeO3�ɱ�ʾΪ(HO)2SeO��(HO)2SeO2��H2SeO3�е�SeΪ+4�ۣ���H2SeO4�е�SeΪ+6�ۣ������Ը��ߣ�����Se-O-H�е�O�ĵ��Ӹ���Seƫ�ƣ�Խ�����H+
��6��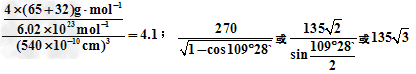
���������
�����Ѷȣ�һ��
3������� Al��Si��Ge(��)��As(��)��Ԫ�����ڱ������ͷǽ�������λ���ϣ�����(As)�뵪ͬ���壬�䵥�ʺͻ������ڽ���ҵ�����ӹ�ҵ��ʯ�ͻ����ȷ���Ӧ�ù㷺����ش��������⣺
(1)As�ļ۵����Ų�ʽΪ____________��
(2)AlCl3�ǻ��������еij��ô������۵�Ϊ192.6�棬����״̬�Զ�����Al2Cl6��ʽ���ڣ�Al2Cl6�л�ѧ��������____________��
(3)���ߵ��Ⱦ�Ե������������(AlN)�ھ�Ե�����е�Ӧ�ù㷺��AlN��������ʯ���ƣ�ÿ��Alԭ����____��Nԭ����������ͬһ��Alԭ��������Nԭ�ӹ��ɵĿռ乹��Ϊ_________�����Ĵ��������У�
AlN����____���塣
(4)Si��Cͬ���壬Si��C��O�ɼ��������

��SiO2�У���ԭ�ӹ���ӻ���ʽΪ________��1mol CO2�к��Цм���ĿΪ______________��������̼���۷е�Զ���ڶ��������ԭ����____________��
(5)SiCl4��Һ����������������ԭ��Si����3d�������ͬH2O(Һ)��λ������ˮ�⣬�ڳ�ʪ�Ŀ����з��̣����û�ѧ����ʽ��ʾ��ԭ��_____________________��
�ο��𰸣�(1)4s24p3
(2)���ۼ�����Ҽ�������λ��
(3)4���������壻ԭ��
(4)sp3��1.204��1024��������̼�Ƿ��Ӿ��壬������������ԭ�Ӿ���
(5)SiCl4+3H2O=H2SiO3��+4HCl��
���������
�����Ѷȣ�һ��
4������� ��ĵ��ʺͻ������ڹ�ҵ������Ҫ��Ӧ�á�
(1)������Ļ����ṹ��Ԫ��������ԭ����ɵ�����ʮ���壬���к���20���ȱ������ε����һ����Ŀ�Ķ��ǣ�ÿ�����Ǹ���һ����ԭ�ӡ���ͼ��ʾ������Ծ�����Ļ����ṹ��Ԫ�ش��������⣺
��B-B�������Ϊ_________��
��������ԭ������________����B-B����________����
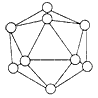
(2)B2O3��C3O2��Ϊ�ȵ����壬��д��C3O2�Ľṹʽ___________��
(3)����[B(OH)3]��һ�ֽ�����һԪ�ᣬ�ۿ�ҽԺ����������������ʵ���в�С�ı�����Һ���˺���ϴ�˿ں��Ϳ�����������ᣬд������ĵ��뷽��ʽ____________������������У�Bԭ����3���ǻ��������侧�������ʯī���ƵIJ�״�ṹ���������Bԭ���ӻ���������ͼ�ͬ����Ӽ����Ҫ�������ֱ���
_______��
A��sp�����»��� B��sp2�����»��� C��sp2����� D��sp3�����
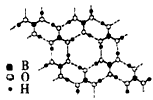
(4)��30�����£�����������ӵ�������������ƵĻ����Һ�У�����һ����ɫ����X����ɷ���֤ʵ���þ�����������ΪNa 14. 72%��B 7.03%�� H 5.12 %����X�Ļ�ѧʽΪ________��
�ο��𰸣�(1)��60�㣻��12��30
(2)O=C=C=C=O
(3)B(OH)3+H2O [B(OH)4]-+H+��C
[B(OH)4]-+H+��C
(4)NaBH8O7��NaBH2O4��3H2O
���������
�����Ѷȣ�һ��
5������� ����Ni����һ����Ҫ�Ľ������ڲ��Ͽ�ѧ�������й㷺Ӧ�ã�
��1��Ni��Ԫ�����ڱ��е�λ����______��
��2�������γ������磺Ni��CO��4��[Ni��NH3��6]2+?�ȣ�д��һ��������CO��Ϊ�ȵ������������______������NH3��Nԭ�ӵ��ӻ�����Ϊ______�����������������ԭ����______����[Ni��NH3��6]2+?Ϊ�������幹�ͣ���[Ni��CO��2��NH3��4]2+�Ľṹ��______�֣�
��3�����������ϼ�Ϊ+2��+3����ˮ��Һ��ͨ��ֻ��+2?�����ӵ���ʽ���ڣ�+3�۵������Ӿ��к�ǿ�������ԣ���ˮ�л���ˮ���������Ѹ�ٷ���������ԭ��Ӧ��Ni3+�ĵ����Ų�ʽΪ______��NiO��OH������Ũ����Ļ�ѧ����ʽΪ______��
��4�������磨
La����ɵ�һ�ֺϽ�LaNix�ǽϺõĴ�����ϣ��ܿ��ٿ���ش洢���ͷ�H2��LaNix�ľ�����ͼ���䴢��ԭ��Ϊ�������Ͻ�����H2��H2����Ϊԭ�ӣ�H�����������γ�LaNixH6��LaNixH6�У�x=______��������������Ͻ���ĭ������������������Һ��ɵ������ر���������ԭ���ӣ���Ӧԭ��Ϊ��
LaNixHy+y?NiO��OH��?LaNix+y?NiO+y?H2O��д����ŵ�ʱ�����ĵ缫��Ӧ����ʽ______��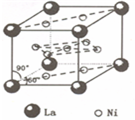
�ο��𰸣���1��Ni��ԭ������Ϊ28��λ�����ڱ��������ڵڢ��壬�ʴ�Ϊ���������ڣ��ڢ��壻
��2��CO�ĵ�����Ϊ14������2��ԭ�ӣ����ĵȵ������е�CN-��C22-��NH3��Nԭ���γ�4���ļ���Ϊ�ӻ�sp3��������Һ����Һ��ʱ���մ������ȣ��������������[Ni��CO��2��NH3��4]2+�Ľṹ�У�CO��λ��ƽ������ں��������λ�ã�
�ʴ�Ϊ��CN-��C22-��sp3��Һ̬������ʱ�����մ������ȣ�2��
��3��Ni3+�ĵ����Ų�ʽΪ��[Ar]3d7��1s22s22p63s23p63d7��NiO��OH�����������ԣ������ᷢ��������ԭ��Ӧ����ѧ����ʽΪ2NiO��OH��+6HCl��Ũ��=2NiCl2+Cl2��+4H2O��
�ʴ�Ϊ��[Ar]3d7��1s22s22p63s23p63d7��2NiO��OH��+6HCl��Ũ��=2NiCl2+Cl2��+4H2O��
��4���ɾ����ṹ��֪��Niλ�ھ��������ϣ�����10��Ni����ƽ������Ni�ĸ���Ϊ10��12=5��ԭ��ظ�������������Ӧ����ԭ����ܷ�Ӧʽ��֪��������ӦʽΪLaNi5H6+6OH--6e-�TLaNi5+6H2O��
�ʴ�Ϊ��5��?LaNi5H6+6OH--6e-�TLaNi5+6H2O��
���������
�����Ѷȣ�һ��