微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将Mg、Cu组成的2.64?g混合物投入适量稀硝酸中恰好反应,固体完全溶解时收集到的还原产物NO气体0.896?L(标准状况),向反应后的溶液中加入2?mol/L的NaOH溶液60?mL时金属离子恰好沉淀完全.则形成沉淀质量为
[? ]
A.4.32?g?
B.4.68?g
C.5.36?g?
D.6.38?g
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列反应:8NH3+3Cl2=6NH4Cl+N2被氧化的氨气和未被氧化的氨气的质量比为
A.3:1
B.1:3
C.1:1
D.3:8
参考答案:B
本题解析:分析:在8NH3+3Cl2=6NH4Cl+N2反应中,氯气中氯元素化合价由0价降低为-1价,氯元素被还原,氨气中氮元素化合价由-3价升高为0价,氮元素被氧化,根据产物中氮元素化合价可知,参加反应的氨气中有 的起还原剂作用,
的起还原剂作用, 的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.
的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.
解答:在8NH3+3Cl2=6NH4Cl+N2反应中,氯气中氯元素化合价由0价降低为-1价,氯元素被还原,氨气中氮元素化合价由-3价升高为0价,氮元素被氧化,
根据产物中氮元素化合价可知,参加反应的氨气中有 的起还原剂作用,被氧化,
的起还原剂作用,被氧化, 的氨气中氮元素化合价不变,仅作为反应物参加反应.
的氨气中氮元素化合价不变,仅作为反应物参加反应.
所以被氧化的氨气和未被氧化的氨气的质量比为 :
: =1:3.
=1:3.
故选:B.
点评:本题考查氧化还原反应概念及计算,难度不大,关键根据化合价变化判断参加反应的氨气中有 的起还原剂作用.
的起还原剂作用.
本题难度:困难
3、选择题 往含0.2mol?NaOH和0.1mol?Ca(OH)2的溶液中持续稳定地通入CO2气体,当通入气体的体积为6.72L(标准状况下)时立即停止,则在这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)?
[? ]
A.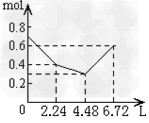
B.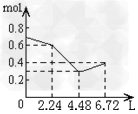
C.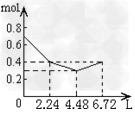
D.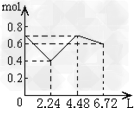
参考答案:C
本题解析:
本题难度:一般
4、计算题 二氧化硫(SO2)是形成酸雨的因素之一,它的含量是空气质量监测的一个重要指标。某兴趣小组同学取到热电厂(燃煤电厂)附近的刚下的雨水进行实验。①测得该雨水样品的pH为4.73;②向雨水样品中滴加BaCl2溶液,有白色沉淀生成;③每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
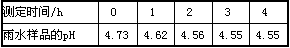
根据以上信息,回答下列问题:
(1)分析上述数据变化,你认为形成这一变化的原因是__________________________(用化学方程式表示);
(2)常温下,取该雨水与一定量的蒸馏水相混合,则pH将____(填“变大”、“变小”或“不变”);
(3)兴趣小组同学取3小时后这种雨水VL,加入1.00 mol/L的Ba(OH)2溶液至不再产生沉淀时,恰好消耗20.0mLBa(OH)2溶液。请你计算:
①生成沉淀物的质量是多少?
②该VL雨水中溶解SO2的体积(标准状况)。
参考答案:(1)2H2SO3+O2=2H2SO4
(2)变大
(3)①4.66g;②0.448L
本题解析:
本题难度:一般
5、选择题 已知硫铁矿在沸腾 炉中煅烧时通入的气体原料是空气,且空气中N2的体积分数为0.8,O2的体积分数为0.2,则从沸腾炉排出的气体中SO2的体积分数可能是
[? ]
A.0.10?
B.0.12?
C.0.16?
D.0.20
参考答案:AB
本题解析:
本题难度:一般