微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在IIA族中,Be是惟一可以生成含氧酸根(铍酸根离子:BeO22-)的元素,与铍的性质相似的短周期元素是?
A.Na
B.Mg
C.Al
D.Si
参考答案:C
本题解析:试题分析:金属铝也能形成含氧酸根Al(OH)4-,所以答案选C。
考点:考查元素周期律的应用
点评:本题属于基础性试题的考查,难度不大。主要是考查学生对常见元素及其化合物性质的熟练掌握程度以及灵活运用知识解决实际问题的能力。
本题难度:一般
2、选择题 下列有关元素周期表的叙述错误的是
? [? ]
A.原子半径最小的是氢
B.所含元素种类最多的族是第VIII族
C.金属元素的种类多于非金属元素
D.第n周期第n主族的元素不一定为金属
参考答案:B
本题解析:
本题难度:简单
3、选择题 下列元素中,原子半径最大的是( )
A.锂
B.钠
C.钾
D.铷
参考答案:Li、Na、K、Rb是同一主族的元素,电子层数依次增多,原子半径逐渐增大.
故选D.
本题解析:
本题难度:简单
4、简答题 下表列出了①~⑥六种元素在周期表中的位置:
?族
周期 | | 0
1
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
①
②
3
③
④
⑤
⑥
⑦
⑧
|
请按要求回答下列问题.
(1)元素⑥的氢化物的电子式是______.
(2)这六种元素中,位于第三周期且原子半径最小的是(填元素符号)______.
(3)这六种元素中,属于两性氧化物的是(填化学式)______.⑤⑥⑦⑧四种元素的最高价氧化物的水化物中,酸性强弱顺序为______.
(4)写出实验室制取元素②的氢化物的化学方程式______.
(5)在盛有水的小烧杯中加入元素③的单质,反应后向溶液中再加入元素④的单质,此时发生反应的离子方程式为______.
参考答案:由元素在周期表中的位置可知,①为C元素、②为N元素、③为Na元素、④为Al元素、⑤为Si元素、⑥为P元素、⑦为S元素、⑧为Cl元素,
(1)PH3中P原子与H原子之间形成1对共用电子对,电子式为
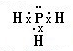
,故答案为:
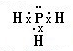
;
(2)同周期自左而右原子半径减小,故原子半径最小的元素是Cl,故答案为:Cl;
(3)Al(OH)3是两性氢氧化物,同周期自左而右非金属性增强,故非金属性Si<P<S<Cl,非金属性越强,最高价氧化物的水化物酸性越强,故酸性HClO4>H2SO4>H3PO4>H2SiO3,
故答案为:Al(OH)3;HClO4>H2SO4>H3PO4>H2SiO3;
(4)实验室利用氯化铵与氢氧化钙加热制备氨气,反应方程式为2NH4Cl+Ca(OH)2?△?.?CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2?△?.?CaCl2+2NH3↑+2H2O;
(5)钠与水反应生成氢氧化钠,铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为2A1+2OH-+2H2O=2A1O2-+3H2↑,
故答案为:2A1+2OH-+2H2O=2A1O2-+3H2↑.
本题解析:
本题难度:一般
5、选择题 锶(Sr)是元素周期表中第五周期IIA族的元素,下列关于锶及其化合物的说法中不正确的是( )
A.锶能与冷水剧烈反应
B.锶的失电子能力比钙强
C.Sr(OH)2的碱性比Ca(OH)2弱
D.氧化锶是碱性氧化物
参考答案:A.Ca、Ba等金属能与是剧烈反应,Sr与Ca、Ba等元素位于同一主族,且金属性更强,能与冷水发生剧烈反应,故A正确;
B.同主族元素从上到下元素的金属性逐渐增强,故B正确;
C.同主族元素从上到下元素的金属性逐渐增强,对应的最高价氧化物的水化物的碱性逐渐增强,故C错误;
D.Sr具有较强的金属性,对应的氧化物为碱性氧化物,故D正确.
故选C.
本题解析:
本题难度:一般