��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
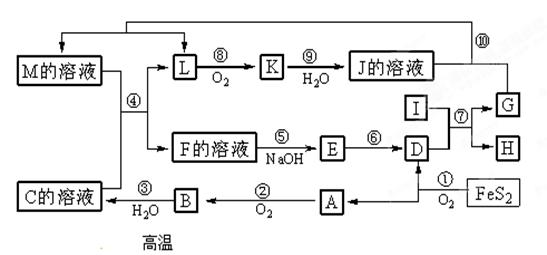
1������� ( 8��)��ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г��������У�I���ɵ�������Ԫ����ɵĵ������۵���ߵĽ����� K��һ�ֺ���ɫ���塣
 ����ʾ��4FeS2+11O2
����ʾ��4FeS2+11O2 2Fe2O3+8SO2��
2Fe2O3+8SO2��
����д���пհף�
�� �����ڱ��У���ɵ���G��Ԫ��λ�ڵ�___? _?_����_________�塣
�� �ڷ�Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ___________________��
�� �ڢڡ��ۡ��ޡ����м����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ����___________������ţ�
�� ��Ӧ�ܵ����ӷ���ʽ�ǣ�______________________________________________��
�� ��������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч��ˮ��K2FeO4��������أ���ͬʱ������KNO2��H2O���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�__________________________________��
�ο��𰸣���1���ģ���4������?��2��1:2?��3����?
��4��3Fe2����NO3�� ��4H�� = 3Fe3����NO����2H2O?
��5��Fe2O3��3KNO3��4KOH =2K2FeO4��3KNO2��2H2O
�����������K��һ�ֺ���ɫ���壬��֪K��NO2,L��NO����I���ɵ�������Ԫ����ɵĵ������۵���ߵĽ�������֪I��Al���ָ���4FeS2+11O2 2Fe2O3+8SO2�����Ƶ�D��Fe2O3,A����SO2�� B��SO3�� C��H2SO3��I��D�������ȷ�Ӧ����Fe��Al2O3�����ݹ�ǰ��ķ�Ӧ�����Ƶ�G��Fe��H��Al2O3����M����ҺΪFe(NO3)3��Һ,M��C��Ӧ����NO��Fe2(SO4)3,�ɵ�F��Fe2(SO4)3��E��Fe(OH)3����ˣ�1������ɵ���Fe��Ԫ�ؾ�λ�ڵ������ڢ��塣��2���ⷴӦ��Fe��Al2O3�������ȷ�Ӧ��������Al2O3�뻹ԭ��Fe�����ʵ���֮��Ϊ1:2����3�������SO2��O2��Ӧ����SO3���ǻ��Ϸ�Ӧ��ͬʱҲ��������ԭ��Ӧ������SO3��ˮ��Ӧ����H2SO3�����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ�����Ƿֽ�Fe(OH)3����Fe2O3���ڷֽ�
2Fe2O3+8SO2�����Ƶ�D��Fe2O3,A����SO2�� B��SO3�� C��H2SO3��I��D�������ȷ�Ӧ����Fe��Al2O3�����ݹ�ǰ��ķ�Ӧ�����Ƶ�G��Fe��H��Al2O3����M����ҺΪFe(NO3)3��Һ,M��C��Ӧ����NO��Fe2(SO4)3,�ɵ�F��Fe2(SO4)3��E��Fe(OH)3����ˣ�1������ɵ���Fe��Ԫ�ؾ�λ�ڵ������ڢ��塣��2���ⷴӦ��Fe��Al2O3�������ȷ�Ӧ��������Al2O3�뻹ԭ��Fe�����ʵ���֮��Ϊ1:2����3�������SO2��O2��Ӧ����SO3���ǻ��Ϸ�Ӧ��ͬʱҲ��������ԭ��Ӧ������SO3��ˮ��Ӧ����H2SO3�����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ�����Ƿֽ�Fe(OH)3����Fe2O3���ڷֽ�
����NO2��ˮ�ķ�Ӧ�в����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ�����Ը���Ĵ��Ǣۡ���4���ⷴӦ�ܵ����ӷ���ʽ�ǣ�3Fe2����NO3�� ��4H�� = 3Fe3����NO����2H2O����5���⣬�����������������K2FeO4������������ԭ��Ӧ��ʧ�����غ㣬�ɵøû�ѧ��Ӧ�Ļ�ѧ��Ӧ����ʽ�ǣ�Fe2O3��3KNO3��4KOH =2K2FeO4��3KNO2��2H2O
�����������ۺ��˵�������������ˮ��������֪ʶ�����ƶϹ��̲��Ǻܸ��ӣ���Ҫѧ����סһЩ�����Ļ�ѧ��Ӧ������������ԭ��Ӧ����ʽ����ƽ���Ƶ���
�����Ѷȣ�����
2������� ����X��Y��Z���ֳ���������Ԫ�أ�x��ԭ�ӽṹʾ��ͼ��ͼ��Y��zΪͬ���ڽ���Ԫ�أ�Y��Z������������Ӧˮ������Է�Ӧ�����κ�ˮ���ش��������⣺
��1����֪Y2?X2Ϊdz��ɫ�������ʣ����������Ӹ�����Ϊ______�����к��еĻ�ѧ��������______��
��2��������Z�ı�Ƭ�ھƾ����ϼ������ۻ����۲쵽������______�������������ԭ����______��
��3��Y��Z����������Ӧ��ˮ�����Ϸ�Ӧ�����κ�ˮ�����ӷ���ʽΪ______��
��4������3���������ﻹ�ɱ�ʾΪYZ��OH��4����YZ��OH��4�����HC1��Һ��Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�X��Y��Z���ֳ���������Ԫ�أ�����X��ԭ�ӽṹʾ��ͼ��֪a=2����XΪOԪ�أ���ϣ�1��Y2?X2Ϊdz��ɫ�������ʣ���֪YΪNaԪ�أ�Y��ZΪͬ���ڽ���Ԫ�أ����ߵ�����������Ӧˮ������Է�Ӧ�����κ�ˮ��Ϊ��������������������Ӧ����ZΪAlԪ�أ�
��1��Na2O2������������������ӹ��ɵ����ӻ�������������Ӹ�����Ϊ1��2��������������������֮���γ����Ӽ�����������������ԭ��֮���γɷǼ��Լ����ʴ�Ϊ��1��2�����Ӽ����Ǽ��Լ���
��2��������Al�ı�Ƭ�ھƾ����ϼ������ۻ������ڷ�Ӧ���������������������۵�����ߣ�������Ĥ��ס�����ڻ��ɵ�С�����£��ʴ�Ϊ���ڻ��ɵ�С�����£����������۵�����ߣ�
��3����������������������Ӧ����ƫ��������ˮ����Ӧ���ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O���ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��4��NaAl��OH��4�����HC1��Һ��Ӧ�����Ȼ������Ȼ�����ˮ����Ӧ���ӷ���ʽΪ��Al��OH��4-+4H+=Al3++4H2O���ʴ�Ϊ��Al��OH��4-+4H+=Al3++4H2O��
���������
�����Ѷȣ�һ��
3������� ��ͼ1��A��J���ճ������г��������ֽ����������ֽ�����NaOH���ԭ��أ�A��������F�����������壬�����������µ�ת����ϵ�����ֲ��P������ȥ����

��ش��������⣺
��1��д��ԭ��صĸ�����Ӧ����ʽ______��
��2������ʱpH=12��C��Һ�У����ʵ������������ʵ�������Ũ��֮��Ϊ______��д������ʽ������ͬ�����£���Ũ�ȵ�C��Һ��CH3COONa��Һ�У�C����������CH3COO-Ũ�ȵĴ�С��ϵ��ǰ��______���ߣ��á���������������=����ʾ����
��3������A���Ȼ���е�ϵͣ������������ܷ������������Ȼ���������A��______��ԭ����______��
��4��д���ڵĻ�ѧ����ʽ______��
��5��д��A��J��Ӧ�Ļ�ѧ����ʽ______��
��6����AԪ�ص�ij��X������ˮ����X����ɫ��Ӧʱ�����ܲ����۲�������ɫ����
��ˮ��Һ��NaHCO3��Һ��ϣ���Ӧ�����ӷ���ʽΪ��______
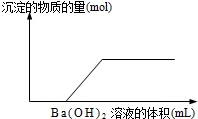
��500mLX����Һ��Ba��OH��2��Ӧ���ɳ��������������Ba��OH��2���ʵ����Ĺ�ϵ��ͼ2����ش�X���������Ϊ______������Һ�����ʵ���Ũ��Ϊ______mol/L��
�ο��𰸣���1������H��AΪ��ҵұ����������A��JΪ���ȷ�Ӧ��Ϊ�ƶ����ͻ�ƿڣ����ο�֪C��E��H��A��J��ת������ѧ��ѧ�г�����Ӧ��ΪAlO2-��Al��OH��3��Al2O3��Al��Fe֮���ת������ԭ��������������������������������ҺΪNaOH��������֪��AΪAl��CΪNaAlO��EΪAl��OH��3��HΪAl2O3��JΪFe��MΪFeS��ԭ����У�Al���������������ڼ�����Һ������AlO2-���缫��ӦʽΪ��Al+4OH--3e-=AlO2-+2H2O���ʴ�Ϊ��Al+4OH--3e-=AlO2-+2H2O��
��2����ҺCΪNaAlO2��������Һ�ʵ����ԣ���c��AlO2-��+c��OH-��=c��Na+��+c��H+����֪��c��Na+��-c��AlO2-��=c��OH-��-c��H+��=10-2-10-12?mol/L���ʴ�Ϊ��10-2-10-12?mol/L��c��OH-��-c��H+����?
��3������A���Ȼ���ΪAlCl3��Ϊ���ۻ�����������״̬�²����磬�ʴ�Ϊ������ΪA���Ȼ����۷е�ͣ��ݴ��ж����ľ���Ϊ���Ӿ��壬������̬ʱ�����룬���ܱ���⣻
��4��ԭ�����������H2����DΪH2����GΪ�⻯���G��I��K��ת����֪���⻯���д��ڱ�۷ǽ���Ԫ�أ�ӦΪNԪ�أ���GΪNH3��IΪNO��KΪNO2��LΪHNO3����Ӧ��Ϊ��ҵ�ϳɰ�����Ҫ��Ӧ����ӦΪ��4NH3+5O2?����.��?4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2?����.��?4NO+6H2O?
��5����ӦA��JΪ���ȷ�Ӧ����ӦΪ��Fe2O3+2Al?����?.?2Fe+Al2O3?�ʴ�Ϊ��Fe2O3+2Al?����?.?2Fe+Al2O3?
��6����AlCl3ˮ��Һ��NaHCO3��Һ��Ӧ��ٽ���ˮ�⣬��ӦΪAl3++3HCO3-=Al��OH��3��+3CO2�����÷�ӦΪ��ĭ������ķ�Ӧԭ�����ʴ�Ϊ��Al3++3HCO3-=Al��OH��3��+3CO2����
?�ں�AԪ�ص�ij��X������ˮ����X����ɫ��Ӧʱ�����ܲ����۲�������ɫ��˵�����к�����Ԫ�غͼ�Ԫ�أ�Ϊ�������׳�Ϊ���������
���ݷ�Ӧ���㣺
Ba2++SO42-�TBaSO4
? 1mol? 233g
? n? 233g
��n=1mol������SO42-���ӵ��غ��֪500mLKAl��SO4��2����Һ�к������ʵ����ʵ���Ϊ0.5mol��
��Ũ��Ϊ��0.5mol0.5L=1mol/L���ʴ�Ϊ�����������1mol/L��
���������
�����Ѷȣ�һ��
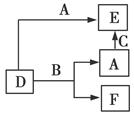
4��ѡ���� A��B��C�ֱ���Ԫ�ؼס��ҡ����ĵ��ʣ����Ƕ��dz����Ľ�����ǽ�����D��E��F�dz��������������������ͼ��ʾת����ϵ��������˵������ȷ����(����)
A��D��E��һ�������м�Ԫ��
B������B�϶���������
C��A��B��C��һ����һ������Ԫ�صĵ���
D����A�Ƿǽ�������Bһ��Ϊ����
�ο��𰸣�B
���������A�Ǽĵ��ʣ�����ͼʾ��E�бغ���Ԫ�أ�B����Ԫ�ص��ʣ���D��Ӧ����A���÷�Ӧ���û���Ӧ������D�бغ���Ԫ�أ�A����ȷ��B�D���������B���ʷ�Ӧ��һ��B�ǻ�ԭ��������C�A��C���ʷ�Ӧ����������E�����Ա���һ������������ȷ��D���A�Ƿǽ�������D��B�ķ�Ӧһ����������ˮ���Ƽ���û�����D����ȷ��
�㲦�����⿼��Ԫ�ػ�����֮���ת���������ƶϡ��Ѷ��еȡ�
�����Ѷȣ�һ��
5��ѡ���� �������ᡢ̼���ơ����ᡢ�Ȼ�ͭ���Ȼ����е�һ�ֻ��ֻ����γɵ�ϡ��Һ�У���������������Һ�����������������������������Һ����Ĺ�ϵ��ͼ��ʾ�������й��ڸ���Һ�����ʵ��ж���ȷ���ǣ�������
A�����ܺ����Ȼ���
B���϶�û��ϡ����
C���϶������Ȼ�ͭ
D�����ܺ���������