微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某元素R的二价阴离子核外共有a个电子,核内有b个中子,则R原子的符号应表示为:?。
参考答案:(a-2+b)(a-2)R2-
本题解析:元素R的二价阴离子核外共有a个电子,则R的质子数=a-2。又因为质子数+中子数=质量数,所以质量数=a-2+b,则该原子符号可表示为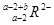 。
。
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。重点考查学生对原子组成以及组成微粒之间数量关系的熟悉了解程度,有利于培养学生的逻辑推理能力和发散思维能力。明确离子的核外电子数与质子数的关系是答题的关键。
本题难度:一般
2、选择题 下列观点正确的是
A.某单质固体能导电,该单质一定是金属
B.某化合物的水溶液能导电,该化合物一定是电解质
C.酸与醇的反应不一定是酯化反应
D.某纯净物常温常压下为气体,则组成该物质的微粒一定含共价键
参考答案:C
本题解析:分析:A.石墨能导电;
B.凡是在水溶液或熔融状态下能导电的化合物叫电解质;
C.氢卤酸也是酸;
D.该气体可能为稀有气体.
解答:A.石墨能导电,是碳的单质,不是金属,故A错误;
B.水溶液能导电不一定是电解质,如氨水是NH3的水溶液能导电,但NH3是非电解质,故B错误;
C.醇与氢卤酸反应,生成卤代烃和水,故C正确;
D.稀有气体是单原子分子,无化学键,故D错误.
故选C.
点评:本题考查单质和化合物、电解质与非电解质、酯化反应、化学键等,难度不大,注意稀有气体是单原子分子,无化学键.
本题难度:困难
3、选择题 核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象.试判断下列哪组原子均可产生NMR现象(? )
A.18O 31P
B.元素周期表中ⅢA族所有元素的原子
C.19F 12C
D.元素周期表中第三周期元素的所有原子
参考答案:B
本题解析:A.18O 质子数为8,中子数为10,没有NMR现象;31P质子数为15,中子数为16,有NMR现象.错误.B.元素周期表中ⅢA族所有元素的原子,元素的原子核内质子数都是奇数,都有NMR现象。正确。C.19F质子数为9,中子数为10,有NMR现象;12C质子数为6,中子数为6,没有NMR现象。错误。D.元素周期表中第三周期元素的所有原子,原子序数为奇数的所有元素因为质子数为奇数都有NMR现象;而原子序数为偶数的元素,如32S质子数为16,中子数为16,没有NMR现象。因此不符合题意。
本题难度:一般
4、选择题 有一种保健食品含有人体所必须的硒元素,有一定的保健作用,已知硒元素与氧元素同族,与钙元素同周期,下列关于硒的描述不正确的是(?)
A.原子序数是24
B.最高价氧化物是SeO3,是酸性氧化物
C.原子半径比钙小
D.气态氢化物化学式是H2Se,稳定性比HCl差
参考答案:A
本题解析:硒元素与氧、硫元素同主族,依据元素周期律,可得硒的原子序数是34,故A不正确;参照硫元素,可知硒的最高价氧化物是SeO3,是酸性氧化物,气态氢化物化学式是H2Se,氯元素的非金属性比硒强,所以稳定性比HCl差,故B、D正确;硒元素与钙元素同周期,原子半径从左到右逐渐减小,故C正确。
点评:本题考查元素周期表中元素性质递变规律及元素周期律,题目难度不大。
本题难度:简单
5、选择题 气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
元素
| I1/eV
| I2/eV
| I3/eV
|
甲
| 5.7
| 47.4
| 71.8
|
乙
| 7.7
| 15.1
| 80.3
|
丙
| 13.0
| 23.9
| 40.0
|
丁
| 15.7
| 27.6
| 40.7
|
下列说法正确的是(?)
A.甲的金属性比乙强?B.乙的化合价为+1价?
C.丙一定为金属元素?D.丁一定是金属元素
参考答案:A
本题解析:根据元素的电离能可知,甲元素的第二电离能远大于第一电离能,则甲应该是第IA族元素。所以选项A正确,其余选项都是错误的,答案选A。
点评:该题是中等难度的试题,试题侧重学生对电离能知识的熟悉了解掌握程度,以及灵活运用电离能知识解决实际问题的能力,有利于培养学生的逻辑推理能力和抽象思维能力。
本题难度:一般