��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� д�����з�Ӧ�����ӷ���ʽ��
��1��ʵ�����Ʊ�CO2______
��2���������������ᷴӦ______
��3��ʳ��ˮ����������Һ��Ӧ______
��4��NaOH��Һ������ķ�Ӧ______��
�ο��𰸣���1��ʵ��������̼��������ᷴӦ��ȡ������̼�������ӷ�ӦΪCaCO3+2H+�TCa2++CO2��+H2O���ʴ�Ϊ��CaCO3+2H+�TCa2++CO2��+H2O��
��2���������������ᷴӦ�������ᱵ��ˮ�������ӷ�ӦΪBa2++2OH-+2H++SO42-�TBaSO4��+2H2O���ʴ�Ϊ��Ba2++2OH-+2H++SO42-�TBaSO4��+2H2O��
��3��ʳ��ˮ����������Һ��Ӧ�����Ȼ����������ƣ������ӷ�ӦΪCl-+Ag+�TAgCl�����ʴ�Ϊ��Cl-+Ag+�TAgCl����
��4��NaOH��Һ������ķ�Ӧ���������ƺ�ˮ�������ӷ�ӦΪOH-+H+�TH2O���ʴ�Ϊ��OH-+H+�TH2O��
���������
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�����ӷ���ʽ�������?��?��
A���������м������Ũ��ˮ��Al3++4OH-====AlO2-+2H2O��
��
B��ͭ��Ũ���ᷴӦ��Cu+2NO3-+4H+====Cu2++2NO2��+2H2O
C��ʵ�����ô���ʯ��ϡ���ᷴӦ�ƶ�����̼���壺CO32-+2H+====CO2��+H2O
D�����Ȼ�����Һ����ӡˢ��·�壺Cu+2Fe3+====Cu2++2Fe2+
�ο��𰸣�AC
�������������������������������������������ᡢ���Ӧ���������ں�������ˮ��Ӧʱ��Ȼ��������������������A ����̼����dz���������������ӷ���ʽ����д��Ҫ��C����
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ�У���д��ȷ����
[? ]
A��̼��������Һ�м��������ʯ��ˮ��Ca2+ + 2HCO3- + 2OH- = CaCO3��+ CO32- + 2H2O
B���Ȼ�����Һ�м��������ˮ��Al3+ + 4NH3��H2O = AlO2- + 4NH4+ + 2H2O
C����̼������Һ����������������2CO32-+2SO2+H2O=2HCO3-+SO32-
D����FeBr2��Һ��ͨ��������Cl2���壺3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ��1�������������ڷǵ���ʵ���______������������ʵ���______������ţ���
�ٰ�ˮ?��SO2?��CI2?�ܴ�����?��BaSO4?���Ҵ�?��H2O?��NaHCO3
��2����Ũ��Ϊ0.1mol-L-1������ζ�����������Һʱ�����²�����ʹ���ƫ�ߵ���______������ţ���
����ƿֻ������ˮϴδ�ô���Һ��ϴ?����ʽ�ζ��ܶ����ǵ�ǰ���ӵκ���
����ʽ�ζ����¶˼��촦�ζ�ǰ�����ݵζ���û��?����ʽ�ζ���δ�ñ�Һ��ϴ
��3����������Һ����μ���Ba��OH��2��Һ��SO42-ǡ�ó�����ȫ��д����Ӧ�����ӷ���ʽ��______����ʱ��Һ��______�ԣ�����ԡ��������ԡ����ԡ�����ԭ��______��
�ο��𰸣���1���ٰ�ˮ�ǻ����Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
��SO2�Ƿǵ���ʣ�?
��Cl2�Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
�ܴ�������������ʣ���ˮ��ֻ�в��ֵ��룻
��BaSO4��ǿ����ʣ�
���Ҵ��ڷǵ���ʣ�
��H2O��������ʣ�
��NaHCO3��ǿ����ʣ�
�ʴ�Ϊ���ڢޣ��ܢߣ�
��2��A��������ˮϴ����ƿ���ô�����Һ������ϴ����V���ᣩ���䣬����Ũ�Ȳ��䣬�ʴ���
B���ζ�ǰ���ӣ��ζ����Ӷ������ᵼ��V���ᣩƫС�������Ũ��ƫС���ʴ���
C���ζ�ǰ���ֵζ��ܵļ��첿�������ݣ��ζ�����ʧ����V���ᣩƫ�������Ũ��ƫ����ȷ��
D��װHCl����ʽ�ζ���δ�ñ���HCl��Һ��ϴ����V���ᣩƫ�������Ũ��ƫ����ȷ��
��ѡ�ۢܣ�
��3��һ���������ػ�ѧʽ�к���2����������ӡ�1�������ӣ�һ������������ѧʽ�к���1�������ӡ�2�����������ӣ���������Һ����μ���Ba��OH��2��Һ��SO42-ǡ�ó�����ȫ���������������������ʵ���֮��Ϊ1��2���������Ӻ����������ӵ����ʵ���֮��Ϊ1��4�����Է����ķ�Ӧ����������Ӻͱ������������ᱵ�����������Ӻ�����������ǡ�÷�Ӧ����ƫ��������ӣ����Է�Ӧ���ӷ���ʽΪAl3++2SO42-+2Ba2++4OH-=2BaSO4��+AlO2-+2H2O��ƫ�������ǿ�������Σ�ƫ���������ˮ�������������Ũ�ȴ���������Ũ�ȣ�ʹ��Һ�ʼ��ԣ�
�ʴ�Ϊ��Al3++2SO42-+2Ba2++4OH-=2BaSO4��+AlO2-+2H2O���KAlO2��ǿ��������ˮ���Լ��ԣ�
���������
�����Ѷȣ���
5��ѡ����
A���ð�ˮ��������SO2���壺2NH3��H2O+SO2=2NH4++SO32-+H2O
B��NaHSO4��Һ�е���Ba(OH)2��Һ�����ԣ�H++SO42-+Ba2+ʮOH-===BaSO4��+H2O
C����H2O2�м�������KMnO4��Һ��2MnO4-+5H2O2+6H+====2Mn2+ +5O2��+8H2O
D���ö��Ե缫��ⱥ���Ȼ�����Һ��2Cl- + 2H+ H2��+ Cl2��
H2��+ Cl2��
�ο��𰸣�AC
���������B�ע�⡰��Һ�����ԡ��Ĺؼ��֣�������ȷ�����ӷ���ʽΪ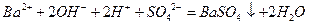 ,D��ö��Ե缫��ⱥ���Ȼ�����Һ�����ӷ���ʽӦΪ��
,D��ö��Ե缫��ⱥ���Ȼ�����Һ�����ӷ���ʽӦΪ��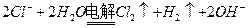 ,����Ŀ�г�����
,����Ŀ�г�����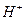 ������֮�����ڰ�ˮ���ˣ�ˮ��������ʣ����ܲ��������ʽ��
������֮�����ڰ�ˮ���ˣ�ˮ��������ʣ����ܲ��������ʽ��
�����Ѷȣ�һ��