微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 不需要化学变化就能够从海水中获得的物质是
[? ]
A.氯.溴.碘
B.钠.镁.铝
C.烧碱.氢气
D.氯化钠
参考答案:D
本题解析:
本题难度:简单
2、填空题 目前世界上60%的镁是从海水中提取的。学生就这个课题展开了讨论的。已知海水提镁的主要步骤如下
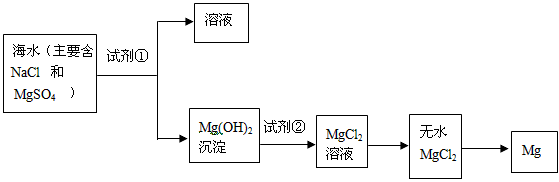
|
学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集?有三个学生提出自己的观点。
学生1的观点:直接往海水中加入沉淀剂。
学生2的观点:高温加热蒸发海水后,再加入沉淀剂。
学生3的观点:利用晒盐后的苦卤水,再加入沉淀剂。
请你评价三个学生提出的观点是否正确(填是或否),并简述理由。
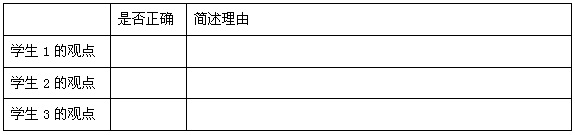
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是_______________(填化学式)。
(2)加入的足量试剂②是_____________(填化学式)。
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是_________________。
A.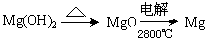
B.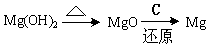
C.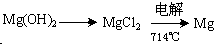
D.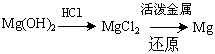
参考答案:(一) (二)(1)NaOH;(2)HCl;(3)C
(二)(1)NaOH;(2)HCl;(3)C
本题解析:
本题难度:一般
3、填空题 目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下
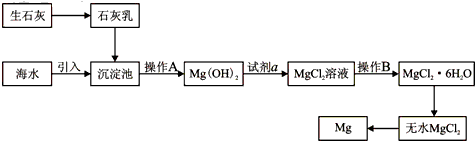
请回答下列问题:
(1)从离子反应的角度思考,在海水中加入石灰乳的作用是_______________________,写出在沉淀池的离子方程式_____________________。
(2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度,生产生石灰的主要原料来源于海洋中的_________________。
(3)操作A是_______________, 操作B是__________________。
(4)加入的足量试剂a是__________________(填化学式)。
(5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为___________________。从考虑成本和废物循环利用的角度,副产物氯气可以用于_________________。
(6)海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
_________________________。
参考答案:(1)沉淀Mg2+ (或使Mg2+形成Mg(OH)2沉淀);Mg2++2OH-==Mg(OH)2↓
(2)贝壳(或牡蛎壳等)
(3)过滤;加热浓缩(或蒸发结晶)
(4)HCl
(5)MgCl2(熔融) Mg+Cl2↑;制盐酸,循环使用
Mg+Cl2↑;制盐酸,循环使用
(6)海水中氯化镁的含量很大,但镁离子浓度很低,该过程可以使镁离子富集,浓度高,且成本低
本题解析:
本题难度:一般
4、填空题 (1)能源是当今社会发展的三大支柱之一。天然气是一种高效、低耗、污染小的清洁能源,主要成分为甲烷,甲烷燃烧的化学方程式为:__________ , 标准状况下,11.2L甲烷燃烧时,转移电子的物质的量为__________ mol。? 在如下图构想的物质循环中太阳能最终转化为 _________能。
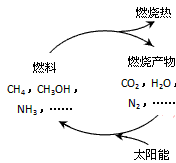
(2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀的主要原因,某同学按下图进行钢铁腐蚀的模拟,则负极的电极反应式为________ , 正极的电极反应式为 _________。 【提示:电化学的总反应式为2Fe+2H2O+O2==2Fe(OH)2】

(3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

操作①的名称是_________ ;反应②的离子方程式是__________ ,下述物质中不可做试剂③的是____________ 。
A.乙醇
B.苯
C.乙酸
D.四氯化碳
参考答案:(1)CH4 +2O2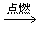 CO2 +2H2O;4; 热。
CO2 +2H2O;4; 热。
(2)2Fe - 4e- == 2Fe2+, O2 + 2H2O + 4e- = 4OH-
(3)溶解、过滤; H2O2 +2I-+2H+ = 2H2O + I2;? AC。
本题解析:
本题难度:一般
5、选择题 一位海上遇难的水手,随着木排在海上漂流.他用完了淡水,感到异常口渴,但他不喝海水,因为他知道海水会致命,主要原因是( )
A.海水有苦涩味,根本喝不下去
B.海水中含有多种盐,能使肠胃腐烂致人死亡
C.海水中有许多微生物,有些微生物能致人死亡
D.海水会造成人体水分从血液和组织内脱离出来,进入肠胃中,使人脱水死亡
参考答案:D
本题解析:
本题难度:一般