微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。将带余烬的木条插入试管D中,木条复燃。
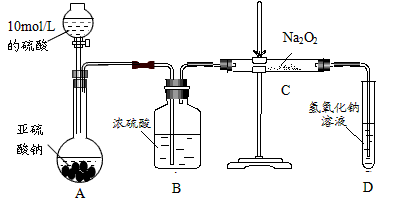
请回答下列问题:
(1)写出装置A中反应的化学方程式_____________________。
(2)第1小组同学通过类比思维,认为C装置中发生了如下反应:2Na2O2+2SO2=2Na2SO3+O2。该小组同学类比思维的类比理由方程式是_____________________。实验中,若去掉B装置,将SO2直接和
Na2O2反应,则不能证明实验中产生的O2是由SO2和Na2O2反应所得,原因是_____________________。
(3) 第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。第2小组同学的理由是_____________________。
参考答案:(1)Na2SO3+H2SO4==Na2SO4+SO2↑+H2O
(2)2Na2O2+2CO2==2Na2CO3+O2;若不用浓硫酸干燥,H2O与Na2O2也能反应生产O2
(3)Na2O2有强氧化性,可把Na2SO3氧化生产Na2SO4
本题解析:
本题难度:一般
2、实验题 某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象.请你帮 助该学生整理并完成实验报告
(1)实验目的:对同主族元素性质递变规律进行探究
实验用品:仪器:试管、胶头滴管等药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳
实验内容(在下列空格内填写相关内容)
(2)实验结论:_________________________
(3)问题和讨论:
①请用物质结构理论简单说明得出上述结论的原因______________________
②由于F2过于活泼,很难设计一个简单的实验验证其氧化性的强弱.试列举一个事实说明F的非金属性比Cl强:____________________
参考答案:“略”
本题解析:
本题难度:一般
3、实验题 (8分)(2011・西宁模拟)甲醛是世界卫生组织(WHO)确认的致癌物质和致畸物质之一。我国规定:室内甲醛含量不得超过0.08mg・m-3。某研究性学习小组打算利用酸性KMnO4溶液测定新装修房屋内的空气中甲醛的含量,请你参与并协助他们完成相关的学习任务。
测定原理:
酸性KMnO4为强氧化剂,可氧化甲醛和草酸,其反应方程式如下所示:
4MnO4-+5HCHO+12H+===4Mn2++5CO2↑+11H2O
2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
测定装置:
部分装置如下图所示:

测定步骤:
(1)用______________量取5.00 mL 1.00×10-3mol・L-1KMnO4溶液,注入洗气瓶中,并滴入几滴稀H2SO4,加水20 mL稀释,备用。
(2)将1.00×10-3 mol・L-1的草酸标准溶液置于酸式滴定管中备用。
(3)打开a,关闭b,用注射器抽取100 mL新装修房屋内的空气。关闭________,打开________(填“a”或“b”),再推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。再重复4次。
(4)将洗气瓶中的溶液转移到锥形瓶中(包括洗涤液),再用草酸标准溶液进行滴定,记录滴定所消耗的草酸标准溶液的体积。
(5)再重复实验2次(每次所取的高锰酸钾溶液的体积均为5.00 mL)。3次实验所消耗的草酸标准溶液的体积平均值为12.38 mL。
交流讨论:
(1)计算该新装修房屋内的空气中甲醛的浓度为________mg・m-3,该新装修房屋内的甲醛________(填“是”或“否”)超标;
(2)某同学用该方法测量空气中甲醛的含量时,所测得的数值比实际含量低,请你对其可能的原因(假设称量或量取、溶液配制及滴定实验均无错误)提出合理假设:______________、______________(至少答出两种可能性);
(3)实验结束后,该小组成员在相互交流的过程中一致认为:
①实验原理可以简化
实验中可不用草酸标准溶液滴定,可多次直接抽取新装修房屋内的空气,再推送到洗气瓶中,直至_________________________________________________________;
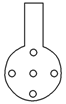
②实验装置应加以改进
可将插入酸性KMnO4溶液中的导管下端改成具有多孔的球泡(如图所示),有利于提高实验的准确度,其理由是___________________________________________________。
参考答案:测定步骤:(1)酸式滴定管"(3)a"b
交流讨论:(1)3.6"是
(2)注射器推送气体速度过快"装置气密性较差"同一地点取样次数太多等(任选其中两个作答或其他合理答案均可)
(3)①酸性KMnO4溶液刚好褪色"②可增大气体与溶液的接触面积,使空气中的甲醛被充分吸收
本题解析:本题考查了氧化还原滴定的计算,核心内容是得失电子守恒。实验的基本原理:先用过量的酸性高锰酸钾将甲醛氧化成CO2,然后用草酸还原剩余的酸性高锰酸钾。根据题目信息可知实验总共消耗含甲醛的空气体积为5×100 mL=0.5 L=0.0005 m3;
设0.5 L空气中甲醛的物质的量为x,则:
4x/5+0.01238 L×1.00×10-3 mol・L-1×2/5=5.00×10-3 L×1.00×10-3 mol・L-1
解得x=6.0×10-8mol
甲醛的质量:6.0×10-8mol×30000 mg・mol-1=1.8×10-3 mg
甲醛的浓度:1.8×10-3 mg÷0.0005 m3=3.6 mg・m-3。故新装修房屋内的甲醛超标。
本题难度:一般
4、实验题 某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
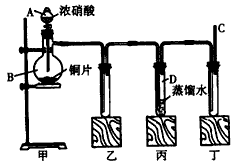
请回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是___________,该装置中发生反应的化学方程式为______________________。
(2)实验过程中,装置乙、丙中出现的现象分别是_________、___________,装置丙中的试管内发生反应的离子方程式为_____________________。
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是______。
(4)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________色,为了证明铁元素在该反应中的产物,可以再在溶液中滴加KSCN溶液,溶液变为___________色。
参考答案:(1)分液漏斗;Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
(2)生成红棕色气体;生成无色气体、蒸馏水中有气泡;3NO2+H2O=2H++2NO3-+NO
(3)氧气
(4)黄;红(或“血红”)
本题解析:
本题难度:一般
5、实验题 “碘钟”实验中,3I-+ S2O82-=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:

?回答下列问题:
(1)该实验的目的是____。
(2)显色时间t1=___。
(3)温度对该反应的反应速率的影响符合一般规律,若在 40℃下进行编号③对应浓度的实验,显色时间如的范围为 ___(填序号)。
A.< 22. 0s? B.22. 0s~44. 0s? C.> 44. 0s? D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是__。
参考答案:(1)研究反应物I-与S2O82-的浓度对反应速率的影响
(2)29.3s
(3)A
(4)反应速率与反应物起始浓度乘积成正比(或显色时问与反应物起始浓度乘积成反比)
本题解析:
本题难度:一般