微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列属于硅酸盐工业产品的是( )
A.水泥
B.晶体硅
C.沙子
D.陶瓷
参考答案:AD
本题解析:
本题难度:简单
2、选择题 海水资源丰富,海水淡化问题已成为科学家的主要研究方向,若实行海水淡化来供应饮用水,下列方法不正确的是 (? )?
A.利用太阳能,将海水蒸馏淡化
B.加入明矾,使海水的盐份沉淀并淡化
C.通直流电,采用电渗透法使海水淡化
D.通过离子交换膜,除去所含的盐分使海水淡化
参考答案:B
本题解析:蒸馏法是工业上淡化海水的一种常用方法,故A正确;明矾可以净水,其原理是明矾溶于水产生胶体,胶体能够吸附水中的悬浮物,从而达到净水的目的,而明矾不会吸附水中的离子,所以明矾不可以淡化海水,故B错误;电渗析法也是海水淡化的一种方法,C正确;通过离子交换树脂可以除去海水中的离子,从而达到淡化海水的目的,故D正确,答案选B。
点评:该题是基础性试题的考查,难度不大,记住即可。现在所用的海水淡化方法有蒸馏法、电渗析法、离子交换法等,其中蒸馏法的历史最久、技术和工艺也比较成熟,但成本较高。
本题难度:一般
3、填空题 (12分)【化学――化学与技术】
资源开发、材料制备及工农业生产等都离不开化学。请回答下列问题:
(1)工业制肥皂时,在皂化反应结束后需要在混合物中加入饱和食盐水。加入饱和食盐水的目的是?。
(2)Al2O3的熔点高达2050oC,工业上为了降低能量消耗,在金属铝的冶炼中通常采取的措施是?。
(3)工业上合成氨所需的氮气来源于?,氢气来源于?,写出工业上在催化剂作用下制取氢气的其中一个化学方程式?。
(4)工业制硫酸时,SO3的生成是在?(填设备名称)中进行的,工业上常采用浓硫酸吸收SO3,而不直接用水吸收的原因是?。在吸收塔中,为提高SO3的吸收率所采取的措施为?。
参考答案:(1)盐析,使肥皂从混合液中分离出来。(2)在氧化铝中加入冰晶石,降低混合物的熔点。(3)空气,水和碳氢化合物,CH4+H2O CO+H2或CH4+2H2O
CO+H2或CH4+2H2O CO2+2H2。(4)接触室,防止形成酸雾,影响SO3的吸收效率。从塔的下部通入SO3,从塔上部淋洒浓H2SO4,SO3和浓H2SO4在填料表面接触而被吸收。
CO2+2H2。(4)接触室,防止形成酸雾,影响SO3的吸收效率。从塔的下部通入SO3,从塔上部淋洒浓H2SO4,SO3和浓H2SO4在填料表面接触而被吸收。
本题解析: (1)工业制肥皂时,加入饱和食盐水的目的是盐析,使肥皂从混合液中分离出来。(2)Al2O3的熔点高达2050oC,工业上为了降低能量消耗,在金属铝的冶炼中通常采取的措施是在氧化铝中加入冰晶石,降低混合物的熔点。(3)工业上合成氨所需的氮气来源于空气,氢气来源于水和碳氢化合物,工业上在催化剂作用下制取氢气的化学方程式为CH4+H2O CO+H2或CH4+2H2O
CO+H2或CH4+2H2O CO2+2H2。(4)工业制硫酸时,SO3的生成是在接触室中进行的,工业上常采用浓硫酸吸收SO3,而不直接用水吸收的原因是防止形成酸雾,影响SO3的吸收效率。在吸收塔中,为提高SO3的吸收率所采取的措施为从塔的下部通入SO3,从塔上部淋洒浓H2SO4,SO3和浓H2SO4在填料表面接触而被吸收。
CO2+2H2。(4)工业制硫酸时,SO3的生成是在接触室中进行的,工业上常采用浓硫酸吸收SO3,而不直接用水吸收的原因是防止形成酸雾,影响SO3的吸收效率。在吸收塔中,为提高SO3的吸收率所采取的措施为从塔的下部通入SO3,从塔上部淋洒浓H2SO4,SO3和浓H2SO4在填料表面接触而被吸收。
本题难度:一般
4、计算题 今有CH4、HCHO、O2三种成分的混合气体,同温同压下与乙烷气体的密度相同。问:
(1)混合气体中CH4和O2的物质的量之比为多少?
(2)若某条件下水为气态,气体的摩尔体积为50 L・mol-1,在该条件下点燃混合气体,混合气恰好完全燃烧,共生成CO2 13.2 g,求原混合气体中氧气的物质的量和生成的混合气体在该条件下的密度。
参考答案:(1)混合气中n(CH4)∶n(O2)=1∶7,
(2)原混合气中含O2 0.35 mol。
本题解析:(1)CH4、HCHO、O2三种气体的相对分子质量分别为16、30、32,而混合气的平均相对分子质量即为C2H6的相对分子质量30。正巧与HCHO的相对分子质量相同。故CH4和O2组成气体的平均相对分子质量必须为30,用十字交叉法求出其物质的量比。
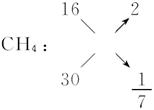
O2: ?32?14
即n(CH4)∶n(O2)="1∶" 7
(2)n(CO2)=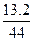 ="0.3" mol
="0.3" mol
设原有CH4 x mol,则n(HCHO)="(0.3-x)" mol,n(O2)="7x" mol
CH4完全燃烧时:CH4―2O2
x? 2x
HCHO完全燃烧时:HCHO ―O2
0.3-x? 0.3-x
2x+0.3-x="7x" ?x="0.05" (mol)
n(O2)="7x=0.35" mol
又CH4、HCHO燃烧前后Δn=0(H2O为气态),反应前后平均分子量不变。
又因为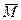 =30, 而
=30, 而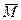 =50・ρ
=50・ρ
所以ρ=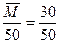 ="0.6" g・L-1
="0.6" g・L-1
本题难度:简单
5、选择题 利用金属活性的不同,可以采取不同的冶炼方法冶炼金属。下列反应所描述的冶炼方法不可能实现的是(?)
A.2Al2O3(熔融)  4Al+3O2↑
4Al+3O2↑
B.Fe2O3+3CO 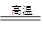 2Fe+3CO2
2Fe+3CO2
C.Fe+CuSO4 ===FeSO4+Cu
D.2NaCl(水溶液) 2Na+Cl2↑
2Na+Cl2↑
参考答案:D
本题解析:金属的冶炼一般依据金属性强弱选择,活泼的金属采用电解法,不活泼的金属采用热分解,处于中间的金属,采用还原剂还原,所以ABC都是正确的,D不正确,钠属于活泼的金属,应该用电解法,答案选D。
本题难度:一般