��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �Ʋ�����Na2O��CaO��SiO2���ߵ����ʵ���֮��Ϊ1��1��6�����Ʋ�����Na2SiO3��CaSiO3��SiO2�����ʵ���֮��Ϊ��?��
A��1��1��6
B��2��1��6
C��1��1��4
D��2��1��4
�ο��𰸣�C
����������������������廯���ٶ������ơ������ƺͶ�����������ʵ�����Ϊ1Ħ��1Ħ��6Ħ������˹�ϵ��ֻ��C�
�����Ѷȣ���
2��ѡ���� �±��н�����ұ��ԭ���뷽������ȫ��ȷ���ǣ�?��
?
| ұ��ԭ��
| ����
|
A
| 2HgO 2Hg��O2�� 2Hg��O2��
| �ȷֽⷨ
|
B
| 2Al2O3�����ڣ� 4Al��3O2�� 4Al��3O2��
| ��ⷨ
|
C
| Cu2S��O2 2Cu��SO2 2Cu��SO2
| �ȷֽⷨ
|
D
| Fe2O3��2Al 2Fe��Al2O3 2Fe��Al2O3
| �Ȼ�ԭ��
|
?
�ο��𰸣�C
������������ý���K��Ca��Na��Mg��Al���õ�ⷨұ�����еȻ��ý���Zn��Fe��Sn��Pb��Cu�����Ȼ�ԭ��ұ���������ý���Hg��Ag�����ȷֽⷨұ������A��B��D������ȷ��C�����
�����Ѷȣ�һ��
3������� ��12�֣�þ��һ����;�ܹ�Ľ������ϣ�Ŀǰ������60����þ�Ӻ�ˮ����ȡ����ˮ����Ҫ��NaCl��MgCl2�ȡ���Ҫ�������£�
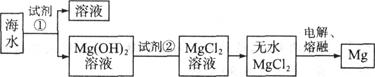
(1)Ϊ��ʹMgCl2ת��ΪMg(OH)2���Լ��ٿ���ѡ��___________��ҪʹMgCl2��ȫת��Ϊ�����������Լ��ٵ���Ӧ___________����֤MgCl2����ȫת��ΪMg(OH)2�ķ�����_______________________________��
(2)�����Լ��٣��ܹ�����õ�Mg(OH)2�����ķ����� ____________________ ��
(3)�Լ��ڿ���ѡ��___________________________��
(4)��ˮMgCl2������״̬�£�ͨ�������Mg��д���÷�Ӧ�Ļ�ѧ����ʽ
�ο��𰸣�

��4��MgCl2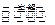 Mg + Cl2��
Mg + Cl2��
�����������
�����Ѷȣ���
4��ѡ���� �������ʵ�ת���ڸ�����������ʵ�ֵ��ǣ�������
��Na
Na2O2NaOH
��FeFe2O3FeCl3
��AlNaAlO2Al��OH��3
��SiSiO2H2SiO3
��Cu2��OH��2CO3CuOCuSO4��
A���٢ۢ�
B���ڢۢ�
C���ڢܢ�
D���٢ܢ�
�ο��𰸣�A
���������
�����Ѷȣ���
5������� ������Si3N4��һ�ַ�����������մɽṹ���ϣ���ĩ״��Si3N4������SiCl4��������NH3���Ļ���ﷴӦ��ȡ����ĩ״Si3N4�Կ�����ˮ�����ȶ�����ĩ״Si3N4��ˮ������һ���д̼�����ζ��������������������һ�������Ե����ĩ״Si3N4������Ӵ��ܲ���N2������һ�����ʣ����ǣ�����ĩ״Si3N4������MgO�����ۣ���230��1.01��105Pa��185����ܱ��������ȴ��������Եõ��ṹʮ�ֽ��ܡ��Կ�����ˮ���൱�ȶ��Ĺ�����ϣ�
��1��д����SiCl4��NH3�Ʊ�Si3N4�ķ�Ӧ����ʽ��______��
��2���ֱ�д����ĩ״Si3N4��H2O��O2��Ӧ�ķ���ʽ��______��______��
��3��Ϊʲô�ṹ���ܵĹ���Si3N4������H2O��O2����ʴ��
�ο��𰸣���1��SiCl4��������NH3�Ļ���ﷴӦ����Si3N4���仯ѧ����ʽΪ��3SiCl4+4NH3�TSi3N4+12HCl���ʴ�Ϊ��3SiCl4+4NH3�TSi3N4+12HCl��
��2����ĩ״Si3N4��ˮ������һ���д̼�����ζ��������������������ǰ�����һ�������Ե����ǹ��ᣬ�䷴Ӧ����ʽΪ��Si3N4+9H2O�T3H2SiO3+4NH3����ĩ״Si3N4������Ӵ��ܲ���N2������һ�����ʣ�����ԭ���غ��֪Ϊ�������裬�䷴Ӧ����ʽΪSi3N4+3O2�T3SiO2+2N2��
�ʴ�Ϊ��Si3N4+9H2O�T3H2SiO3+4NH3��Si3N4+3O2�T3SiO2+2N2��
��3����Ϊ�ڼ�ѹ�ͼ���������Si3N4��������������SiO2����MgOһ���γ����ܵ������ﱣ��Ĥ��ʹ����Si3N4������H2O��O2����ʴ��
�ʴ�Ϊ���ڼ�ѹ�ͼ���������Si3N4��������������SiO2����MgOһ���γ����ܵ������ﱣ��Ĥ��
���������
�����Ѷȣ�һ��