微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 湿润的蓝色石蕊试纸伸入盛有氯气的集气瓶中,观察到试纸变色的现象为( )
A.变红
B.变白
C.先变红后褪色
D.不变色
参考答案:氯气能与水反应生成盐酸和次氯酸,盐酸和次氯酸都具有酸性,使湿润的蓝色石蕊试纸变红,次氯酸具有强氧化性,有色物质为无色物质,所以现象为:先变红后变白,故选:C.
本题解析:
本题难度:简单
2、实验题 (10分)下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中D瓶中放有干燥红色布条;E中为铜网,E右端出气管口附近为石棉球。
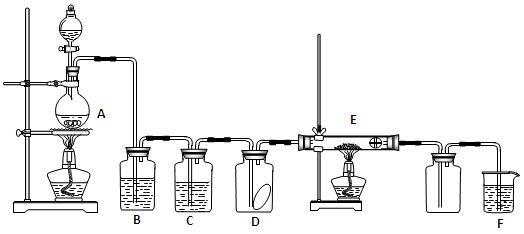
试回答:
(1)A中发生反应的方程式为_____________?_________________________________;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______________;
(3)C中盛放的试剂为_____________;
(4)E中所发生反应的方程式为____________________________________________。
(5)? F中应加入的试剂为?,其作用是?。
(6)若A中有14.6g HCl 被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量?为_____________g。
参考答案:MnO2 +4HCl(浓)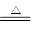 MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
Cu + Cl2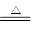 CuCl2 ?;碱液;吸收多余的氯气;50.8 g
CuCl2 ?;碱液;吸收多余的氯气;50.8 g
本题解析:(1)A是制取氯气的,方程式为MnO2 +4HCl(浓)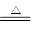 MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。
(2)由于浓盐酸易挥发,所以生成的氯气中混有氯化氢气体,而氯化氢极易溶于水,所以可以通过饱和食盐水来除去氯气中的氯化氢气体。
(3)D中是干燥的布条,所以要验证其漂白性,氯气应该是干燥的,所以C中是浓硫酸,用来干燥氯气。
(4)氯气具有强氧化性,在加热的条件下,能和铜反应生成氯化铜,方程式为Cu + Cl2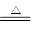 CuCl2 。
CuCl2 。
(5)氯气有毒,属于大气污染物,因此需要尾气处理。可用氢氧化钠等碱液来吸收。
(6)14.6g HCl 被氧化,则生成氯气是 ,因此可用产生0.2mol单质碘,其质量是0.2mol×254g/mol=50.8g。
,因此可用产生0.2mol单质碘,其质量是0.2mol×254g/mol=50.8g。
本题难度:一般
3、填空题 (8分)氯气及氯的化合物有着广泛的应用
(1)已知可逆反应Cl2+H2O ?HCl+HClO,向氯水中加入NaHCO3固体后,溶液中HClO的浓度?(填增大、减小、不变),原因是:?。
?HCl+HClO,向氯水中加入NaHCO3固体后,溶液中HClO的浓度?(填增大、减小、不变),原因是:?。
(2)我国卫生部已明确提出:逐步用二氧化氯替代氯气进行饮用水的消毒。
①用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO2-)。卫生部规定,饮用水中ClO 2-的含量应不超过0.2mg・L-1。当pH≤2.0时, ClO2-能被I-还原成Cl-。请写出反应的离子方程式?。
2-的含量应不超过0.2mg・L-1。当pH≤2.0时, ClO2-能被I-还原成Cl-。请写出反应的离子方程式?。
②用ClO2处理过的自来水中会残留ClO2?,可用FeCl2将ClO2还原为Cl-,该反应的氧化产物是?(填化学式)。现用V L(已换算为标准状况)ClO2处理一定量自来水,再加入a mol FeCl2可将残留的ClO2恰好除去。则该自来水中残留ClO2的物质的量为?mol。
参考答案:(8分)(1)增大(1分);氯气与水反应生成HCl和HClO,加入NaHCO3固体后,降 低H+的浓度,平衡正反应方向移动,HClO浓度增大(2分)
低H+的浓度,平衡正反应方向移动,HClO浓度增大(2分)
(2)①ClO2-+4H++4 I-=Cl-+2I2+2H2O (2分)
I-=Cl-+2I2+2H2O (2分)
②Fe(OH)3或FeCl3(1分);0.2a (2分)
本题解析:略
本题难度:简单
4、选择题 下列试剂保存方法不正确的是(? )
A.AgNO3溶液保存在棕色细口瓶中
B.氢氟酸保存在特制塑料瓶中
C.澄清石灰水保存在带胶塞的无色细口玻璃瓶中
D.AgBr保存在无色试剂瓶中
参考答案:D
本题解析:AgNO3见光分解,应保存在棕色细口瓶中;氢氟酸能腐蚀玻璃,常用特制塑料瓶盛装;Ca(OH)2能与玻璃成分之一的SiO2反应,盛石灰水的玻璃试剂瓶常用胶塞;AgBr见光易分解,不能保存在无色试剂瓶内。
本题难度:简单
5、选择题 如图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是

A.烧瓶中立即出现白烟
B.烧瓶中立即出现红棕色
C.烧瓶中发生的反应表明常温下氨气有还原性
D.烧杯中的溶液是为了吸收有害气体
参考答案:B
本题解析:A、氯气与氨气发生反应,生成白色固体氯化铵,正确;B、氯气与氨气发生氧化还原反应,氨气被氧化成无色氮气,错误;C、烧瓶中发生的反应表明常温下氨气有还原性,被氧化成氮气,正确;D、氯气、氨气对空气都有污染,不能直接排入空气中,所以用氢氧化钠溶液吸收,正确,答案选B。
本题难度:简单