微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。
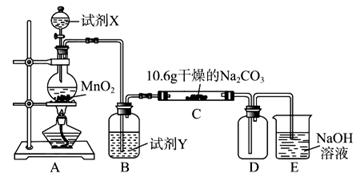
(1)写出装置A中发生反应的化学方程式:?。
(2)写出试剂Y的名称:??。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。可以确定的是C中含有的氯盐只有一种,且含有NaHCO3,现对C成分进行猜想和探究。
①提出合理假设。
假设一:存在两种成分: NaHCO3和?;
假设二:存在三种成分: NaHCO3和?、?。
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
实验步骤
| 预期现象和结论
|
步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。
| ?
|
步骤2:
| ?
|
步骤3:
| ?
|
(4)已知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为?。
参考答案:(12分)(1)4HCl(浓)+MnO2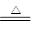 MnCl2+Cl2↑+2H2O (2分)
MnCl2+Cl2↑+2H2O (2分)
(2)饱和食盐水(或饱和氯化钠溶液) (1分)
(3)①假设一:NaCl (1分)
②假设二:NaCl? Na2CO3(2分)
 (每空1分)
(每空1分)
(3)2Cl2+2 Na2CO3+H2O ="=" 2NaHCO3+2NaCl+Cl2O (2分)
本题解析:(1)装置A是制取氯气的,所以反应的方程式是
4HCl(浓)+MnO2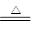 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)由于生成的氯气中含有挥发出的氯化氢,而氯化氢也能与碳酸钠反应。所以装置B中的试剂是除去氯气中的氯化氢气体的,因此试剂是饱和食盐水(或饱和氯化钠溶液) 。
(3)①在反应中氯气既是氧化剂,也是还原剂,所以一定有氯化钠生成,即假设一就是碳酸氢钠和氯化钠;又因为碳酸钠在反应中可能是过量的,所以假设二就是含有氯化钠、碳酸钠和碳酸氢钠。
②碳酸钠的检验可以利用氯化钡。而氯化钠的检验可以利用硝酸酸化的硝酸银溶液。
(4)0.1mol氯气生成0.1mol氯化钠,转移0.1mol电子。根据电子得失守恒可知,氧化产物中氯元素的化合价应该是+1价,即化合物是Cl2O ,所以反应的方程式是2Cl2+2 Na2CO3+H2O ="=" 2NaHCO3+2NaCl+Cl2O。
本题难度:一般
2、选择题 氯水在空气中长期放置,不考虑水蒸发的情况下,下列微粒的物质的量会增多的是( )
A.ClO-
B.HClO
C.水
D.Cl-
参考答案:A、氯水在空气中长期放置,次氯酸会分解,次氯酸根离子的量减少,故A错误;
B、氯水在空气中长期放置,次氯酸会分解,量减少了,故B错误;
C、不考虑水的蒸发,水的量几乎不变,故C错误;
D、氯水在空气中长期放置,次氯酸会分解,得到的是稀盐酸,次氯酸中的氯元素变为氯离子,所以氯离子的量增多了,故D正确.
故选D.
本题解析:
本题难度:简单
3、选择题 下列说法不正确的是?
A.钠、铁和铜一样都能在氯气中燃烧生成金属氯化物
B.检验氯气中是否混有氯化氢气体,可用硝酸银溶液
C.氯气跟变价金属反应生成高价金属氯化物
D.氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸
参考答案:B
本题解析:A中钠、铁和铜一样都能在氯气中燃烧生成金属氯化物,A正确;B中硝酸银溶液与氯气反应也生成白色沉淀氯化银,不能检验氯气中是否混有氯化氢,B不正确;C中氯气具有氢氧化性,氯气跟变价金属反应生成高价金属氯化物,C正确;氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸,D正确,答案选B。
点评:该题是高考中的常见考点,主要是考查学生对氯气性质的熟悉了解程度,特别是氯气漂白性,有利于调动学生的学习兴趣,增强学生的学习自信心,注意平时知识的积累和梳理。
本题难度:一般
4、实验题 二氧化锰与浓盐酸混合加热得到氯气,如图是制取并探究Cl2化学性质的装置图。

(1)圆底烧瓶中发生反应的化学方程式为________。
(2)若要得到干燥纯净的气体,B、C中应分别盛放的试剂为________、________。
(3)E中若装有FeCl2溶液,反应的离子方程式为________,E中若装有淀粉碘化钾溶液,能观察到的实验现象是______________________________________。
(4)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象某化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸加热
d.MnO2与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是__________________________________________,
实验c的目的是_________________________________________________。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是____________________________________________。
参考答案:(1)MnO2+4HCl(浓)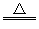 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)饱和食盐水?浓硫酸
(3)2Fe2++Cl2=2Fe3++2Cl-?溶液变蓝
(4)①探究c(Cl-)对反应的影响?探究c(H+)对反应的影响?②c(H+)的大小
本题解析:(1)MnO2与浓盐酸反应的化学方程式为:MnO2+4HCl(浓) MnCl2+
MnCl2+
Cl2↑+2H2O。
(2)用该方法制得的氯气中含有HCl和水蒸气,分别用饱和食盐水和浓硫酸除去。
(3)氯气与FeCl2溶液反应的离子方程式是:2Fe2++Cl2=2Fe3++2Cl-。氯气将KI氧化为单质碘,单质碘使淀粉变蓝色。
(4)对比a、b、c、d、e五个实验方案可以看出,五个实验中都有MnO2和Cl-,只有a、c、e中有较大浓度的H+,这三个实验产生了Cl2,b、d中有较大浓度的Cl-,但无H+,没有产生Cl2,说明影响氯气生成的原因是H+浓度的大小。实验b的目的是探究c(Cl-)对反应的影响,实验c的目的是探究c(H+)对反应的影响。
本题难度:一般
5、选择题 能与氯气和盐酸反应且生成不相同氯化物的是(? )
A.Fe
B.Al
C.Mg
D.Zn
参考答案:A
本题解析:Al、Mg、Zn与氯气或盐酸反应均分别是生成AlCl3、MgCl2、ZnCl2。铁和氯气反应生成氯化铁,和盐酸反应生成氯化亚铁,答案选A。
点评:该题是基础性试题的考查,试题难度不大。该题的关键是熟练记住常见反应的特点,然后灵活运用即可,有利于巩固学生的基础知识,提高学生分析问题、解决问题的能力。
本题难度:一般