微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某无色混合盐溶液中,除水电离产生的离子外可能含有①Na+?②Ba2+?③Cl-?④Br-?⑤SO32-?⑥SO42-离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤 | 操作 | 现象
(1)
用pH试纸检验
溶液的pH大于7
(2)
向溶液中滴加氯水,再加入CCl4振荡,静置
CCl4层呈橙色
(3)
分液,向所得水溶液中加入Ba(NO3)2溶液和稀HNO3
有白色沉淀产生
(4)
过滤,向滤液中加入AgNO3溶液和稀HNO3
有白色沉淀产生
|
下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑥
C.不能确定的离子是①
D.只能确定④存在,②不存在
参考答案:依据题干中的条件,溶液是无色混合溶液,则有色离子不存在,PH测得溶液PH大于7,溶液呈碱性,说明一定有弱酸根离子,则含有SO32-,无Ba2+;
溶液中滴加氯水后萃取,萃取层呈橙色证明原溶液含溴离子;
分液加入Ba(NO3)2溶液和稀HNO3,有白色沉淀生成,说明溶液中可能含硫酸根离子,过滤,向滤液中加入AgNO3溶液和稀HNO3,有白色沉淀生成,证明是氯离子,但(2)加入氯水加入了氯离子,不能确定是否含氯离子;
根据以上分析溶液中一定含有SO32-、Br-,无Ba2+;
依据电荷守恒,溶液中一定含Na+;
所以溶液中一定存在的离子是①④⑤;
故选A.
本题解析:
本题难度:简单
2、填空题 在Na+的物质的量浓度为0.5mol?L-1的某澄清溶液中,还可能含有如表中所示的若干种离子.
| 阳离子 | K+、Ag+、Mg2+、Ba2+
阴离子
NO、CO、SiO、SO
|
取100mL该溶液进行如下实验(气体体积在标准状况下测定):
| 序号 | 实验内容 | 实验结果
Ⅰ
想该溶液中加入足量稀盐酸
生成白色沉淀并在标准状况下放出0.56L气体
Ⅱ
将Ⅰ中产生的混合液过滤,将沉淀洗涤、灼烧至恒重,称量所得固体的质量
固体质量为2.4g
Ⅲ
向Ⅱ中所得的滤液中滴加BaCl2溶液
无明显现象
|
请回答下列问题:
(1)由实验Ⅰ确定一定不存在的离子是______.
(2)实验Ⅰ中生成沉淀的离子方程式为______.
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写表中阴离子的物质的量浓度(能计算出结果的填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
| 阴离子 | NO | CO | SiO | SO
c/mol?L-1
______?
______
______?
______?
|
(4)判断K+是否存在,若存在,求其最小浓度,若不存在,请说明理由:______.
参考答案:由题意知溶液为澄清溶液,因此溶液中含有的离子必须能大量共存.由实验Ⅰ可知,该溶液中一定含有CO32-,其浓度为0.56L22.4L/mol0.1L=0.25mol/L,则一定没有Ag+、Mg2+、Ba2+;由生成白色沉淀判断溶液中一定含有SiO32-,发生反应SiO32-+2H+=H2SiO3↓,SiO32-的浓度为2.4g60g/mol0.1L=0.4mol/L.由实验Ⅲ可知溶液中不含SO42-,根据电荷守恒2c(CO32-)+2c(SiO32-)=2×0.25mol/L+2×0.4mol/L=1.3mol/L>0.5mol/L,因此溶液中一定含有K+,且其浓度至少为0.8mol/L,不能确定NO3-是否存在.
(1)由实验Ⅰ可知,加入足量稀盐酸生成白色沉淀并在标准状况下放出0.56L气体,则该溶液中一定含有CO32-、SiO32-,则一定没有Ag+、Mg2+、Ba2+,
故答案为:Ag+、Mg2+、Ba2+;
(2)实验Ⅰ中生成沉淀的离子方程式为:SiO32-+2H+=H2SiO3↓,
故答案为:SiO32-+2H+=H2SiO3↓;
(3)通过上述分析计算可知,
阴离子NO3-?CO32-SiO32-SO42-c/mol?L-1?0.25mol/L0.4mol/L?0?(4)根据电荷守恒2c(CO32-+)+2c(SiO32-)=2×0.25mol/L+2×0.4mol/L=1.3mol/L>0.5mol/L,因此溶液中一定含有K+,且其浓度至少为0.8mol/L,
故答案为:存在,其浓度至少为0.8mol/L.
本题解析:
本题难度:一般
3、选择题 能够大量共存的离子组是:
A.强碱性溶液中:Na+、K+、SO42-、AlO2-
B.含有0.1 mol・L-1Fe3+的溶液中:K+、Mg2+、Cl-、SCN-
C.某无色溶液中:NH4+、Fe2+、MnO4-、NO3-
D.与铝反应生成H2的溶液中:Na+、K+、Cl-、SO42-
参考答案:AD
本题解析:A 可以大量共存,离子之间不反应
B 不可以 Fe3+与SCN-不能大量共存
C?不符合Fe2+为浅绿色,不是无色
D 可以?与铝反应生成H2的溶液可能显酸性,也可能显碱性,但这些离子都不和H+、
OH-反应
本题难度:简单
4、选择题 下列表示正确的是(?)
A.用碳酸钠溶液吸收少量二氧化硫: 2CO32-+SO2+H2O =2HCO3-+SO32-
B.CO(g)的燃烧热是283.0kJ・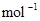 ,则
,则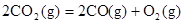 反应的
反应的

C.含有大量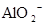 的溶液中:K+、
的溶液中:K+、 、
、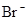 、
、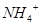 可共存
可共存
D.在某钠盐溶液中含有等物质的量的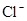 、
、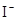 、
、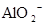 、
、 、
、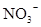 、
、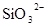 中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,阴离子种数减少3种,则原溶液中一定有
中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,阴离子种数减少3种,则原溶液中一定有
参考答案:A
本题解析:酸性:亚硫酸强于碳酸,所以向碳酸钠溶液中通入少量二氧化硫发生反应产生亚硫酸钠和碳酸氢钠,从而可以用来吸收二氧化硫气体。反应的离子方程式是:2CO32-+SO2+H2O =2HCO3-+SO32-。正确。B.一氧化碳燃烧放热,则二氧化碳分解吸热。故2CO2(g)=2CO(g)+O2(g)反应的反应热为ΔH=+566KJ/mol.错误。C. 含AlO2-的溶液显碱性,在碱性溶液中NH4+不能大量存在。错误。D.加入过量盐酸时H+?、I-、 NO3-发生氧化还原反应产生NO气体和I2,I2使溶液颜色加深,AlO2-反应转化为Al3+,SiO32-与氢离子反应产生硅酸沉淀。所以即使没有碳酸根离子也会有气泡产生。故错误。
本题难度:一般
5、选择题 下列各组离子中,能在溶液中大量共存的是
[? ]
A.Na+、Cu2+、Cl-
B.H+、Cl-、CO32-
C.Ba2+、Na+、SO42-
D.H+、K+、OH-
参考答案:A
本题解析:
本题难度:一般