微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (13分)实验室要配制1 mol・L-1的稀硫酸250mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸 mL
(2)配制时,必须使用的仪器有 (填代号)
①烧杯 ②100 mL量筒 ③20 mL量筒 ④1000 mL容量瓶 ⑤250 mL容量瓶 ⑥托盘天平(带砝码) ⑦玻璃棒还缺少的仪器是 。
(3)配制时,该实验两次用到玻璃棒,其作用分别是 ? 、 。
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”)
①没有洗涤烧杯和玻璃棒。 。
②如果加水超过了刻度线,取出水使液面恰好到刻度线。 。
③容量瓶没有干燥。
④定容时俯视容量瓶瓶颈刻度线??
参考答案:(1)13.6(3分)(2)①③⑤⑦(2分)胶头滴管 (2分)
(3)搅拌(1分)、引流 (1分)
(4)偏低、偏低、无影响、偏高(各1分)
本题解析:略
本题难度:一般
2、简答题 某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示:
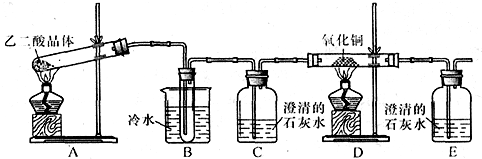
查阅资料可知:乙二酸晶体(H2C2O4?2H2O)熔点100.1℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu.
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:______;
(2)装置B的作用是______;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是______;______.
(3)实验结束后向装置B的试管中加入NaHCO3溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是______.
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物.实验小组进一步探究:①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是______.②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L.则红色固体中含单质铜的质量分数是______.
参考答案:(1)C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,说明乙二酸晶体加热生成一氧化碳、二氧化碳和水,反应的化学方程式:H2C2O4?2H2O?△?.?CO↑+CO2↑+3H2O;
故答案为:H2C2O4?2H2O?△?.?CO↑+CO2↑+3H2O;
(2)乙二酸可以和氢氧化钙发生反应,所以防止对检验分解产物CO2的干扰,要除去生成物中带出的乙二酸蒸汽,一氧化碳在还原氧化铜之前要将气体干燥,一氧化碳有毒,所以要进行尾气处理,
故答案为:除去生成物中带出的乙二酸蒸汽,防止对检验分解产物CO2的干扰;在C与D之间再装配一个盛浓硫酸的洗气瓶(或装有碱石灰的干燥管),将装置E中出来的气体引到酒精灯火焰上让其燃烧(或收集装置E中逸出的尾气);
(3)B的试管中是乙二酸,加入NaHCO3溶液,产生大量无色气体应该是二氧化碳,化学反应遵循强酸制弱酸的原理,所以酸性是乙二酸大于碳酸(或H2C2O4>H2CO3),故答案为:乙二酸大于碳酸(或H2C2O4>H2CO3);
(4)①金属铜和硫酸不反应,但是氧化亚铜可以和硫酸反应生成金属铜和硫酸铜,根据实验现象:溶液变为蓝色,则证明红色固体中含有Cu2O,故答案为:红色固体中含有Cu2O;
②设红色固体中氧化亚铜的物质的量是x,金属铜的物质的量为y,根据质量关系得:144x+64y=6.8,根据电子守恒,得出:2x+2y=1.12L22.4L/mol×(5-2),两式联立解得x=0.025mol,y=0.05mol,所以Cu的质量分数为:0.05mol×64g/mol6.8g×100%=50%,故答案为:50%.
本题解析:
本题难度:一般
3、实验题 某校学生活动小组设计如图所示装置探究工业制硫酸接触室中反应产物,并测定此条件下二氧化硫的转化率。实验时,装置D锥形瓶中溶液产生白色沉淀,装置E中溶液褪色。
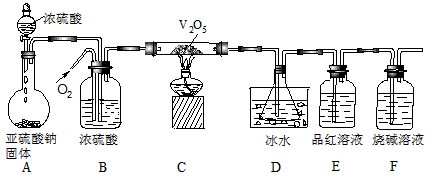
(1)装置B的三个作用是①______________;②______________;③______________。
(2)实验过程中,当V2O5表面红热后,应将酒精灯移开一会儿后再继续加热,其原因是____________________________。
(3)D中锥形瓶盛放的溶液可以是(选填序号)__________。
① 少量澄清石灰水 ②少量小苏打溶液 ③少量氯化钡溶液 ④少量硝酸钡溶液
反应停止后,要通过装置D锥形瓶中产生的白色沉淀的量,测定已被氧化的二氧化硫的量时,在滤出沉淀前必须进行的一步实验操作是(简述过程)___________________________。
(4)若从锥形瓶溶液中得到的沉淀质量为m g,要测定该条件下二氧化硫的转化率,实验时还需要测定的数据是(选填序号)______________,二氧化硫的转化率是______________(用含有m、a、b、c、d中的一种或几种字母的代数式表示)。
① 装置F增加的质量a g ② 装置A中亚硫酸钠减少的质量b g
③ 装置B增加的质量c g ④ 装置E增加的质量d g
参考答案:(1)①干燥氧气和二氧化硫;②使氧气和二氧化硫混合均匀;③便于通过观察气泡的速率,控制氧气和二氧化硫的比例
(2)该反应的正反应放热,温度过高平衡逆向移动,不利于三氧化硫的生成;且影响催化剂的活性
(3)③;向锥形瓶中滴加氯化钡溶液,直至沉淀量不再增加。(或“静置后向上层清液中滴入氯化钡溶液,若产生沉淀,继续加入氯化钡溶液,重复上述过程至清液中不再产生沉淀)
(4)①④;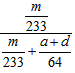 ×100%
×100%
本题解析:
本题难度:困难
4、实验题 (4分)用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
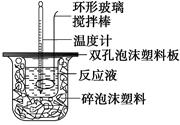
(1)烧杯间填满碎泡沫塑料的作用是?;
(2)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是?;实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量?(填“相等”或“不相等”),若实验操作均正确,则所求中和热?(填“相等”或“不相等”);
参考答案:(1)减少热量损失(1分)
(2)为了确保盐酸完全被中和(1分);不相等(1分);相等(1分)。
本题解析:略
本题难度:简单
5、填空题 (10分)阅读下列实验内容,根据题目要求回答问题。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol・L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol・L-1 NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入2滴酚酞。
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2―3cm处,再把碱式滴定管固定好,调节液面至 刻度“0”或“0”刻度以下
