微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,分别将四块形状相同、质量为7g?的铁块同时放入下列四种溶液中,产生H2速率最快的是
A.150mL 2mol・L-1的盐酸
B.500mL 2mol・L-1的硫酸
C.50mL 6mol・L-1的稀硝酸
D.50mL 18.4mol・L-1的硫酸
参考答案:B
本题解析:酸的浓度越大产生氢气的速率越快,2mol・L-1的盐酸中氢离子浓度为2 mol・L-1,? 2mol・L-1的硫酸中氢离子浓度为4 mol・L-1。硝酸与浓硫酸与铁反应不产生氢气。
本题难度:一般
2、选择题 下列事实不能用勒夏特列原理解释的是
①氯化铁溶液加热蒸干最终得不到氯化铁固体?②铁在潮湿的空气中容易生锈
③实验室可用排饱和食盐水的方法收集氯气
④常温下,将1 mL pH=3的醋酸加水稀释至100 mL,测得其pH<5
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)  ?K(g)+NaCl(l)
?K(g)+NaCl(l)
⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深
A.②⑥
B.①②③
C.②⑤⑥
D.①③④⑤
参考答案:A
本题解析:①因为FeCl3在溶液中水解:FeCl3+3H2O Fe(OH)3+3HCl,加入HCl挥发,平衡正移,故氯化铁溶液加热蒸干最终得不到氯化铁固体;②铁在潮湿的空气中容易生锈,属于电化学腐蚀;③因为Cl2+H2O
Fe(OH)3+3HCl,加入HCl挥发,平衡正移,故氯化铁溶液加热蒸干最终得不到氯化铁固体;②铁在潮湿的空气中容易生锈,属于电化学腐蚀;③因为Cl2+H2O HClO+H++Cl-,饱和食盐水中Cl-大,抑制了反应的正向进行,故实验室可用排饱和食盐水的方法收集氯气;④稀释促进了醋酸的电离,常温下,将1 mL pH=3的醋酸加水稀释至100 mL,故测得其pH<5;⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)
HClO+H++Cl-,饱和食盐水中Cl-大,抑制了反应的正向进行,故实验室可用排饱和食盐水的方法收集氯气;④稀释促进了醋酸的电离,常温下,将1 mL pH=3的醋酸加水稀释至100 mL,故测得其pH<5;⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)  ?K(g)+NaCl(l),K蒸气逸出,使平衡正向移动;⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深,是因为加压缩小体积,增大了NO2的浓度,颜色加深,与平衡移动无关。
?K(g)+NaCl(l),K蒸气逸出,使平衡正向移动;⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深,是因为加压缩小体积,增大了NO2的浓度,颜色加深,与平衡移动无关。
本题难度:一般
3、选择题 对于反应aA(g)+bB(g) cC(g)+dD(g),达到平衡后其他条件不变改变压强,则右图适合于哪种情况(? )
cC(g)+dD(g),达到平衡后其他条件不变改变压强,则右图适合于哪种情况(? )

A.a+b<c+d,减压
B.a+b>c+d,加压
C.a+b<c+d,加压
D.a+b>c+d,减压
参考答案:A
本题解析:向正方向移动的同时,速率均变小。而减小压强向增大压强方向移动,所以c+d>a+b。
本题难度:简单
4、选择题 把在空气中久置的铝片 5.0 g投入盛有500mL0.5mol・L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如右的坐标曲线来表示,下列推论错误的是
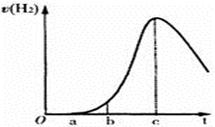
A.t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液
B.t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高
C.t=c时反应处平衡状态
D.t>c产生氢气的速率降低主要是因为溶液中c(H+)降低
参考答案:C
本题解析:金属铝与稀硫酸的反应不是可逆反应,不存在平衡状态,选项C不正确,其余选项都是正确的,答案选C。
本题难度:简单
5、选择题 下列事实中,能用勒沙特列原理来解释的是
A.由H2(g)、I2(g)、HI(g)组成的混合气体平衡体系加压后颜色加深
B.久置的氯水变成了稀盐酸
C.在FeCl3溶液中加入铁粉防止氧化变质
D.加入催化剂有利于SO2与O2反应制SO3
参考答案:B
本题解析:A选项,由于反应2HI(g)?H2(g)+I2(g) 反应物与生成物计量数之和相等,加压后平衡不移动,颜色加深是由于浓度变大的原因,故错误。B选项,Cl2+H2O?HCl+HClO, 2HClO=2HCl+O2由于次氯酸见光会分解,消耗了次氯酸,使第一个可逆反应向正方向进行,不断的消耗了氯气,最终为盐酸。故正确。C选项,在FeCl3溶液中加入铁粉,是由于防止氧化还原反应,与勒夏特列原理无关。D选项,加入催化剂反应平衡不移动。故错误。
本题难度:一般