��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ������أ�K2FeO4�����м�ǿ�������ԣ���һ��������ˮ��������
��1��FeO42-��ˮ��Ӧ�ķ���ʽΪ��4FeO42- + 10H2O  ?4Fe(OH)3 + 8OH��+ 3O2��
?4Fe(OH)3 + 8OH��+ 3O2��
K2FeO4�ڴ���ˮ�Ĺ����������������?��?��

��2��������K2FeO4���Ƴ�c(FeO42-) ��1.0��10-3 mol��L-1��1.0mmol��L-1�����������������ֱ�����20�桢30�桢40���60��ĺ���ˮԡ�У��ⶨc(FeO42-)�ı仯�������ͼ���⣨1���еķ�ӦΪFeO42-�仯������Ӧ���÷�Ӧ�ġ�H?0��
��3��FeO42-��ˮ��Һ�еĴ�����̬��ͼ����ʾ������˵����ȷ����?������ĸ����
A��������Һ�������α仯����Ԫ�ض���4�ִ�����̬
B���ı���Һ��pH������Һ��pH��10����pH��4�Ĺ����У�HFeO4���ķֲ�������������С
C����pH��8��������Һ�м�KOH��Һ��������Ӧ�����ӷ���ʽΪ��H2FeO4��OH����HFeO4����H2O
D��pHԼΪ2.5 ʱ����Һ��H3FeO4+��HFeO4�������൱
��4��HFeO4�� H++FeO42-�ĵ���ƽ�ⳣ������ʽΪK=___________________������ֵ�ӽ�?������ĸ����
H++FeO42-�ĵ���ƽ�ⳣ������ʽΪK=___________________������ֵ�ӽ�?������ĸ����
A��10-2.5?B��10-6?C��10-7?D��10-10
��5��25��ʱ��CaFeO4��Ksp = 4.536��10-9����Ҫʹ100mL��1.0��10-3 mol��L-1��K2FeO4��Һ�е�c(FeO42- )��ȫ����������������Ҫ�����Ca(OH)2�����ʵ���Ϊ?mol��
��ȫ��������Һ�в�����c(FeO42- )Ϊ______________��
�ο��𰸣���1��ɱ���������������ʣ�2��>��3��BD��4��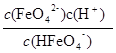 ?C��5��4.536��10-5��1��10-5mol/L
?C��5��4.536��10-5��1��10-5mol/L
�����������1��FeO42-����ǿ�����ԣ�������ɱ����FeO42-��ˮ���ɵ�Fe(OH)3����������ˮ�е������ʹˮ�徻������2����ͼI���Կ������¶�Խ�ߣ���Һ��c(FeO42-)ԽС��˵�������¶ȣ�ƽ�������ƶ�����������Ӧ�����ȷ�Ӧ����3����ͼ��֪��pHС��1.5ʱ����Һ��ֻ��H3FeO4+��H2FeO4��A����pH��10����4ʱ��HFeO4���ķֲ�������������С��B��ȷ����pH=8�ĸ���Һ�м�KOH��Һ��pH�������ӷ���ʽΪHFeO4-+OH-=FeO42-+H2O��C����pHԼΪ2.5 ʱ�� H3FeO4+��HFeO4���ֲ�������ȣ�D��ȷ����4��HFeO4�� H++FeO42-�ĵ���ƽ�ⳣ��K=
H++FeO42-�ĵ���ƽ�ⳣ��K=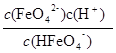 ����pH�ӽ�7ʱ��c(FeO42-)=c(HFeO4-)��K��10-7����5��Ҫ�γ�CaFeO4����������c(Ca2+)��c(FeO42-)>Ksp(CaFeO4)��
����pH�ӽ�7ʱ��c(FeO42-)=c(HFeO4-)��K��10-7����5��Ҫ�γ�CaFeO4����������c(Ca2+)��c(FeO42-)>Ksp(CaFeO4)��
��������ɳ����ԭ������������ƽ����ϵ��������Һ��ϣ��γɳ�����������Q>Ksp��
�����Ѷȣ�����
2��ѡ���� ij�¶��£���һ��2L���ܱ������У�����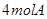 ��
��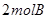 �������·�Ӧ��
�������·�Ӧ��
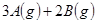

 ����Ӧһ��ʱ���ﵽƽ�⣬�������
����Ӧһ��ʱ���ﵽƽ�⣬�������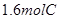 ��������˵����ȷ����
��������˵����ȷ����
A���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��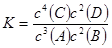
B����ʱ��B��ƽ��ת������40%
C���������ϵ��ѹǿ����ѧƽ�ⳣ������
D������B��B��ƽ��ת��������
�ο��𰸣�B
�������������C�ǹ��壬���ܳ�����ƽ�ⳣ���ı���ʽ�У�A����ȷ������1.6mol��C��������B��0.8mol������ת������0.8��2��100����40����ѡ��B��ȷ��ƽ�ⳣ��ֻ���¶��й�ϵ��C����ȷ������B������ƽ��������Ӧ�����ƶ������A��ת���ʣ�������B��ת���ʣ�D����ȷ����ѡB��
�����Ѷȣ�һ��
3������� ��14�֣�
��ҵ�ϳɰ���Ӧ��N2+3H2 2NH3����һ���������Ѵﵽƽ��״̬��
2NH3����һ���������Ѵﵽƽ��״̬��
��1���������¶ȣ���ʹ����ƽ�������ɰ��ķ����ƶ�������ÿĦ�����ķ�Ӧ����ֵ��46.2KJ/mol,��÷�Ӧ���Ȼ�ѧ����ʽΪ?��
��2�����ں��������£���N2��H2��һ��������ϵ�����ͨ��һ���ݻ�Ϊ2���̶��ݻ����ܱ������У�5���Ӻ�Ӧ��ƽ��ʱ��n(N2)="1.2mol," n(H2)="1.2mol," n (NH3)=0.8mol,��Ӧ����V��N2��=?mol��L-1��min-1��H2��ת����=?��ƽ�ⳣ��=?���������������¶Ⱥ��ݻ����䣬������ƽ����ϵ�еĻ�������Ũ������1������ƽ��?��������p���һ��ƶ����ƶ���
��3�����ں��º�ѹ�����£���1 molN2��3 molH2�Ļ������ͨ��һ���ݻ��ɱ�������з�����Ӧ����ƽ�������a molNH3,��ʱN2�����ʵ���Ϊ?mol,���ú�a�Ĵ���ʽ��ʾ��������ʼʱֻͨ��N2��H2����ƽ��ʱ����3amolNH3����ʼʱӦͨ��N2?3mol,H2 =?mol(ƽ��ʱNH3������������ǰ����ͬ)������ʼʱͨ��x molN2�p6molH2��2mol NH3����ƽ���N2��NH3�����ʵ����ֱ�Ϊy mol��3a mol,��x=?mol,y=?mol���ú�a�Ĵ���ʽ��ʾ��
�ο��𰸣���14�֣�
��1�� N2(g) +3H2(g)  2NH3(g),��H=-92.4KJ��mol-1
2NH3(g),��H=-92.4KJ��mol-1
��2�� 0.04? 50%? 1.23?����
��3��? 1-a/2? 9? 2? 3-3a/2
�����������
�����Ѷȣ�һ��
4������� ��6�֣���ˮ��Һ�гȺ�ɫ��Cr2O72�����ɫ��CrO42��������ƽ���ϵ��
Cr2O72����H2O  ?2CrO42����2H������K2Cr2O7����ˮ���ϡ��Һ, ��Һ�ʳ�ɫ��
?2CrO42����2H������K2Cr2O7����ˮ���ϡ��Һ, ��Һ�ʳ�ɫ��
��1����������Һ�м���NaOH��Һ����Һ��_______ɫ��ƽ��________��(������ơ��������ơ�����ͬ��)
��2���ټ������ϡH2SO4������Һ��_______ɫ��ƽ��________��
��3����ԭ��Һ�м���Ba(NO3)2��Һ����֪BaCrO4Ϊ��ɫ��������ƽ��_______________����Һ��ɫ��__________��
�ο��𰸣���1����ɫ�������ƣ�2���Ⱥ�ɫ�������ƣ�3�������Ʊ�dz
�����������������Һ�м���NaOH��Һ���к�H+ƽ��������Ӧ�����ƶ�����ɫ��CrO42-��࣬��Һ�ʻ�ɫ����1)���ټ������ϡH2SO4��ƽ�����淴Ӧ�����ƶ�����Һ�ʳȺ�ɫ��C(CrO42-)��Сƽ��������Ӧ�����ƶ�����Һ��ɫ��dz����ΪŨ�ȱ�С�ˡ�
�����Ѷȣ�һ��
5������� ��12�֣���һ��2L���ܱ������У�Ͷ�뷴Ӧ�������Ӧ2SO3(g) 2SO2(g)��O2(g)? ��H��0������SO3�ı仯����ͼ��ʾ��
2SO2(g)��O2(g)? ��H��0������SO3�ı仯����ͼ��ʾ��
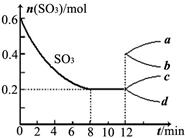
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ������8minʱ����ƽ���������?��
��2����O2��ʾ0��8min�ڸ÷�Ӧ��ƽ������v=?��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����?��
A��v(SO3)=2v(O2) ? B��������ѹǿ���ֲ���
C��v(SO2)��=2v(O2)��?D���������ܶȱ��ֲ���
��4���ڵ�12minʱ������ѹ����1L����SO3�ı仯����Ϊ?��
A��a? B��b? C��c? D��d
��5���������ݻ������ڵ�12minʱ������SO3(g)����ƽ����?��Ӧ�����ƶ�����������桱����SO3���������?�������С������
�ο��𰸣���1��K= = 0.4?��2��0.0125 mol/(L��min)
= 0.4?��2��0.0125 mol/(L��min)
��3��B��C?��4��C?��5����?����
�����������1��K= ��8����ʱc(SO3)=0.1mol/L����c(SO2)=0.2mol/L��c(O2)=0.1mol/L������K=0.4��
��8����ʱc(SO3)=0.1mol/L����c(SO2)=0.2mol/L��c(O2)=0.1mol/L������K=0.4��
��2��v(O2)=
��3����Ӧǰ��ѹǿ���ȣ����Կ�����ѹǿ���ٱ仯�жϷ�Ӧ��ƽ�⣬v(SO2)��=2v(O2)�������淴Ӧ������ȣ������жϷ�Ӧ��ƽ�⣬���ѡBC��
��4������ѹ����˲�䣬SO3���ʵ������䣬�漴ƽ�������ƶ���SO3�����ʵ�����������c���߷��ϡ�
��5���������ݻ������ڵ�12minʱ������SO3(g)���൱�ڶ���ϵ��ѹ��ƽ�������ƶ�����SO3�������������
����������dz�������ֻҪ����Ӱ��ƽ���ƶ������ؼ��ɡ�
�����Ѷȣ�һ��