��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� Ϊ���������CO2�ĺ�����������⣬ij��ѧ���������ɫ���ɡ����룺�ѹ����ų��ĸ���CO2�ķ�������������̼�����Һ���գ�Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧʹ�����е�CO2ת��Ϊȼ�ϼ״�������ɫ���ɡ�����IJ��ּ����������£�

��1���ϳ����з�Ӧ�Ļ�ѧ����ʽΪ______����H��0����ƽ���ƶ�ԭ���������������������ԭ������ƽ��ת���ʣ���ʵ�������в���300����¶ȣ��������¶ȶԷ�Ӧ���ʵ�Ӱ���⣬����Ҫ������______��
��2���Ӻϳ���������״���ԭ��������______������ԭ���Ƚ����������ĸ����
A������?B����Һ?C������?D���ᾧ
��3����ҵ������һ��������ѭ�����á�����ѭ�����á������Ч�桢���ܻ�������Ҫ��ʩ������ɫ���ɡ����뼼���������ܹ���ѭ�����á��ģ���K2CO3��Һ��CO2��H2�⣬������______��
��4�������Ϊ2L�ĺϳ����У�����2mol?CO2��6mol?H2�����CO2��g����CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ���ӷ�Ӧ��ʼ��ƽ�⣬v��H2��=______����ʹƽ����ϵ��n��CH3OH��/n�� CO2������Ĵ�ʩ��______��
��5���罫CO2��H2��1��4������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4����֪CH4��g��+2O2��g��=CO2��g��+2H2O��l����H1=-890.3kJ/mol��H2?��g��+
O2��g��=H2O��l����H2=-285.8kJ/molд��CO2��g����H2��g����Ӧ����CH4��g����Һ̬ˮ���Ȼ�ѧ����ʽ______��
2������� ��16�֣�
I����ȡ��������Ӧ�Ļ�ѧ����ʽΪ��2SO2��g��ʮO2��g�� 2SO3��g��
2SO3��g��
��1���˷�Ӧ�ǹ�ҵ������ ����Ҫ���衣
��2���ܹ�˵���ں��º��������£�������Ӧ�Ѿ��ﵽ��ѧƽ��״̬���� ������ţ���
a��ÿ����1mol SO3��ͬʱ����0.5mol O2
b�������л��������ܶȲ���
c��SO2��O2��SO3�����ʵ���֮��Ϊ2��1��2
d��������������ѹǿ����
��3����400��ʱ����ѹ�£��ݻ�Ϊ1.0L���ܱ������г���1.00mol SO2(g)��0.96mol O2(g)����ַ�Ӧ��û���0.04mol SO2ʣ�࣬���ų�190.08KJ��������
�ٸ����й����ݣ�������ڹ�ҵ������ѡ��ѹ��Ӧ����ԭ��
��
��д���˷�Ӧ���Ȼ�ѧ����ʽ��
2SO2��g��ʮO2��g�� 2SO3��g�� ��H�� ��
2SO3��g�� ��H�� ��
��1����ij�¶��£���1.00 mol NH3����ˮ�����1.00 L��Һ�������Һ��OH��Ũ�Ⱥ�ʱ���ͼ�����£�
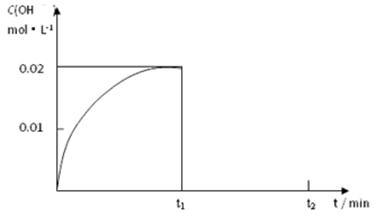
������¶�ʱ����ˮ�ĵ���ƽ�ⳣ��K�� ��
�� ��t1ʱ���ټ���H2O���2L��Һ����t2ʱ�����´ﵽƽ�⣬��������ϵ�л���t1��t2ʱ����OH��Ũ����ʱ��仯�����ߡ�
��2����a mol/L�������b mol/L��ˮ�������ϣ���Ϻ����Ϊ���ǰ���֮�ͣ���ַ�Ӧ��������Һ�����ԡ�
�� a b ���<������=����>����
�� ���������غ�ԭ�������Ϻ���Һ��ʣ�ఱˮŨ�ȣ�c(NH3��H2O)�� ��
���ú���a��b��ʽ�ӱ�ʾ��
3��ѡ���� ���������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ���ǣ� ? ��
A����֪C��ʯī��s���TC�����ʯ��s����H��0������ʯ��ʯī�ȶ�
B����֪C��s��+O2��g���TCO2��g����H1C��s��+1/2O2��g���TCO��g����H2�����H2����H1
C����֪2H2��g��+O2��g���T2H2O��g����H=-483.6kJ/mol����������ȼ����Ϊ241.8kJ/mol
D����֪NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.3kJ/mol����20gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��к���Ϊ28.65kJ/mol
4��ѡ���� N2��H2�ϳ�NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ��( )
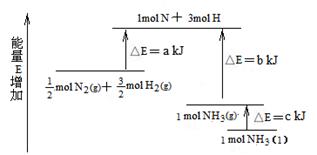
A��N2(g)��3H2(g) �� 2NH3(g) ����H �� 2(b��a) kJ/mol
B��N2(g)��3H2(g) �� 2NH3(l)����H �� 2(a��b��c) kJ/mol
C��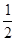 N2(g)��
N2(g)��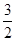 H2(g) �� NH3(l) ����H �� (b��c��a) kJ/mol
H2(g) �� NH3(l) ����H �� (b��c��a) kJ/mol
D��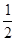 N2(g)��
N2(g)��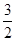 H2(g) ��NH3(g) ����H �� (a��b) kJ/mol
H2(g) ��NH3(g) ����H �� (a��b) kJ/mol