��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����22.68kJ�������Ȼ�ѧ����ʽ��ȷ����
[? ]
A��CH3OH��l��+3/2O2��g��== CO2��g��+2H2O��l�� ��H=+725.8 kJ/mol
B��2CH3OH��l��+3O2��g��== 2CO2��g��+4H2O��l�� ��H=��1452 kJ/mol
C��2CH3OH��l��+3O2��g��== 2CO2��g��+4H2O��l�� ��H=��725.8 kJ/mol
D��2CH3OH��l��+3O2��g��== 2CO2��g��+4H2O��l�� ��H=+1452 kJ/mol
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2������� �������ҹ��ĺ�����ҵȡ���˾�ijɾͣ��ں��췢��ʱ���£�N2H4�����������ﳣ��������ƽ�����
��1��Һ̬�������ȼ��ʱ����Һ̬N2O4��Ϸ���������ԭ��Ӧ����֪ÿ1g�³�ַ�Ӧ��������̬ˮ�ų�����ΪaKJ����д���÷�Ӧ���Ȼ�ѧ����ʽ______��
��2����ʵ�����У���N2H4?H2O��NaOH����һ�������ռ�114��116�����ּ�Ϊ��ˮ�£�
������������в���Ҫ��������______���������ĸ����
A���ƾ��� B����ֱ�������� C����ƿD��������
E��ţ�ǹܣ���Һ�ܣ� F��������ƿ G����ʽ�ζ���
�ڳ���������������⣬��ȱ�ٵIJ���������______��
��3������ʹ��¯�ڱڵ����⣨��Ҫ�ɷ�Fe2O3����ɴ�����������Fe3O4���㣬�ɼ�����¯��ʴ������Ӧ��������ת��Ϊ��������ÿ����1mol Fe3O4����Ҫ�����µ�����Ϊ______g��
��4��������������Fe3O4������ɿ�д��FeO?Fe2O3��ij��ѧʵ��С��ͨ��ʵ����̽��һ��ɫ��ĩ�Ƿ���Fe3O4��CuO��ɣ�������������ɫ���ʣ���̽���������£�
������裺����1����ɫ��ĩ��CuO������2����ɫ��ĩ��Fe3O4��
����3��______��
���̽��ʵ�飺
ȡ������ĩ��������ϡ�����У���������Һ�еμ�KSCN�Լ���
��������1��������ʵ��������______��
����������Һ��Ѫ��ɫ�������______������
��Ϊ��һ��̽����������������Һ�����������ۣ�������______�����������3������
����һС��ͬѧ��������������CuO�������٣����ܼ������ۺ�ʵ���������ԣ�
�������ϣ�Cu2+��������ˮ��Ӧ��������ɫ��Һ��Cu2++4NH3?H2O�TCu��NH3��42++4H2O��
��Ϊ̽���Ǽ���2���Ǽ���3��������ȡ������ĩ��ϡ�������ܽ���ټ���������ˮ��������2�����������______����������______���������3������
�ο��𰸣���1��N2O4��l��+2N2H4��l��=3N2��g��+4H2O��g�� Q
1gaKJ
64g 64aKJ
���Ը÷�Ӧ���Ȼ�ѧ����ʽΪ��N2O4��l��+2N2H4��l��=3N2��g��+4H2O��g����H1=-64a kJ?mol-1��
�ʴ�Ϊ��N2O4��l��+2N2H4��l��=3N2��g��+4H2O��g����H1=-64a kJ?mol-1��
��2������ʵ���õ��������У��ƾ��ƣ�������ƿ���¶ȼƣ��������������ܣ�ţ�ǹܣ��ձ���
����������в���Ҫ�������dz�ֱ�������ܡ���ʽ�ζ��ܣ�
����������������⣬��ȱ�ٵIJ����������¶ȼƣ�
�ʴ�Ϊ����BG�� ���¶ȼƣ�
��3����Fe3O4����д��FeO?Fe2O3����֪1��Fe3O4����2����Ϊ+3�ۣ�1����Ϊ+2�ۣ�������Fe2O3�γ�һ��Fe3O4�õ�1�����ӣ���ÿ����1mol Fe3O4��ת�Ƶ��ӵ����ʵ���Ϊ1mol��
����Fe2O3�γ�һ��Fe3O4�õ�1�����ӣ�1��N2H4���£�ת���N2�õ�4�����ӣ����ݵ��ӵ�ʧ�غ㣺n��Fe3O4����1=n��N2H4����4������n��N2H4��=0.25mol����m��N2H4��=0.25mol��32g/mol=8g��
�ʴ�Ϊ��8��
��4���������Ǻ�ɫ���壬Ҳ���ܼȺ���CuO�ֺ���Fe3O4��ɫ��ĩ����CuO��Fe3O4�Ļ���
�ʴ�Ϊ����ɫ��ĩ��CuO��Fe3O4�Ļ���
������������ͭ������Ӧ��CuO+H2SO4=CuSO4+H2O������ͭ��Һ����ɫ��������1������ʵ������Ϊ����Һ����ɫ��
�ʴ�Ϊ����Һ����ɫ��
��������������KSCN�Լ���ϳɺ�ɫ�����������������Һ��Ѫ��ɫ��֤��������������������������ӣ�˵����ɫ�����к���Fe3O4�����Լ���2��3���п��ܣ�
�ʴ�Ϊ��2��3��
��������ͭ���ӷ�����Ӧ��2Cu2++Fe=3Fe2++Cu���������������ɫ���ʣ�֤����Һ�д���ͭ���ӣ����ɫ�����к���CuO
���ʼ���3��ȷ��
�ʴ�Ϊ���к�ɫ����������
���������2����������������õ�����Һ�к������������ӣ����백ˮ�����������������ɫ�������������3����������������Һ�мȺ������������ӻ�����ͭ���ӣ�����������ˮ��Ӧ���������������ɫ������ͭ�����백ˮ������ӦCu2++4NH3?H2O�TCu��NH3��42++4H2O�������Ϊ����ɫ��
�ʴ�Ϊ�����ɫ���������ɫ������ͬʱ��Һ������ɫ��
���������
�����Ѷȣ�һ��
3������� ����ú��ƶ�͡����������ҹ���Դ��չ���ٵ���״��������Դ��������ţ���չ��ú���������ҹ���Դ�ṹ�ĵ���������Ҫ���塣��ͼ��ú������ҵ��֮һ��
���ྻú�������о����������൱�ձ飬������Աͨ�������ú������¯�н�����������ˮ�����ķ���������������ֵ�ܸߵ�ú̿�ϳ���������Ҫ�ɷ���CO��H2��CO��H2����Ϊ��Դ�ͻ���ԭ�ϣ�Ӧ��ʮ�ֹ㷺��
��1����֪��C(s)+O2(g)=CO2(g) ��H1����393.5 kJ��mol
�ο��𰸣�
���������
�����Ѷȣ�����
4������� (15��)��Դ�������������������ᷢչ������أ��о����ǵ��ۺ���������Ҫ���塣
��1����������ԭ���������������ת����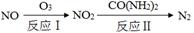
�ٷ�Ӧ��Ϊ��NO��O3��NO2��O2������11.2 L O2(��״��)ʱ��ת�Ƶ��ӵ����ʵ����� mol��
�ڷ�Ӧ���У���n(NO2)��n[CO(NH2)2]��3��2ʱ����Ӧ�Ļ�ѧ����ʽ�� ��
��2����������һ�ֹ��ϵ���������ķ�����ͬʱʵ���˵��������ѭ��ת������Ҫ��ӦΪ��NO2(g)��SO2(g) SO3(g)��NO(g) ��H����41.8 kJ��mol��1��֪��2SO2(g)��O2(g)
SO3(g)��NO(g) ��H����41.8 kJ��mol��1��֪��2SO2(g)��O2(g) 2SO3(g) ��H����196.6 kJ��mol��1д��NO��O2��Ӧ����NO2���Ȼ�ѧ����ʽ ��
2SO3(g) ��H����196.6 kJ��mol��1д��NO��O2��Ӧ����NO2���Ȼ�ѧ����ʽ ��
��3��ij��ѧ��ȤС�鹹�뽫NOת��ΪHNO3��װ������ͼ���缫Ϊ����Բ��ϡ����ĵ缫��Ӧʽ�� ��

��4����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)��
CH3OCH3(g)+3H2O(g)��
�ٸ÷�Ӧƽ�ⳣ������ʽΪK�� ��
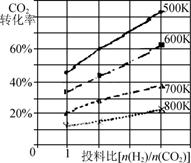
����֪��ijѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ת������ͼ��ʾ���÷�Ӧ�Ħ�H________(�>������<������)0��
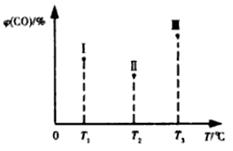
��5���ϳ���CO��H2��һ���������ܷ������·�Ӧ��CO(g) +2H2(g) CH3OH(g) ��H<0�����ݻ���ΪVL��I����������ͬ�ܱ������зֱ����amol CO��2a mol H2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�t minʱCO�����������ͼ��ʾ����ʱI��������������һ���ﵽ��ѧƽ��״̬���� �������������ڵķ�Ӧ���ﵽ��ѧƽ��ʱ��COת�������ķ�Ӧ�¶��� ��
CH3OH(g) ��H<0�����ݻ���ΪVL��I����������ͬ�ܱ������зֱ����amol CO��2a mol H2�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�t minʱCO�����������ͼ��ʾ����ʱI��������������һ���ﵽ��ѧƽ��״̬���� �������������ڵķ�Ӧ���ﵽ��ѧƽ��ʱ��COת�������ķ�Ӧ�¶��� ��
�ο��𰸣��Ţ�1��2�֣���6NO2��4CO(NH2)2��7N2��8H2O��4CO2��2�֣�
��2NO(g)+O2(g) �� 2NO2(g) ��H����113.0 kJ/mol��2�֣� ��NO��3e����2H2O��NO3����4H+��2�֣�
�Ȣ�c(CH3OCH3)��c3(H2O)]/[c2(CO2)��c6(H2) ��2�֣� ��< ��2�֣� �ɢ�2�֣���T1��1�֣�
�����������1����������ԭ���������������ת����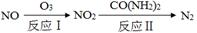
�ٱ�״����11.2L���������ʵ�����0.5mol������ݷ�ӦNO��O3��NO2��O2��֪����11.2 L O2ʱ������NO��0.5mol����Ԫ�صĻ��ϼ۴ӣ�2�����ߵ���4�ۣ�ʧȥ2�����ӣ�����ת�Ƶ��ӵ����ʵ�����0.5mol��2��1mol��
�ڷ�Ӧ���У���n(NO2)��n[CO(NH2)2]��3��2ʱ������ԭ���غ��֪�������ɵ����⣬����CO2��ˮ���ɣ����Է�Ӧ�Ļ�ѧ����ʽ��6NO2��4CO(NH2)2��7N2��8H2O��4CO2��
��2����֪����NO2(g)��SO2(g) SO3(g)��NO(g) ��H����41.8 kJ��mol��1����2SO2(g)��O2(g)
SO3(g)��NO(g) ��H����41.8 kJ��mol��1����2SO2(g)��O2(g) 2SO3(g) ��H����196.6 kJ��mol��1������ݸ�˹���ɿ�֪�ڡ��١�2���ɵõ�NO��O2��Ӧ����NO2���Ȼ�ѧ����ʽ2NO(g)+O2(g) �� 2NO2(g) ��H����113.0 kJ/mol��
2SO3(g) ��H����196.6 kJ��mol��1������ݸ�˹���ɿ�֪�ڡ��١�2���ɵõ�NO��O2��Ӧ����NO2���Ȼ�ѧ����ʽ2NO(g)+O2(g) �� 2NO2(g) ��H����113.0 kJ/mol��
��3��ԭ����и���ʧȥ���ӣ�����������Ӧ�����NO�ڸ���ͨ��ʧȥ����ת��Ϊ��������缫��Ӧʽ��NO��3e����2H2O��NO3����4H+��
��4����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)��
CH3OCH3(g)+3H2O(g)��
�ٻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪�÷�Ӧƽ�ⳣ������ʽΪK��c(CH3OCH3)��c3(H2O)]/[c2(CO2)��c6(H2)��
�ڸ���ͼ���֪��Ͷ�ϱ���ͬ�������£������¶�CO2��ת���ʽ��ͣ���˵�������¶�ƽ�����淴Ӧ������У���������Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ�Ħ�H<0��
��5�����ŷ�Ӧ�Ľ���CO�����ģ��������ͣ����ﵽƽ��״̬�Ժ�CO�ĺ�����͡���������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ������У�����CO�ĺ�������������ͼ���֪I��������������CO��ߵ��Ǣ���͵��Ǣ���˵���¶���T1��T2ʱCO�ĺ������ͣ���Ӧ������Ӧ������У���Iһ��û�дﵽƽ��״̬���¶���T2��T3ʱCO�ĺ������ߣ�˵����Ӧ���淴Ӧ������У����Ԣ�һ����ƽ��״̬�����������ƽ��״̬������һ���ﵽ��ѧƽ��״̬���Ǣ��¶ȵ�������CO��ת�������������������ڵķ�Ӧ���ﵽ��ѧƽ��ʱ��COת�������ķ�Ӧ�¶���T1��
���㣺����������ԭ��Ӧ����˹���ɡ����������ƽ��״̬��Ӱ��ͼ����Լ��缫��Ӧʽ��
�����Ѷȣ�����
5��ѡ���� �Ȼ�ѧ����ʽC��s��+H2O��g��
?CO��g��+H2��g������H=+131.3kJ/mol��ʾ��������
A��̼��ˮ��Ӧ����131.3kJ����
B��1mol̼��1molˮ��Ӧ����һ����̼������������131.3kJ����
C��1mol��̬̼��1molˮ������Ӧ����һ����̼�����������������131.3kJ
D��1����̬̼ԭ�Ӻ�1����ˮ������Ӧ����131.1kJ
�ο��𰸣�C
���������
�����Ѷȣ���