微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g);ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g);ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
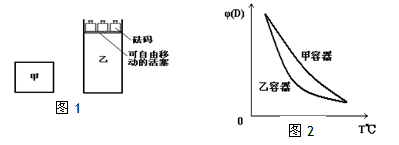
关于两容器中反应的说法正确的是
A.甲容器中的反应先达到化学平衡状态
B.两容器中反应均达平衡后,平衡体系中各组分的体积百分组成相同,浓度也相同
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示
D.在甲容器中再充入2?mol?A和2?mol?B,平衡后甲中c(C)是乙中c(C)的2倍
参考答案:BD
本题解析:A 错误,乙中的反应等价于起始状态下的4摩尔A和4摩尔B的反应,甲恒容,乙恒压,由于该反应是气体体积数不变的反应,所以甲乙两容器自始至终各成分的浓度均相等,正逆反应速度任何时刻均相等,故甲乙两容器应同时达到化学平衡状态
B 正确 上述分析知甲乙两容器达到的平衡状态完全相同,故平衡体系中各组分的体积百分组成相同,浓度也相同
C 错误 两容器达平衡后升高相同的温度时,平衡左移两容器中物质D的体积分数随温度变化的情况也相同
D 正确 设想另有一与甲完全相同的容器,在相同条件下完成上述反应,此时平衡状态与甲应完全相同,再假想把该容器中的反应混合物挤入甲容器中,于是相当于给甲加压并使其容积减小一半,平衡不移动,但平衡混合物中各成分的浓度都增大到原来的2倍,即平衡后甲中c(C)是乙中c(C)的2倍
本题难度:一般
2、选择题 在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)  2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是
2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是
A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态
B.15℃时氨基甲酸铵的分解平衡常数为2.048×10-9(mol/L)3
C.恒温下压缩体积,NH3的体积分数减小
D.再加入一定量氨基甲酸铵,可加快反应速率
参考答案:B
本题解析:A、反应物为固体,生成物全部为气体,从反应开始到平衡状态,气体的平均相对分子质量始终是(2×17+44)/3=26,错误;B、15℃时,平衡气体总浓度为2.4×10-3mol/L,则平衡时氨气浓度是1.6×10-3mol/L,二氧化碳浓度是0.8×10-3 mol/L,K=c2(NH3)c(CO2)=2.048×10-9(mol/L)3,正确;C、恒温下压缩体积,压强增大,平衡虽然逆向移动,但NH3与CO2的物质的量比始终是2:1,所以NH3的体积分数不变,正确;D、氨基甲酸铵是固体,再加入一定量氨基甲酸铵,对反应速率无影响,错误,
答案选B。
本题难度:一般
3、选择题 在蒸发皿中蒸 干并灼烧(低于400 ℃)下列物质的溶液,可以得到该溶质的是(? )
A.氯化铝
B.碳酸氢钠
C.硫酸镁
D.高锰酸钾
参考答案:C
本题解析:当加热蒸干时,AlCl3发生水解:2AlCl3+3H2O 2Al(OH)3↓+6HCl↑;
2Al(OH)3↓+6HCl↑;
NaHCO3受热分解:2NaHCO3 Na2CO3+CO2↑+H2O;KMnO4受热分解:2KMnO4
Na2CO3+CO2↑+H2O;KMnO4受热分解:2KMnO4 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
本题难度:一般
4、填空题 1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g)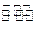 Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。
则5分钟内H2的平均反应速率为?。
(2)能说明该反应已达到平衡状态的是____(填序号)。
a.容器内压强保持不变? b.容器内气体密度保持不变
c.c(H2)=c(H2O)? d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)
①加入少量Na2SO4固体,则平衡:?②加入少量灼热的碳粉,则平衡:__?
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性___?_,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是?。
参考答案:

本题解析:略
本题难度:一般
5、填空题 在一定温度下有甲、乙两容积相等的密闭容器
(1) 向甲容器中通入1mol N2和3 mol H2,反应达到平衡时,生成NH3 amol。此时,NH3的质量分数是________。(用含有“a”的表达式表示)。
(2) 若起始时(两容器容积保持不变)。向乙中通入2mol N2和6mol H2,达到平衡时,生成的NH3的物质的量为b mol, (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(3) 若起始时甲保持容积不变,向甲容器中通入1mol N2和3 mol H2,反应达到平衡时,生成NH3 amol,而乙保持压强不变, 向乙容器中通入1mol N2和3 mol H2,反应达到平衡时,生成NH3 b mol,则a _______b(选填“>”、“<”或“=”)
参考答案:(1) a/2
(2) <
(3)? <
本题解析:
本题难度:一般