微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 在常压和500℃时把O2和SO2按?1:2?体积比混合,如果混合前O2有?10mol,平衡时SO3占总体积的91%,求:
(1)平衡时有多少摩O2转化?
(2)混合气中SO2的体积分数.
(3)SO2的转化率.
(4)若保持与前面相同的条件,改用20molSO3代替O2和SO2,则达平衡时O2的体积分数为多少?
参考答案:令参加反应的氧气的物质的量为nmol,根据三段式解题法,用n表示求出混合气体各组分物质的量的变化量、平衡时各组分的物质的量.?
? 2SO2(g)+O2(g)
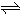
2SO3(g).
开始(mol):20?10?0
变化(mol):2n?n?2n
平衡(mol):20-2n?10-n?2n?
(1)平衡时SO3占总体积的91%,所以2n20-2n+10-n+2n×100%=91%
解得,n=9.38
答:平衡时有9.38molO2转化.
(2)混合气中SO2的体积分数为20-2×9.3830-9.38×100%=6%.
答:混合气中SO2的体积分数为6%.
(3)SO2的转化率为2×9.3820×100%=93.8%.
答:SO2的转化率为93.8%.
(4)与原平衡等效,所以平衡时O2体积分数为10-9.3830-9.38×100%=3%.
答:平衡时O2体积分数为3%.
本题解析:
本题难度:一般
2、选择题 在一定条件下,对于反应mA(g)+nB(g) 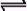 cC(g)+dD(g),C物质的体积分数(C%)与温度、压强的关系如图所示.
cC(g)+dD(g),C物质的体积分数(C%)与温度、压强的关系如图所示.

下列判断正确的是
A.ΔH<0 m+n>c+d
B.ΔH<0 m+n<c+d
C.ΔH>0 m+n>c+d
D.ΔH>0 m+n<c+d
参考答案:B
本题解析:由图分析可知,在相同温度下,压强越大C%越小,即增大压强,平衡向逆反应方向移动,即逆反应方向为气体体积减少的方向,得m+n<c+d;在相同压强下,随温度的升高C%减少,即升高温度C%减少即正反应方向为放热反应,ΔH<0;所以正确选项为B;
本题难度:一般
3、选择题 在一密闭容器中,反应 mA(s)+nB(g)  pC(g),达到平衡时,测得c(C)为0.5 mol・L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(C)为0.3 mol・L-1。则下列判断正确的是(?)
pC(g),达到平衡时,测得c(C)为0.5 mol・L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(C)为0.3 mol・L-1。则下列判断正确的是(?)
A.化学计量数:m+n>p? B.平衡向逆反应方向移动了
C.物质B的转化率减小了? D.物质C的质量分数增加了
参考答案:D
本题解析:将容器体积扩大一倍的瞬间c(C)为0.25 mol・L-1;,但平衡后c(C)为0.3 mol・L-1,说明平衡向正反应方向移动,所以n小于p,因此正确的答案是D。
本题难度:一般
4、简答题 在?2L的密闭容器中,充入?1mol?N2?和?3mol?H2,在一定的条件下反应,2?分钟后达到平衡状态,相同温度下,测得平衡时混合气体的压强比反应前混合气体的压强减小了?1/10,计算:
(1)平衡时混合气体中三种气体的物质的量比为多少?
(2)N2?的转化率为多少?
(3)2分钟内,NH3?的平均反应速率为多少?
参考答案:根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量.
令参加反应的氮气的物质的量为nmol,则:
? N2 +3H2

2NH3 ,
开始(mol):1 ? 3 ? 0
变化(mol):n ? 3n ? 2n
平衡(mol):1-n? 3-3n? 2n
压强之比等于物质的量之比,所以(1-n+3-3n+2n)mol=(1+3)mol×(1-110),解得n=0.2,
(1)平衡时n(N2)=(1-n)mol=(1-0.2)mol=0.8mol
平衡时n(H2)=(3-3n)mol=(3-3×0.2)mol=2.4mol
平衡时n(NH3)=2n=0.2mol×2=0.4mol
所以,平衡时混合气体中N2、H2、NH3三种气体的物质的量比为0.8mol:2.4mol:0.4mol=2:6:1.
答:平衡时混合气体中N2、H2、NH3三种气体的物质的量比为2:6:1.
(2)N2?的转化率为0.2mol1mol×100%=20%
答:N2?的转化率为20%.
(3)2分钟内,以NH3?表示的平均反应速率v(NH3)=0.2mol×22L2min=0.1 mol/L?min.
答:2分钟内,以NH3?表示的平均反应速率为0.1 mol/L?min.
本题解析:
本题难度:一般
5、选择题 对于反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A.K=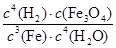
B.K=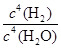
C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D.改变反应的温度,平衡常数不一定变化
参考答案:B
本题解析:化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应式3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)可知,该反应的平衡常数K=
Fe3O4(s)+4H2(g)可知,该反应的平衡常数K=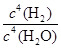 ,A不正确,B正确;C、平衡常数只与温度有关系,所以增大c(H2O)或减小c(H2),该反应的平衡常数不变,C不正确;D、平衡常数只与温度有关系,所以改变反应的温度,平衡常数一定变化,D不正确,答案选B。
,A不正确,B正确;C、平衡常数只与温度有关系,所以增大c(H2O)或减小c(H2),该反应的平衡常数不变,C不正确;D、平衡常数只与温度有关系,所以改变反应的温度,平衡常数一定变化,D不正确,答案选B。
本题难度:一般